
题目列表(包括答案和解析)
25.(5分)本题相对分子质量用以数据:Na2O 62.0 Na2O2 78.0 NaOH 40.0
(1)Na2O和Na2O2的混合物140mg和足量水作用,得到400mL溶液,其中含溶质160mg。
试计算原混合物中Na2O2的质量和所得溶液在常温下的pH。
24.(12分)化合物A是石油化工的一种重要原料,用A和水煤气为原料经下列途径合成化合物D(分子式为C3H6O3)。
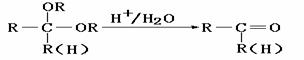
已知:
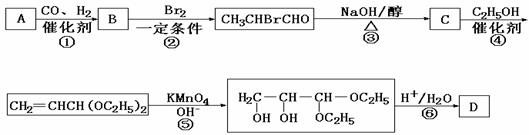
请回答下列问题:
(1)写出下列物质的结构简式:
A:__________;B:____________;C:_____________;D:___________。
(2)指出反应②的反应类型______________________。
(3)写出反应③的化学方程式___________________________________________。
(4)反应④的目的是___________________________________________________。
(5)化合物D’是D的一种同分异构体,它最早发现于酸牛奶中,是人体内糖类代谢的中间产物。D’在浓硫酸存在的条件下加热,既可以生成能使溴水褪色的化合物E(C3H4O2),又可以生成六原子环状化合物F(C6H8O4)。请分别写出D’生成E和F的化学方程式:
D’→E:___________________________________________________________。
D’→F:___________________________________________________________。
23.(6分)实验测得某烃中碳元素的质量分数为91.3%,相对分子质量为92,则该烃的分子式为____________。若该烃为芳香烃,在其分子的“C-C”键或“H-C”键中
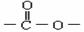
插入基团“ ”可形成六种含苯环的酯,请写出其中四种酯的结构简式:
__________________________________、____________________________________、
__________________________________、____________________________________。
22.(12分)物质M、N、A、B、C、D、E、F、G、H,其中C、H为常见金属,且混合气体A在常温下不与空气接触时能发生如图所示变化(其他有关反应条件均略去):
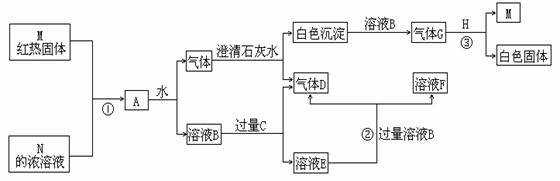
试回答:
(1)写出C、D和H的化学式: C:_____________;D_______________;H______________。
(2)写出反应①②③的化学方程式:
①____________________________________________________________。
②____________________________________________________________。
③____________________________________________________________。
21.(9分)短周期主族元素A、B、C、D的原子序数依次增大,其中A、C同主族,B、C、D同周期,A原子的最外层电子数是次外层电子数的3倍,B是短周期元素中原子半径最大的主族元素。试回答下列问题:
(1)A的元素符号_____________; D的原子结构示意图____________。
(2)A、B、C三种元素形成的简单离子的半径由大到小的顺序是____________________;
(3)A、B、C、D形成的化合物B2A2、CD2、D2A、DA2中.各原子都满足最外层8电子结构的是_______________________ (请填写具体的化学式)。
(4)CA2与D元素的单质在水溶液中反应的化学方程式是_________________________。
20.(11分)(1)实验室利用下图装置检验浓硫酸和木炭粉在加热条件下反应所得全部产物。
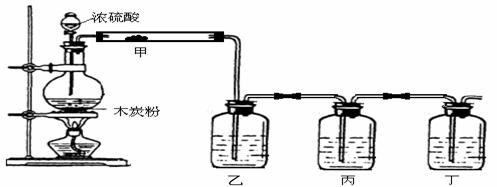
请回答:
①装置甲中应加的试剂是_________________;
②装置乙、丙和丁中所加试剂分别是___________(填下列选项的字母序号);
A.澄清石灰水、品红溶液、高锰酸钾酸性溶液
B.品红溶液、高锰酸钾酸性溶液、澄清石灰水
C.高锰酸钾酸性溶液、品红溶液、澄清石灰水
D.澄清石灰水、高锰酸钾酸性溶液、品红溶液
③实验时为了确保丁所验证的结论正确,丙中应观察到的现象是__________________。
(2)某校化学兴趣小组为测定混合物组成的质量比,实验过程中所加试剂和操作步骤如下表所示:
|
实验 序号 |
混合物A |
加入适量水得到 |
加入试剂B |
过滤后经洗涤干燥所得固体C |
蒸发滤液得到晶体D |
称量 |
|
Ⅰ |
BaCl2 NaCl |
溶液 |
过量CO2 |
 |
D |
A、D |
|
Ⅱ |
CaCl2 NaCl |
溶液 |
过量饱和Na2CO3溶液 |
CaCO3 |
NaCl |
A、C |
|
Ⅲ |
Na2SO4 MgSO4 |
溶液 |
|
|
|
|
试回答下列问题:
①实验Ⅰ中D的成分是_____________,通过称量后_______(填“能”或“不能”)计算得到A中各组分的质量比。
②实验Ⅱ填写的内容中一定错误的是___________,其原因是______________________。
③对实验Ⅲ进行设计,并将相应内容填入Ⅲ中对应的空格内。
19.(9分)在实验室利用胆矾晶体和烧碱溶液制备氧化铜固体,其实验操作可分解为如下几步:①混合 ②过滤 ③加热分解 ④溶解 ⑤洗涤。就此实验完成下列填空:
⑴正确操作步骤的顺序是(填序号) ;
⑵步骤②中所用到的玻璃仪器有 ;
⑶在实验中多次用到玻璃棒,其作用有三个,分别是 、 、 。
18.已知相同条件时碳酸中c(CO32-)比偏铝酸中c(AlO2-)大得多,则下列推论中正确的是( )
A.少量CO2通入NaAlO2溶液中,肯定有CO32-生成
B.含CO32-的溶液容易使Al(OH)3溶液变成AlO2-
C.HCO3-只能跟Al3+反应而不能和AlO2-反应
D.NH4+、AlO2-和HCO3-能大量共存于同一溶液中
第II卷(非选择题共78分)
17.常温时0.1mol·L-1HA溶液的pH>1,0.1mol·L-1BOH溶液中c(OH-):c(H+)=1012,将两溶液等体积混合,以下判断正确的是( )
A. c(H+)< c(OH-)< c(A-)< c(B+)
B. c(OH-)< c(H+)< c(B+) < c(A-)
C. c(H+)+ c(B+)= c(A-)+ c(OH-)
D. c(A-)= c(B+)> c(H+)= c(OH-)
16.不用其他试剂无法鉴别的一组溶液是( )
A.硝酸银溶液和稀氨水 B.硫酸钠溶液和氯化钠溶液
C.碳酸钠溶液和稀盐酸 D.氯化铁溶液和氯化铜溶液
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com