
题目列表(包括答案和解析)
2.通过钠与水反应的现象及实质的学习,能正确分析钠与酸溶液、盐溶液、碱溶液反应时的 现象及实质.
1.通过钠的化学性质的学习,能正确分析钠长久露置于空气中发生的一系列变化的现象和原 理.
3.碳酸钠和碳酸氢钠的性质和制法:
|
名称和化学式 |
碳酸钠(Na2CO3) |
碳酸氢钠(NaHCO3) |
|
俗名 |
纯碱、苏打 |
小苏打 |
|
颜色和状态 |
白色晶体 |
白色粉末 |
|
水中溶解性 |
易溶 |
易溶(比Na2CO3I小) |
|
热稳定性 |
稳定 |
不稳定 2NaHCO3 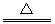 Na2CO3+CO2↑+H2O Na2CO3+CO2↑+H2O |
|
与酸反应 |
CO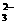 +H+ +H+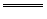 HCO HCO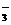 HCO 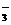 +H+ +H+ H2O+CO2↑ H2O+CO2↑ |
HCO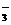 +H+ +H+ CO2↑+H2O CO2↑+H2O |
|
与某些碱反应 |
CaCl2+Na2CO3 BaCO3↓+2NaOH BaCO3↓+2NaOH |
NaHCO3+Ca(OH)2 CaCO3↓+NaOH+H2O CaCO3↓+NaOH+H2O2NaHCO3+Ca(OH)2  CaCO3↓+Na2CO3+2H2O CaCO3↓+Na2CO3+2H2O |
|
与某些盐反应 |
CaCl2+Na2CO3BaCO3↓+2NaCl |
NaHCO3+NaHSO4Na2SO4 +H2O+CO2↑ |
|
与CO2反应 |
Na2CO3+CO2+H2O 2NaHCO3 2NaHCO3 |
不反应 |
|
相互转化 |
NaCO3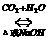 NaHCO3 NaHCO3 |
|
|
制法 |
NaOH+CO2 NaHCO3 NaHCO32NaHCO3  2Na2CO3+H2O 2Na2CO3+H2O+CO2↑ |
NaOH+CO2 NaHCO3 NaHCO3 |
|
鉴别 |
加酸产生CO2 加热难分解 |
加酸产生CO2较Na2CO3快 加热分解出CO2 |
|
用途 |
制玻璃、肥皂、造纸、纺织 |
发酵粉、治胃酸过多 |
2.钠的氧化物和氢氧化物的性质和制法:
|
名称和化学式 |
氧化钠(Na2O) |
过氧化钠(Na2O2) |
氢氧化钠(NaOH) |
|
颜色和状态 |
白色固体 |
淡黄色固体 |
无色固体 |
|
类别 |
碱性氧化物 离子化合物 |
过氧化物 离子化合物 |
碱 离子化合物 |
|
电子式 |
Na+[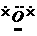 ]Na+ ]Na+ |
Na+[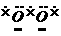 ] ] |
Na+[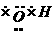 ] ] |
|
氧元素化合价 |
-2 |
-1 |
-2 |
|
化学键 |
离子键 |
离子键 非极性键 |
离子键 极性键 |
|
稳定性 |
不稳定 |
比Na2O稳定 |
稳定 |
|
与水反应 |
Na2O+2HCl 2NaOH 2NaOH |
2Na2O2+2H2O 4Na 4NaOH+O2↑ |
不反应 |
|
与酸反应 |
Na2O+2HCl 2NaCl 2NaCl+H2O |
2Na2O2+4HCl 4Na 4NaCl+O2↑2H2O |
NaOH+HCl NaCl+H2O NaCl+H2O |
|
与酸酐反应 |
Na2O+CO2 Na2CO3 Na2CO3 |
2Na2O2+2CO2 2Na2CO3 2Na2CO3+O2↑ |
2NaOH+CO2 Na2CO3+H2O Na2CO3+H2ONaOH+CO2  NaHCO3 NaHCO3 |
|
与盐溶液反应 |
Na2O+2NaHSO4 2Na2SO4+H2O Na2O+H2O+CuSO4  Cu(OH)2↓+Na2SO4 |
2Na2O2+4NaHSO4 4Na2SO4+O2↑+2H2O 2Na2O2+H2O+CuSO4  Cu(OH)2↓+2Na2SO4+O2 |
NaOH+NaHSO4 Na2SO4+ Na2SO4+H2O 2NaOH+CuSO4  Cu(OH)2↓+Na2SO4 Cu(OH)2↓+Na2SO4 |
|
用途 |
制氢氧化钠 |
漂白剂、供氧剂、 氧化剂 |
化工原料、制纸浆、肥皂 |
1. 碱金属元素原子结构、单质性质、制法:
|
名称和符号 |
锂(Li) |
钠(Na) |
钾(K) |
铷(Rb) |
铯(Cs) |
||
|
|
原子序数 |
3 |
11 |
19 |
37 |
55 |
|
|
结 构 |
原子结构结构简图 |
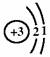 |
 |
 |
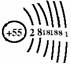 |
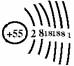 |
|
|
电子式 |
Lix |
Nax |
Kx |
Rbx |
Csx |
||
|
主要化合价 |
+1 |
+1 |
+1 |
+1 |
+1 |
||
|
相同点 |
最外层电子数相同,都是1个电子 |
||||||
|
不同点 |
原子核外电子层数不同,依次增多 |
||||||
|
原子半径 |
依次递增 |
||||||
|
离子半径 |
依次递增 |
||||||
|
金属活动性 |
依次递增 |
||||||
|
质还原性 |
依次递增 |
||||||
|
阳离子氧化性 |
依次递减 |
||||||
|
物理性质 |
颜色和状态 |
银白色固体 |
|||||
|
密度 |
0.534g/cm3 |
0.97g/cm3 |
0.86g/cm3 |
1.523g/cm3 |
1.879g/cm3 |
||
|
熔点 |
依次递减 |
||||||
|
沸点 |
依次递减 |
||||||
|
化学性质 |
跟氧气反应 |
4Li+O2 2Li2O |
4Na+O2 2Na2O 2Na+O2  Na2O2 |
2K+O2 K2O2 K+O2  KO2 |
Rb+O2 RbO2 |
Cs+O2 CsO2 |
|
|
跟卤素反应 |
2M+X2 2MX(M、X2表示碱金属、卤素) 2MX(M、X2表示碱金属、卤素) |
||||||
|
跟硫反应 |
2M+S M2S M2S |
||||||
|
与水反应 |
2M+2H2O 2MOH+H2↑ 反应剧烈程度:Li<Na<K<Rb<Cs 2MOH+H2↑ 反应剧烈程度:Li<Na<K<Rb<Cs |
||||||
|
与酸反应 |
2M+2H+ 2M++H2↑ 2M++H2↑ |
||||||
|
与盐溶液反应加(CuSO4) |
|
||||||
|
制法 |
2MCl 2M+Cl2↑(K:Na+KCl 2M+Cl2↑(K:Na+KCl K+NaCl) K+NaCl) |
||||||
3.掌握碱金属的性质,理解碱金属原子结构与性质递变规律,掌握用焰色反应检验金属钠和 钾及其离子的操作技能.
2.掌握钠的氧化物的性质,钠的重要化合物的用途及Na2CO3与NaHCO3的联系与区别.
1.掌握钠的重要性质,了解钠的保存和重要用途.
21.(本题共12分)
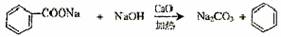 (1)
(1)

(2)
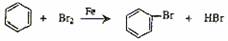
(或其它合理答案)
(3)稳定 (4)a d (5)介于单键和双键之间的特殊的键(或其它合理答案)
21.(本题共12分)
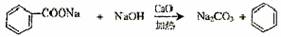 (1)
(1)

(2)
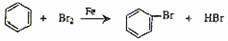
(或其它合理答案)
(3)稳定 (4)a d (5)介于单键和双键之间的特殊的键(或其它合理答案)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com