
题目列表(包括答案和解析)
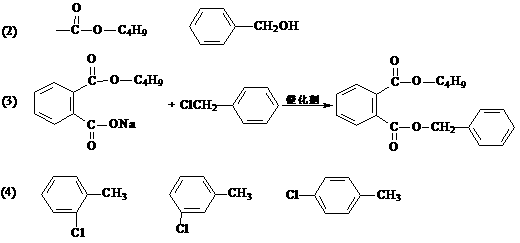
13.(1) 取代 酯化
16.(14分)取A、B两份物质的量浓度相等的NaOH溶液,体积均为50mL,分别向其中通入一定量的CO2后,再分别稀释为100mL
(1)在NaOH溶液中通入一定量的CO2后,溶液中溶质的组成可能是:
①______________②_____________③_____________④_____________
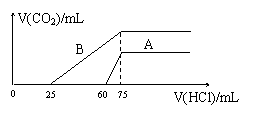 (2)在稀释后的溶液中分别逐滴加入0.1mol/L的盐酸,产生CO2的体积(标准状况)与所加盐
(2)在稀释后的溶液中分别逐滴加入0.1mol/L的盐酸,产生CO2的体积(标准状况)与所加盐
酸的体积关系如图所示:
①分别加入足量的盐酸后,溶液中的溶质是_______________,原NaOH溶液的物质的量浓度为__________________mol/L。
②A曲线表明,原溶液通入CO2后,所得溶质与HCl反应产生CO2的最大体积是_____________mL(标准状况)。
③B曲线表明,原溶液通入CO2后,所得溶质的化学式为____________,其物质的量之比为____________________。
非选择答案:
15. (14分)甲、乙、丙、丁四种单质在点燃的条件下反应生成X、Y、Z、W四种化合物,转化关系如右图所示。又知:①甲、乙、丙均为短周期元素的单质,常温下均为气态,丁是日常生活中的常见金属;②常温下,X是无色液体,Y是黑色固体;③丙在乙中燃烧发生苍白色火焰,丁在乙中燃烧生成棕色烟,W的水溶液呈黄色。
(14分)甲、乙、丙、丁四种单质在点燃的条件下反应生成X、Y、Z、W四种化合物,转化关系如右图所示。又知:①甲、乙、丙均为短周期元素的单质,常温下均为气态,丁是日常生活中的常见金属;②常温下,X是无色液体,Y是黑色固体;③丙在乙中燃烧发生苍白色火焰,丁在乙中燃烧生成棕色烟,W的水溶液呈黄色。
请填空:
(1)丁在甲和X同时存在的条件下,容易被腐蚀,写出电极反应式:
负极:__________________________ 正极:_________________________________
(2)将饱和W的溶液滴入到热的X中煮沸几分钟,反应的化学方程式为
__________________________________________________________________________。
(3)Y与足量的稀HNO3反应的离子方程式为:
__________________________________________________________________________。
(4)在一定条件下,丁分别Y、Z反应生成等物质的量的丙时,消耗丁的物质的量之比
为___________。
14.(20分)如图所示,是一个制取氯气并以氯气为原料进行特定反应的装置,其中各试剂瓶装的试剂为:B(氢硫酸)、C(碘化钾淀粉溶液)、D(水)、F(紫色石蕊试液)。
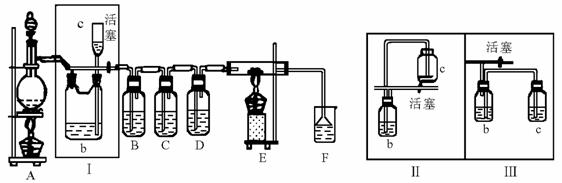
(1)A是氯气发生装置,其化学反应方程式可以是:__________________________________。
(2)Ⅰ中b瓶内宜加入的液体一般是____________。怎样检验这一部分装置的气密性_____
__________________________________。
(3)用图示的Ⅱ或Ⅲ代替Ⅰ是否可行?________。简要说明理由________________________
__________________________________。
(4)实验开始时,先点燃A处酒精灯,打开分液漏斗旋塞和Ⅰ处活塞,让氯气充满整个装置,再点燃E处酒精灯,回答下列问题:
①怎么证明氯气已充满了整个装置___________________________________________。
②下列装置中的现象是B_____________________,C_____________________。
(5)E装置的硬质玻璃管内盛有炭粉,发生氧化还原反应,其产物为二氧化碳和氯化氢,写出E中反应的化学方程式_______________________________________________。
(6)在F处,紫色石蕊试液的颜色由紫色变为红色,再变为无色,其原因是_____________
____________________________________________________________________。
13.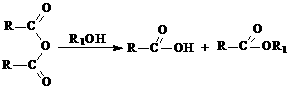 (16分)某有机物J(C19H20O4)不溶于水,毒性低,与聚氯乙烯、聚乙烯等树脂具有良好相容性,是塑料工业主要增塑剂,可以用下列方法合成。
(16分)某有机物J(C19H20O4)不溶于水,毒性低,与聚氯乙烯、聚乙烯等树脂具有良好相容性,是塑料工业主要增塑剂,可以用下列方法合成。
已知:
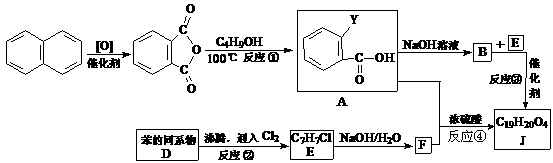
合成路线为:
上述流程中:(i)反应A→B仅发生中和反应,(ii)F与浓溴水混合不产生白色沉淀。
(1)指出反应类型:反应②____________________,反应④_____________________。
(2)写出结构简式:Y____________________________,F______________________。
(3)写出B+E→J的化学方程式:___________________________________________。
(4)写出E的属于芳香烃衍生物的同分异构体的结构简式:____________________、
____________________、____________________。
12.氢是重要而洁净的能源,要利用氢气作能源,必须安全有效地储存氢气。有报道称某种合金材料有较大的储氢容量,其晶体结构的最小单元如图所示。则这种合金的化学式:
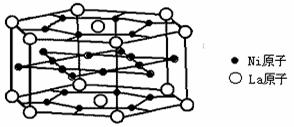
A.LaNi3 B.LaNi4 C.LaNi5 D.LaNi6
第二卷(非选择题,共64分)
11.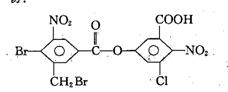 已知苯环上由于取代基的影响,使与硝基邻位上的卤原子的反应活性增强。1mol有机物:与足量的NaOH溶液混合,在一定的条件下反应共消耗NaOH物质的量为
已知苯环上由于取代基的影响,使与硝基邻位上的卤原子的反应活性增强。1mol有机物:与足量的NaOH溶液混合,在一定的条件下反应共消耗NaOH物质的量为
A.4mol B.6mol C.8mol D.10mol
10.10月13日有关媒体报道天津巨能化学有限公司生产的巨能钙含有双氧水,经农业部产品质量监督检验测试中心检测,部分送检品种不同程度地含双氧水。双氧水属于危险化学品及有毒有害物质,以前也曾作为漂白剂、杀菌剂、防腐剂广泛用于食品中。下列有关H2O2的叙述中正确的是
A.H2O2是二元弱酸,将H2O2溶液滴入含有酚酞的NaOH溶液中,红色消失,一定是因为发生了酸碱中和反应
B.H2O2分子中含有非极性键,因此H2O2是非极性分子
C.H2O2的自然分解过程非常缓慢,一般不易察觉,但正因为如此,一般药用的双氧水在贮存期间也会逐渐失效
D.人体中含有过氧化氢酶,过氧化氢酶可以使H2O2分解,因此人体即使吸收多量的H2O2也没有关系,可以被过氧化氢酶分解为无毒物质
9.将一定量的Fe、Fe2O3、CuO的混合物放入体积为100mL、浓度为2.2mol·L-1的H2SO4溶液中,充分反应后,生成气体896mL(标况),得到不溶固体1.28g,过滤后,滤液中的金属离子只有Fe2+(假设滤液体积仍为100mL)。向滤液滴加2mol·L-1的NaOH溶液至40mL时开始出现沉淀。则未滴加NaOH溶液前滤液中FeSO4的物质的量浓度为:
A.2mol·L-1 B.1.8mol·L-1 C.1.9mol·L-1 D.无法计算
8.2005年4月22日是第36个“世界地球日”,我国国土资源部确定今年“世界地球日”的主题为“善待地球-科学发展,构建和谐”。你认为下列行为中不符合这一主题的是
A.开发太阳能、水能、风能、可燃冰等新能源、减少使用煤、石油等化石燃料
B.控制含磷剂的生产和使用,防止水体富营养化,保护水资源
C.研究采煤、采油新技术,尽量提高产量以满足工业生产的快速发展
D.实现资源的“3R”利用观,即:减少资源消耗(Reduce)、增加资源的重复使用(Reuse)、资源的循环再生(Recycle)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com