
题目列表(包括答案和解析)
5、通常情况下,多个羟基连在同一个碳原子上的分子结构是不稳定的,容易自动失水,生成碳氧双键的结构:
 下面是9个化合物的转变关系:
下面是9个化合物的转变关系:
 (1)化合物①是___________,它跟氯气发生反应的条件A是_________
(2)化合物⑤跟⑦可在酸的催化下去水生成化合物⑨, ⑨的结构简式是:_______名称是______________________
(3)化合物⑨是重要的定香剂,香料工业上常用化合物⑧和②直接合成它。此反应的化学方程式是___________________________________________。
(1)化合物①是___________,它跟氯气发生反应的条件A是_________
(2)化合物⑤跟⑦可在酸的催化下去水生成化合物⑨, ⑨的结构简式是:_______名称是______________________
(3)化合物⑨是重要的定香剂,香料工业上常用化合物⑧和②直接合成它。此反应的化学方程式是___________________________________________。
4、提示:通常,溴代烃既可以水解生成醇,也可以消去溴化氢生成不饱和烃。如:
 请观察下列化合物A-H的转换反应的关系图(图中副产物均未写出),并填写空白:
请观察下列化合物A-H的转换反应的关系图(图中副产物均未写出),并填写空白:

(1)写出图中化合物C、G、H的结构简式:C________、G________、H_______。
(2)属于取代反应的有(填数字代号,错答要倒扣分)________。
3、写出以 为原料制备
为原料制备 的各步反应方程式。(必要的无机试剂自选)_______________________________________________________。
的各步反应方程式。(必要的无机试剂自选)_______________________________________________________。
2、已知乙烯在催化剂作用下,可被氧化生成乙醛,试以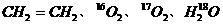 为主要原料合成
为主要原料合成 。写出有关的化学方程式。
。写出有关的化学方程式。
_______________________________________________。
1.工业上可用乙基蒽醌(A)制备H2O2,其工艺流程可简单表示如下:
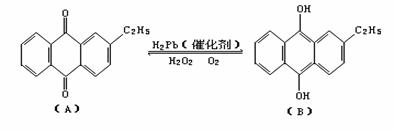
(1)A的分子式为______,B的分子式为_______。
(2)涉及氧化反应的反应式可写成:_______________。涉及还原反应的反应式可写成:____________。
(3)“绿色化学”是当今社会人们提出的一个新概念。在绿色化学中,一个重要的衡量指标是原子的利用率,其计算公式为:原子利用率=期望产品的摩尔质量/化学方程式按计量所得产物的摩尔质量如 ,则制备
,则制备

学工艺”中,理想状态原子利用就为100%,试问该法生产H2O2可否称为理想状态的“绿色工艺”?简述理由 。
2、化合物A最早发现于酸牛奶中,它是人体内糖代谢的中间体,可由马铃薯、玉米淀粉等发酵制得,A的钙盐是人们喜爱的补钙剂之一。A在某种催化剂的存在下进行氧化,其产物不能发生银镜反应。在浓硫酸存在下,A可发生如下所示的反应。

试写出:
⑴化合物的结构简式:A ,B ,D 。
⑵化学方程式:A→E ,
A→F 。
⑶反应类型:A→E ,A→F 。
[随堂作业]
1、松油醇是一种调香香精,它是α、β、γ三种同分异构体组成的混合物,可由松节油分馏产品A(下式中18O是为区分两个羟基而人为加上的)经下列反应制得:

试回答:
(1)α-松油醇的分子式
(2)α-松油醇所属的有机物类别是 (多选扣分)
(a)醇 (b)酚 (c)饱和一元醇
(3)α-松油醇能发生的反应类型是 (多选扣分)
(a)加成 (b)水解 (c)氧化
(4)在许多香料中松油醇还有少量的以酯的形式出现,写出RCOOH和α-松油醇反应的化学方程式 。
(5)写结简式:β-松油醇 ,γ-松油醇
16.(14分)(1)①NaOH、Na2CO3②Na2CO3③Na2CO3、NaHCO3④NaHCO3(每空1分)
(2)①NaCl;a15(各2分)②33.6(2分)③Na2CO3和NaHCO3;1:1(各2分)
15.


(4)3:4(2分)
14.(1)MnO2+4HCl(浓) MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
(2)饱和食盐水 关闭分液漏斗旋塞和Ⅰ处活塞,从c中向容器内加饱和食盐水,当c的下端浸入液面下且c中的液面高于b瓶内液面,并长时间不下降,则说明气密性好
(3)Ⅱ可行,Ⅲ不行 Ⅱ与Ⅰ原理相同,而Ⅲ中因c瓶口密封,体积不能改变,增大压强时会有危险
(4)①观察当整个装置内充满黄绿色气体时,说明氯气已充满整个装置。②有浅黄色沉淀生成 溶液变蓝
(5)C+2H2O+2Cl2
 CO2+4HCl
CO2+4HCl
(6)生成的HCl使紫色石蕊试液变红色,剩余的氯气又与水作用生成次氯酸,又起漂白作用,使红色褪去
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com