
题目列表(包括答案和解析)
4.A、B、C是中学化学中常见的三种元素的单质。A、B、C及其他物质之间的关系如下图所示,其中B、D、E、F溶液显酸性,又知常温下B为气态。

请回答:(1)A、B、C三种单质分别是A________,B_________,C__________。
(2)B与C反应生成E时的现象是______________________________________。
(3)写出下列变化的离子方程式:F+B→D______________________________,
D+C→E+F__________________________________。
3.下图是中学化学中常见的物质间化学反应关系,其中未注明用量的物质间的反应均按恰好充分反应处理,其他有关信息已在框图中说明。
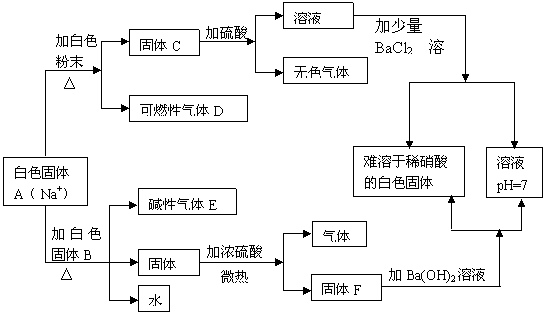
(1)写出下列物质的化学式:A_______,C_______,D_______,E_______,F________。
(2) 写出下列反应的化学方程式:
写出下列反应的化学方程式:
_____________________________________。
(3)白色固体B的化学式是否能确定?________,理由是___________________________。
2.A、B是中学化学里常用的物质,其中B是单质,A是化合物,A、B之间相互反应以及生成物之间的转化关系如图所示。
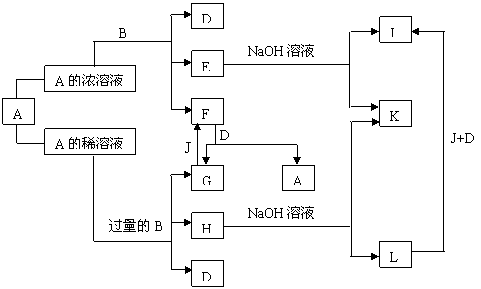
已知E溶液跟石炭酸的稀溶液混合时,溶液呈紫色。请回答:
(1)A和B的浓溶液反应的条件是_________,而常温下难反应的原因是_______________。
(2)写出F和G相互转化的化学方程式:
F→G:_________________________
G→F:________________________
(3)L转化成I的现象是________________________,
有关的化学方程式是___________________________。
1.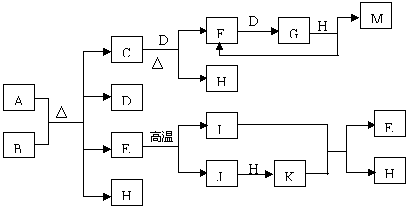 已知A为酸式盐,B为某二价主族金属(其原子序数不超过20)的化合物,常温常压下C、D、F、G、I均呈气态。等物质的量A、B充分混合后加热能恰好完全反应。图中反应条件(除加热外)均已略去。
已知A为酸式盐,B为某二价主族金属(其原子序数不超过20)的化合物,常温常压下C、D、F、G、I均呈气态。等物质的量A、B充分混合后加热能恰好完全反应。图中反应条件(除加热外)均已略去。
(1)写出A的化学式________________,B的电子式__________________。
(2)写出下列反应的离子方程式:
①在A溶液中加入M______________________________________。
②向A溶液中加入过量的NaOH溶液,并加热_________________________________。
(3)如对气体G进行加压操作,产生的现象是____________________________________,
发生反应的化学方程式是__________________________________________________。
7.某课外活动小组利用下图仪器装置和药品进行物质性质与转化关系的探究。当将Ⅱ中铂丝加热至红热时,打开K阀使气流缓缓通过。请回答下列有关问题:
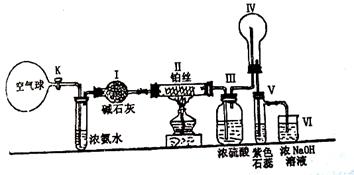
⑴如何检查该装置的气密性:_________________________________________________。
⑵写出Ⅱ中发生的化学方程式:________________________________________。
⑶装置Ⅳ(烧杯)中的现象:__________________________________________;
装置Ⅴ(试管)中的现象:__________________________________________;
⑷装置Ⅰ与Ⅲ都能起到干燥气体作用,两者能否调换位置使用:_______(填“能”或“不能”);理由:________________________________________________________________;
⑸烧杯中NaOH溶液的作用:__________________________________________。
6.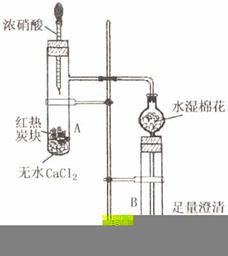 下图所示是进行木炭与浓硝酸反应,并检验生成的气体和反应的热效应的实验装置,它具有无污染,现象明显的特点。具支试管A中所盛固体下层是无水CaCl2(做载体不参加反应),上层是红热的木炭。实验时慢慢将浓硝酸滴到木炭上,反应即开始进行且能长时间剧烈反应。
下图所示是进行木炭与浓硝酸反应,并检验生成的气体和反应的热效应的实验装置,它具有无污染,现象明显的特点。具支试管A中所盛固体下层是无水CaCl2(做载体不参加反应),上层是红热的木炭。实验时慢慢将浓硝酸滴到木炭上,反应即开始进行且能长时间剧烈反应。
请回答下列问题:
写出木炭与浓硝酸反应的化学方程式
______________________________________________
(2)该反应的反应热△H________0(填“>”或“<”),
这一结论的实验证据是________________________
_________________________________________;
(3)实验中具支试管A内出现的现象是______________
________________________________________;
(4)试管B内出现的现象为_______________________,澄清石灰水中发生主要反应的离子方程式为_______________________________;
(5)某学生在实验临近结束时,发现滴管中的浓硝酸难以滴下。若要再滴人几滴浓硝酸使木炭反应完全,最简单的办法是____________________
____________________________________________________________________________。
5.实验室可利用下列反应和下图装置制备少量氨水:
①Zn+2HCl====ZnCl2+H2↑
②NH4Cl(溶液)+NaNO2(溶液)  N2↑+NaCl+2H2O
N2↑+NaCl+2H2O
③N2+3H2  2NH3
2NH3
④NH3+H2O==NH3·H2O

其中反应①可在A装置中进行,A装置可随时控制反应产物的量;反应②可在未画出的C中进行;反应③可在E装置中进行;反应④则可在未画出的F装置中进行。
A装置可选择以下仪器组装而成:a.铁架台(带铁圈和铁夹)b.圆底烧瓶 c.烧杯d.带有胶塞和活塞的单孔导管 e.干燥管 f.大试管 g.酒精灯h.长颈漏斗
请根据上述所给的信息,完成下列问题:
(1)A装置所需仪器是______(用a-h的字母符号填写)。
(2)请在下面两框内分别画出最简单的C和F装置图,并用化学式标明各容器内的物质。(注:为了更简捷表明化学实验装置示意图,可用一些简单图形表示化学仪器:
带胶塞的容器“□”,敞口容器“  ”,普通漏斗“
”,普通漏斗“ 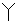 ”,长颈漏斗“
”,长颈漏斗“ 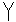 ”,分液漏斗“
”,分液漏斗“ 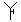 ”,导管“-”或“
”,导管“-”或“  ”,酒精灯“△”,支架装置可以不画出。
”,酒精灯“△”,支架装置可以不画出。
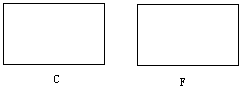
(3)各装置的连接的顺序为(气流由左到右):
A-→( )-→( )-→( )-→F
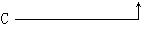
(4)①D装置中 应放入的试剂是______,②其作用是 ______;③B装置的三个作用是 ______。
(5)实验开始时,打开活塞,点燃装置C处的酒精灯,等一会儿,才能点燃装置E处的酒精灯。这样做的原因是 ______。
4.用下图所示装置可进行测定SO2转化为SO3的转化率的实验。
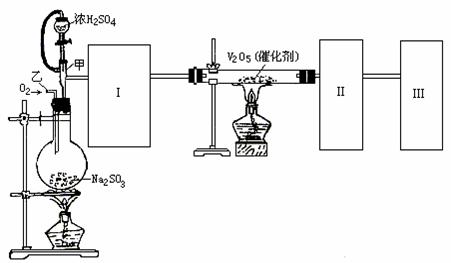
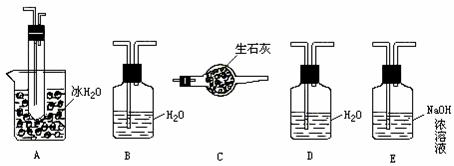
(1)根据实验的需要,Ⅰ、Ⅱ、Ⅲ处应连接合适的装置。请从下图A-E中选择合适的装置,将其序号填入以下空格内。
Ⅰ、Ⅱ、Ⅲ处所连接的装置分别为______、______、______。
(2)实验时,浓硫酸能顺利地滴入烧瓶中,甲仪器所起作用的原理是______。
(3)从乙处均匀通入O2,为使SO2有较高的转化率,实验时,在加热与滴加浓硫酸过程中,应采取的操作是:________________________________________________。
(4)用大火加热烧瓶时,SO2的转化率会______(填提高、不变或降低)。
(5)用a molNa2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,称得(Ⅲ)装置增重bg,则本实验中SO2的转化率为______。
3.实验室提供下列药品:①蒸馏水;②用HNO3酸化的AgNO3溶液;③熟石灰;④淀粉;⑤肥皂水;⑥食醋;⑦废干电池(锌筒内填有炭粉、MnO2、NH4Cl、淀粉等糊状物);⑧NaCl;⑨Na2CO3,某同学准备进行下列小实验:
A.制NaOH溶液
B.制备Cl2并验证其漂白性
C.制CO2气体
D.制硬脂酸
E.进行淀粉的水解实验并检验其水解产物
(1)由于缺少试剂而不能进行的实验是(不考虑电解)_________(填代号)。
(2)该同学为制备NH3,先从废干电池中制备NH4Cl。为此,他设想将废电池中的混合物溶于少量的水中,过滤除去不溶物,再蒸发灼烧滤液,以制得干燥的NH4Cl晶体。他的设想是否合理?答: ______,理由是____________________________________________。
(3)该同学在进行除去淀粉溶液中食盐的实验时,他用一枚鸭蛋自制了一个半透膜小袋向其中装入混有NaCl的淀粉溶液,扎好袋口,他即将进行的实验操作的名称叫 ______;要保证全部除去淀粉溶液里的食盐,实验中必须______。
(4)另有同学设计了实验室制取CO2的如下图四种实验原理和装置;
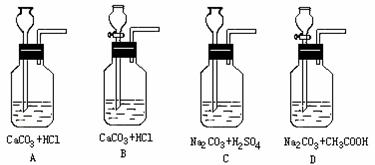
你认为其中不合理的是 ______;理由是 ______。
(5)由于实验(2)中NH4Cl的制备较困难,且难以满足量的要求,现重新提供足量的浓氨水、浓NaOH溶液和NH4Cl晶体,请设计一个最简单的实验,以快速制得NH3。
①你的设计方案是________________________________________________________。
②请运用化学原理对你的方案予以解释______________________________________。
2.某化学课外活动小组对某气体混合物样品设计了如下步骤进行实验。
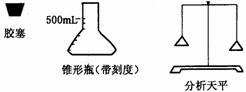
①取一个配有合适胶塞且洁净、干燥的500mL锥形瓶,用精确度为0.001g的分析天平(下同)准确称量,得到质量为ml。
②往锥形瓶中通入足量的干燥的该气体混合物样品,塞好瓶塞,准确称量,得到质量为m2。
③往锥形瓶中加满水,塞好瓶塞,称量,得到质量为m3。
 ④查得水的密度为d水(g·cm-3),空气的密度为d空气(g·cm-3),空气的平均相对分子质量为29.0,则该气体混合物样品的平均相对分子质量为:29.0×
④查得水的密度为d水(g·cm-3),空气的密度为d空气(g·cm-3),空气的平均相对分子质量为29.0,则该气体混合物样品的平均相对分子质量为:29.0×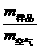 。
。
所用的仪器如图:
请回答下列问题:
(1)实验目的:__________________________________。
(2)计算:
①锥形瓶中空气的质量(写出算式)m空气=______________________________;
②锥形瓶中样品的质量(写出算式)m样品=_______________________________。
(3)问题与讨论:
问题一:实验完成后,有的同学提出,实验不是在标准状况进行的,应该记录实验的温度(T℃)和压强(PkPa),并对有关数据进行换算,你认为是否有必要,并说明理由。
问题二:老师对该小组的实验设计进行点评时指出:为了使实验数据合理、有效,在每次测量时,锥形瓶中的气体(或水)体积都应该相等。对此,你认为应采取的操作是什么?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com