
题目列表(包括答案和解析)
3、取一定量的Fe、Cu的混合物粉末,平均分成四等份,分别向每一份中加入一定量的稀硝酸,实验中收集到的NO气体的体积及所得剩余物的质量记录如下(所有体积均在标准状况下测定):
|
实验序号 |
① |
② |
③ |
④ |
|
硝酸体积 |
100mL |
200mL |
300mL |
400mL |
|
剩余物的质量 |
17.2g |
8g |
? |
? |
|
气体体积 |
2.24L |
4.48L |
? |
? |
请填完成上表空格。
2、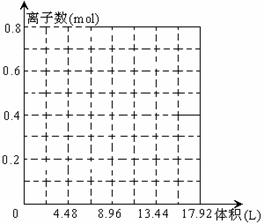 将KOH和Ca(OH)2的混合物1.3g全部溶于一定量水中形成稀溶液,再缓缓通入足量的CO2气体。
将KOH和Ca(OH)2的混合物1.3g全部溶于一定量水中形成稀溶液,再缓缓通入足量的CO2气体。
(1)当生成沉淀的质量刚好最大时,消耗CO2的体积为224mL(标准状况)。
①生成沉淀的最大质量是_____(g);沉淀恰好全部溶解时消耗CO2的体积为_____(mL)。
②原混合物中KOH的质量为________(g)。
(2)若KOH和Ca(OH)2以任意比混合,总质量仍保持1.3g不变,则消耗CO2的总体积V(mL)的取值范围为_____________。
(3)某溶液中有0.1mol Ca(OH)2和0.2mol NaOH, 往溶液中持续通入CO2, 当CO2刚足量时,立即改通NH3, 作出通入气体体积与溶液中离子数的图象。(不考虑气体在水中的溶解度,离子水解忽略不计)
1、 Na2SO4溶液的溶解度曲线如右图,
(1)下列说法正确的是
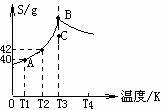 A.A点表示Na2SO4溶液尚未达到饱和,但降温和加入Na2SO4·10H2O晶体都可使其饱和
A.A点表示Na2SO4溶液尚未达到饱和,但降温和加入Na2SO4·10H2O晶体都可使其饱和
B.B、C点表示T3时,Na2SO4溶液在B点的溶解度大于在 C点的溶解度
C.在C点时Na2SO4溶液降温或升温,都可能使溶液变浑浊
D.以上说法均不正确
(2)已知芒硝(Na2SO4·10H2O)在温度T3时开始分解为无水硫酸钠,现有142gT2时的饱和硫酸钠溶液,当温度降为T1或升为T4时析出固体的质量相等。
①不用计算试判断T1和T4时Na2SO4溶解度的大小关系?
②试通过计算说明你的推断是否正确?
③通过右图说明制取芒硝(Na2SO4·10H2O)的最佳方法是_____________________。
5. 以为原料, 并以Br2等其他试剂制取, 写出有关反应的
化学方程式,并注明反应条件(注,已知碳链末端的羟基能转化为羧基)。
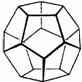 6. (1) 如图所示是十二面体烷的空间构型:
6. (1) 如图所示是十二面体烷的空间构型:
①写出它的化学式 ;
②它的一氯取代物的数目为 ;
③它的二氯取代物的数目为 。
(2) 一卤代物只有一种的烷烃,其分子结构有“球形”(A)和“椭球形”(B)两类,它们的组成有一定的规律性,A类是以甲烷分子为母体,用甲基经过多次循环处理后制得的; B类是以乙烷分子为母体,用甲基多次循环处理后制得的。
①写出碳原子数在10个之内,一卤代烃只有一种的烷烃的结构简式。
;
②在所有A类和B类物质中碳原子数在100个之内,分子量最大的一种物质,
它分子式是 ;
③A类物质的通式是 ;B类物质的通式是 ;
④A与B之间是否存在同分异构体?为什么?
4.乙醇在浓H2SO4存在并加热的条件下可发生脱水反应(A),而产物在加热、加压和有H2SO4存在的条件下可发生水化反应(B),反应可能经历了生成中间体(①)这一步。
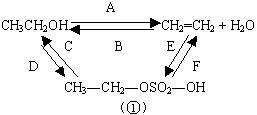
(1)如果将反应按取代、加成和消去分类,则A--F六个反应(将字母代号填入以下空白)中属于取代反应的是______ 属于加成反应的是_______ 属于消去反应的是_____
(2)按系统命名法,中间体(①)的名称是
(3)如果将原料C2H5OH中的羟基中的H用D标记成C2H5OD,则反应后的浓H2SO4中是否可能含有D?为什么?生成物之一的水中是否可能含有D?为什么?
(4)如果将浓H2SO4用D标记成D2SO4,则生成物之一的水中是否可能含有D?为什么?
(5)模仿上题反应原理,完成下列反应(不考虑反应条件,但须配平)
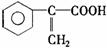
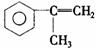
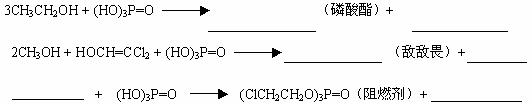
3. 由本题所给①、②两条信息、结合所学知识,回答下列问题:
①、已知有机分子中的烯键可发生臭氧分解反应。例如:
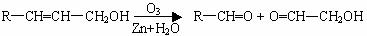
②、在碱存在下

从松树中分离得到的松柏醇,其分子式为C10H12O3,它既不溶于水,也不溶于碳酸氢钠溶液。下图为松柏醇的部分性质。
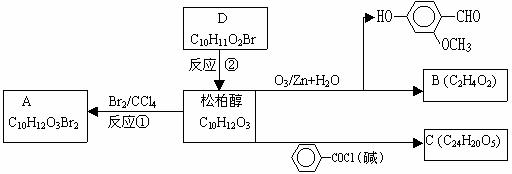
试回答:(1)写出化合物的结构简式:
松柏醇:____________________ B:_____________ C:_____________ D:______________
(2)写出反应类型:反应① 反应②
2. 已知卤代烃的水解反应:R―X + H2O → R―OH + HX(X代表卤原子),某酯A的化学式为C6H8O4Cl2与有机物B、C、D、E的转化关系如图所示:
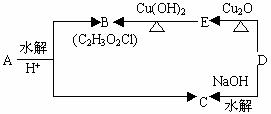
(1)写出A、B、C、D的结构简式:A B C D



 (2)写出E-B的化学方程式:
(2)写出E-B的化学方程式:
 (3)B在氢氧化钠溶液中水解后再酸化可以得到F,写出F发生缩聚反应的化学方程式:
(3)B在氢氧化钠溶液中水解后再酸化可以得到F,写出F发生缩聚反应的化学方程式:
1. 有机物甲的结构简式如下,它可通过不同的化学反应分别制得结构简式为乙~庚的物质。请回答下列问题:
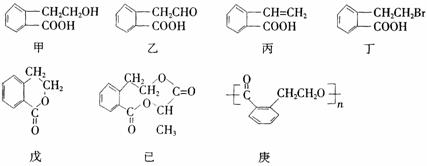
(1)指出反应的类型:
甲→丙:________________,甲→丁:______________________
(2)在甲~庚七种物质中,互为同分异构体的是__________(填代号,多选扣分,下同);
可看作酯类的是_________________。
(3)已知HCHO分子中所有原子都在同一平面内,则在上述分子中所有原子有可能都在同一平面内的物质是_____________。
6.Xe和F2反应,可得三种氟化物,视反应条件而定.图表述的是将0.125mol/L Xe和1.225mol/LF2为始态得到的生成物在平衡体系内的分压与反应温度的关系.
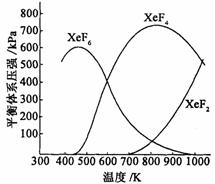
(1)应在什么温度下制备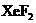 和
和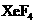 ?
?
(2)Xe和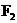 生成
生成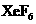 和
和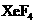 ,哪个反应放热更多?生成________的反应放热更多.理由:
,哪个反应放热更多?生成________的反应放热更多.理由:
(3)为有效地制备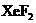 ,应在什么反应条件下为好?简述理由.
,应在什么反应条件下为好?简述理由.
5. 2002年9月26日,中国北京曙光公司研制出了第一款具有完全我国自主知识产权的电子计算机服务器,在这台服务器上,奔腾的就是“龙芯”.
(1)“龙芯”(芯片)的主要成分是________.
(2)在计算机长距离联网使用的传输很快的线路,其使用的材料叫________纤维,主要成分是________.
(3)如果这种埋在地下的纤维裸露在碱性土壤中,结果会________,用离子反应方程式说明原因______________________________________________________________.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com