
题目列表(包括答案和解析)
9. 下列除去杂质的方法正确的是 ( )
|
|
物质 |
杂质 |
试剂 |
主要操作 |
|
A |
SiO2 |
Fe2O3 |
盐酸 |
过滤 |
|
B |
NaHCO3 |
Na2CO3 |
/ |
加热 |
|
C |
Fe |
Al |
氢氧化钠溶液 |
过滤 |
|
D |
Fe(NO3)2 |
Ba(NO3)2 |
硫酸 |
过滤 |
8.将20mL 0.4mol/L硝酸铵溶液跟50mL 0.1mol/L氢氧化钡溶液混合,则混合溶液中以下各 正确的是 ( )
A C(NO3-)>C(OH-)>C(NH4+)>C(Ba2+)
B C(NO3-)>C(Ba2+)>C(OH-)>C(NH4+)
C [Ba2+]+[NH4+]+[H+]=[NO3-]+[OH-]
D 2C(Ba2+)+C(NH4+)+C(H+)=C(NO3-)+C(OH-)
7. 晶体可以分为分子晶体、离子晶体、原子晶体等,在以下①②两个题目中,分别对不同晶体的组成、微粒间的作用力以及晶体的几何构型等进行了描述,请根据各题的提问做出选择:
①下列关于只含非金属元素的化合物的说法正确的是( )
A 一定是共价化合物,且只能构成分子晶体;
B 其晶体不可能是离子晶体,因为微粒间的作用力只有分子间作用力;
C 其晶体不可能是原子晶体,原子晶体只有非金属单质,没有化合物;
D 可能是离子化合物。
②有下列离子晶体空间结构示意图:●为阳离子,○为阴离子。以M代表阳离子,N代表阴离子,化学式为MN2的晶体结构为( )
A 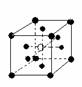 B
B 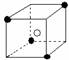 C
C 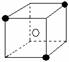 D
D 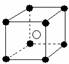
6. 下列说法中,正确的是(用NA表示阿伏加德罗常数值) ( )
A 常温常压下,1mol氖气含有的核外电子数是20NA
B 32g氧气和32g臭氧所含氧原子数都为2NA
C 18g水中所含的电子数是8NA
D 标准状况下,1L戊烷完全燃烧后生成的二氧化碳的分子数是5NA/22.4
5.已知在1×105Pa,298K条件下,2mol氢气燃烧生成水蒸气放出484kJ热量,下列热化学方程式正确的是 ( )
A H2O(g)=H2(g)+1/2O2(g) ΔH=+242kJ·mol-1
B 2H2(g)+O2(g)=2H2O(l) ΔH=-484kJ·mol-1
C H2(g)+1/2O2(g)=H2O(g) ΔH=+242kJ·mol-1
D 2H2(g)+O2(g)=2H2O(g) ΔH=+484kJ·mol-1
4.用0.01mol·L-1NaOH溶液完全中和pH=3的下列溶液各100mL。需NaOH溶液的体积最大的是 ( )
A 盐酸 B 硫酸 C 高氯酸 D 醋酸
3.下列各组物质的性质比较,从强到弱的顺序正确的是 ( )
A 单质熔点:Li>Na>K>Mg>Al B 酸性:HClO4>H2SO4>H3PO4 >H2SiO3
C 稳定性:AsH3>PH3>NH3 D 沸点:HI>HBr >HCl>HF
2.下列实验中,仪器的下端必须插入液面下的是 ( )
①制备氢气的简易装置中的长颈漏斗; ②制备氯气装置中的分液漏斗;
③制备Fe(OH)2操作中的胶头滴管; ④制乙酸乙酯时插入碳酸钠溶液中的导管
⑤用乙醇制取乙烯时的温度计; ⑥分馏石油时的温度计
A ①③⑤ B ②④⑥ C ①③④⑤ D 全部
1.13C-NMR(核磁共振)、15N-NMR可用于测定蛋白质、核酸等生物大分子的空间结构,KurtW ü thrich等人为此获得2002年诺贝尔化学奖。下面有关13C、15N叙述正确的是
A 13C与15N有相同的中子数 B 13C与C60互为同素异形体 ( )
C 15N与14N互为同位素 D 15N的核外电子数与中子数相同
4、(1)用已调零的托盘天平称取5.1g(1g以下为游码)药品时,将药品与砝码的位置放反了,称得药品的质量为_______。
(2)为了测定一包白色粉末的质量,将药品放在天平右盘,砝码放在左盘,并需移动游码使之平衡将导致结果________(填“偏高”、“偏低”或“不变”)。
(3)调平托盘天平时未将游码归零,在其它操作均正确的情况下用此天平称取5.3g药品,称量结果会怎样?________________。
(4)已调平的托盘天平指针略偏右,用此天平称量5g药品,结果如何?______________。
(5)现用已调零的托盘天平称取一种黑火药(硝酸钾、硫磺和木炭的混合物)样品,称量时将药品与砝码放反了(1g以下为游码),称得质量为248g。将药品燃烧后生成67.2L(标准状况下)气体和由K2CO3、K2SO4以及K2SO3组成的固体。其中67.2L气体产物中N2占1/3,其余气体为CO和CO2。求黑火药中硝酸钾、硫磺、木炭的物质的量。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com