
题目列表(包括答案和解析)
3.烧瓶
(1)识别 烧瓶包括圆底烧瓶、平底烧瓶、蒸馏烧瓶。
(2)用途 烧瓶一般作为有液体参加的反应器,也可以装配气体发生器,特殊情况下可用作气体收集装置。蒸馏烧瓶多用于液体的蒸馏与分馏。
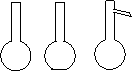 (3)使用方法
(3)使用方法
①加热前烧瓶外壁必须擦干,并垫上石棉网。
②加热时用铁架台固定
③加热时液体量应为容量的1/3-2/3之间
④煮沸、蒸馏时要加几粒沸石或碎瓷片。
[例4]下列仪器:①烧杯 ②蒸发皿 ③平底烧瓶 ④试管 ⑤坩埚 ⑥锥形瓶 其中可以用酒精灯直接加热的仪器为( )
A.①②④⑤⑥ B. ②④⑤ C.①④⑥ D.④⑥
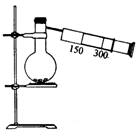 [例5]如图(图中有部分仪器末画出),有一容积为300mL的注射器,与蒸馏烧瓶(500mL)相连,烧瓶中有0.384gCu片,现向烧瓶中加入18mL 2.5mol/L的稀HNO3溶液,并立即用锡箔包住的橡皮塞封住瓶口。
[例5]如图(图中有部分仪器末画出),有一容积为300mL的注射器,与蒸馏烧瓶(500mL)相连,烧瓶中有0.384gCu片,现向烧瓶中加入18mL 2.5mol/L的稀HNO3溶液,并立即用锡箔包住的橡皮塞封住瓶口。
试回答:
(1)欲提高Cu和稀HNO3的反应速率,可采取多种不同的措施:
①若采用加入化学试剂的方法,可加入___________。
A.水 B.无水醋酸钠 C.铂丝 D.硝酸锌
②若用升高温度的方法,还需用的仪器有__________。
(2)橡皮塞用锡箔包住的原因是__________。
(3)反应开始后,烧瓶中可观察到的现象主要有____________
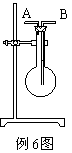 (4)停止反应后,轻轻推拉注射器活塞,使气体与气体、气体与液体皆充分反应。若忽略液体体积的变化,最终溶液中NO3-的物质的量浓度与开始时相比______________
(4)停止反应后,轻轻推拉注射器活塞,使气体与气体、气体与液体皆充分反应。若忽略液体体积的变化,最终溶液中NO3-的物质的量浓度与开始时相比______________
(A)不变 (B)变大 (C)变小 (D)无法确定
[例6] 利用如图所示装置收集以下8种气体(图中烧瓶的位置不得变化)。
①H2 ②C12 ③CH4 ④HCl ⑤NH3 ⑥N0 ⑦H2S ⑧SO2
(1)若烧瓶是干燥的,则由B口进气可收集的气体有____________(填序号)。
(2)若烧瓶充满水,可收集的气体有_____________,这时气体由_____口进入。
(3)若烧瓶是干燥的,则由A口进气,可收集的气体有______________。
(4)若在烧瓶内装人浓硫酸,进行气体干燥,则可用此装置来干燥的气体有_________这时气体由_________口进入。
2.烧杯
(1)识别 如图,有大、中、小不同规格
 (2)用途
(2)用途
①用作溶解试剂,配制一定浓度溶液。
②用作常温或加热时较多试剂之间的反应器
③可用于浓缩、稀释溶液。
④盛放具有腐蚀性药品进行称量
(3)使用方法
①烧杯用作反应容器和加热液体时,液体体积不超过烧杯容积的1/3
②在烧杯里配制溶液时,选用烧杯的容积应比所配溶液的体积大一倍为宜。
③加热前烧杯外壁必须擦干,并垫上石棉网。
④用玻璃棒搅拌烧杯中的溶液时,应注意不要碰触烧杯壁及底部。
⑤从烧杯中倾倒液体时应从杯嘴向外倾倒。
[例3]先选择填空,再简要说明作出选择的理由。
(1)某试管内装有约占其容积的1/10的溶液,则溶液的体积是(用字母回答,下同)_______,因为_______________________________________。
A.约1mL B.约3mL C.约10mL D. 无法判断
(2)拟在烧杯中于加热条件下配制其溶液 50mL,应选择的烧杯是_____________,因为_____________________________________________。
A. 400mL烧杯 B. 250mL烧杯 C. 100mL烧杯 D. 50mL烧杯
1.试管
 (1)识别 试管的形状为圆柱形弧底的玻璃仪器
(1)识别 试管的形状为圆柱形弧底的玻璃仪器
(2)常用规格 有大、中、小号不同的规格的试管。通常用管长×管直径描述规格
(3)用途
①用作少量试剂的反应器
②可用于收集少量气体 ③可用作简易气体发生器④作洗气瓶用
(4)使用方法:
①在常温或加热时使用,可用酒精灯直接加热
②装液体时,液体不超过试管溶积的1/2,如需加热,则不超过1/3
③加热试管要用试管夹。加热前把试管外壁擦干,再使试管均匀受热,以防炸裂
④加热液体时,试管不要对着人,保持试管与台面倾角为45°
⑤加热固体时,试管横放,试管口略向下倾斜,先均匀受热,然后固定受热
⑥振荡试管时应用拇指、食指、中指拿离试管口的1/3处,用腕力
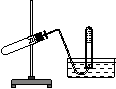 [例1]:下图装置可用于( )
[例1]:下图装置可用于( )
A.加热NaHCO3制CO2
B.用Cu与HNO3 反应制NO
C.用NH4Cl与浓NaOH溶液反应制NH3
D.用NaCl与浓H2SO4反应制HCl
[例2]下列实验不需要用到试管的是( )
A.实验室制取乙炔 B. 测量胆矾里结晶水的含量
C.实验定收集氨气 D. 实验室制取酚醛树脂
4.注意事项
①由于钾与钠性质相似,在钾的化合物里常含有钠离子,给观察钾的焰色反应带来干扰,所以在观察钾的焰色反应时需透过蓝色钻玻璃滤去黄色。
②焰色反应是金属或金属离子的性质,无论是其溶液还是固体都有这一性质。
③若焰色反应中,用铂丝(或铁丝)去蘸取试样粉末,为便于粘上,一般应将金属丝灼烧。 ④洗净铂丝用盐酸而不用硫酸,是因为金属的硫酸盐的沸点比盐酸盐高,金属氯化物在灼烧时易气化而挥发。
[例22] 欲观察氢气燃烧时火焰的颜色,燃气导管口的材料最好是( )。
(A)钠玻璃 (B)钾玻璃 (C)石英玻璃 (D)铜管
[例23] 草木灰中含有碳酸钾,海藻灰中含有碘盐。从草木灰中提取碳酸钾,从海藻灰中提取碘,并做有关检验。
(1)用石蕊试纸检验溶液酸碱性,正确的操作方法是___________________________。
(2)为测定草木灰中碳酸钾含量,需配制一定物质的量浓度的溶液。配制前检查容量瓶是否漏水的方法是____________________________________________________。
(3)从草木灰中提取钾盐。过滤后的溶液在蒸发皿里加热以得到钾盐晶体。加热过程中要____________________,当蒸发到____________________________时停止加热。
(4)用焰色反应检验K+,某学生用无锈铁丝去粘碳酸钾粉末,却粘不上,这是因为__________________;某学生粘上了钾盐粉末,但在酒精灯上灼烧时看到火焰是黄色而看不到紫色,这是因为__________________________。
(5)将氯气通人海藻灰溶液,溶液变为浅棕色,将CCl4加入溶液中,充分振荡,静置分层后,下层液体的颜色是___________________色。
专题二十四 化学实验的基本操作
[例1]D
[例2](1)固定A、甲、乙三管,将A、甲两管橡皮塞塞紧,在乙管中注入适量水,使乙管液面高于甲管液面,静置片刻,水面保持不变,说明装置气密性良好
(2)①取下试管A,向其中加入适量水,再沿试管壁慢慢加入少量浓H2SO4振荡,使液体体积不超过试管容积的1/3,将试管斜放,把锌片放在试管内壁上,塞紧塞子,慢慢直立,使锌片滑下与稀H2SO4接触。
②100ml烧瓶,带分液漏斗和导气管的双孔塞,烧杯及玻璃棒;将锌粒(或片)放入烧瓶内后,用双孔塞塞紧,在烧杯里将浓H2SO4稀释为适当浓度的稀H2SO4后转入分液漏斗中,打开活塞,使反应发生。
(3)调节甲、乙两管的液面高度至相平;以减少测量误差。
(4)洗气瓶、带导管的双孔塞、50ml量筒。
[例3]C
[例4]AD
[例5]C
[例6](1)在阴凉处置于棕色试剂瓶中密封保存
(2)①氯水与NaOH 反应生成两种盐,碱性减弱;
②氯气过量后HClO的漂白性将溶液变成无色;向 无色溶液中再滴加NaOH溶液,若不再出现红色,,应为原因②,若再出现红色,应为原因①
[例7]C
[例8]C
[例9]①调整天平的零点,使天平平衡;②检查滴定管是否漏水;③将试纸用蒸馏水润湿
[例10](1)不正确 (2)若溶液不显中性,则H+或OH―被稀释,测出的不为溶液中H+或OH―对应的pH值,不一定有误差,当溶液为中性时,则不产生误差。(3)测得H3PO4
的pH小,因为在稀释过程中,H3PO4 继续电离出H+,使得溶液中[H+]大。
[例11]D
[例12](1)3→5→4→2→6;C;B (2)除Cl2中混有的水蒸气;除去Cl2中混有的HCl;
Cl2+2NaOH=NaCl+NaClO+H2O (3)气密性;①
(4)4NaCl+4H2SO4+MnO2=MnCl2+4NaHSO4+Cl2+2H2O (5)棕黄;绿
[例13](1)把导管b的下端浸入水中,用手紧握捂热试管a,导管口会有气泡冒出,松开手后,水又回升到试管b中。(2)3Cu+8HNO3=3Cu(NO3)2+2NO+4H2O;2NO+O2=2NO2
(3)①铜片和稀HNO3反应,有无色气泡产生,反应速率开始慢,逐渐加快;②试管上部空间由无色变为红棕色,又变为无色;③试管a中的溶液由无色变为浅蓝色;④反应结束时,铜片全部溶完。(4)由于反应开始时产生的NO和试管a上部空气中的O2作用生成NO2 ,NO2易溶于水并与水起反应,使装置内气体的压强暂时减小,所以导管中的水面会上至一定高度。(5)试管中的水会上升一定高度。
[例14](1)C;B;G;E;F;A (2)溴水;品红溶液;NaOH溶液,吸收尾气。(2)关闭活塞K,向长颈漏斗中注水至漏斗下端液面高于试管中液面,过一段时间,液面高度差保持不变,则气密性良好。(4)关闭⑥中分液漏斗活塞将⑥中烧瓶微热,若仪器②④⑤液面下导管口处有气泡产生,说明②③④⑥不漏气。
[例15]AD
[例16]A
[例17]AB
[例18]D
[例19]A
[例20](1)2NaBr+3H2SO4+MnO2 2NaHSO4+MnSO4+2H2O+Br2↑;冷凝;吸收未冷凝的气体。(2)溴蒸气腐蚀橡胶 (3)当气体被吸收时,液体上升到漏斗中。由于漏斗容积较大,导致烧杯中液面下降,使漏斗口脱离液面,漏斗中液体又流回到烧杯中,从而防止倒吸。
2NaHSO4+MnSO4+2H2O+Br2↑;冷凝;吸收未冷凝的气体。(2)溴蒸气腐蚀橡胶 (3)当气体被吸收时,液体上升到漏斗中。由于漏斗容积较大,导致烧杯中液面下降,使漏斗口脱离液面,漏斗中液体又流回到烧杯中,从而防止倒吸。
[例21](1)液体分层,上层为油状液体;(2)制乙酸,作催化剂和吸水剂;(3)防止倒吸;(4)降低酯在水中的溶解度,除去酯中混有的酸和醇,有利于分层。
[例22]C
[例23](1)将试纸放在玻璃片上,用玻璃棒蘸溶液点在试纸上;(2)往烧瓶加水,塞好烧瓶,用食指顶住瓶塞,另一手托住瓶底,把瓶倒立过来,如果瓶塞周围不漏水,将瓶塞旋转180°再塞上,重复以上操作。(3)不断用玻璃棒搅拌溶液;只剩下少量溶液。(4)无锈铁丝未加热;未隔蓝色钴玻璃观察。 (5)紫。
3.实验现象 用铂丝蘸碳酸钠溶液在火焰上灼烧时火焰呈黄色;当蘸碳酸钾溶液或氯化钾在火焰上灼烧时,透过蓝色钻玻璃观察,火焰呈紫色。
2.操作方法 把装在玻璃棒上的铂丝(也可用光洁无锈的铁丝或镍、铬、钨丝)放在酒精灯外焰里灼烧,等到跟原来的火焰颜色相同的时候,用铂丝蘸碳酸钠溶液,放在火焰上,观察火焰颜色。每次试验完后都要用稀盐酸洗净铂丝,在火焰上灼烧到没有什么颜色,再分别蘸碳酸钾溶液、氯化钾溶液作试验,观察火焰的颜色。在观察钾的火焰颜色的时候,
要透过蓝色的钻玻璃去观察,这样可以滤去黄色的光,避免碳酸钾里钠的杂质所造成的干扰。
1.作用 多种金属或它们的化合物灼烧时火焰呈特殊的颜色,可以用来检验一些金属或金属化合物,测定出它们的存在。钠的焰色反应为黄色,钾的焰色反应透过蓝色钻玻璃观察为紫色。
3.气体的溶解
①溶解度较小者,如H2S、C12、CO2等溶解时,可把导气管直接插入水中。
②溶解度较大的(如极易溶解的NH3、HCl等),在导管末端接一倒置的三角漏斗,让漏斗边缘稍没入水面,这样既可增大气体的吸收率,减小气体的逸出,同时也避免出现液体倒吸。若缺少漏斗,导管末端只能靠近水面,或选用肚形容器替代,防止倒吸(下图)。
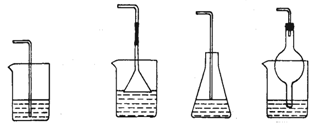
[例19] 实验室制备氯水,应选用的最佳装置是( )。
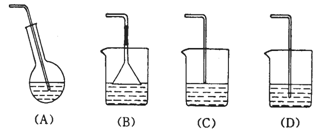
[例20] 根据下图所示的实验,填空和回答问题。
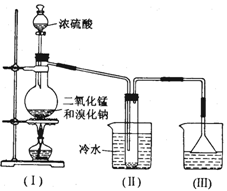
(1)烧瓶中所发生的主要化学反应方程式是______________________________________。装置(Ⅱ)的烧杯中冷水所起作用是____________________________。装置(Ⅲ)的烧杯中液体的作用是___________________________________________
(2)进行此实验时,烧瓶内的橡皮塞最好用锡箔包住,用橡皮管连接的两玻璃管口要相互紧靠,这是因为__________________________________________________。
(3)装置(Ⅲ)的烧杯中使用倒置漏斗可防止液体倒吸,试简述其原因。
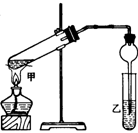 [例21] 如右图所示,在试管甲中先加入2mL
95%的乙醇,并在摇动下缓缓加入2mL浓硫酸,充分摇匀,冷却后再加入2g无水乙酸钠,用玻璃棒充分搅拌后将试管固定在铁架台上。在试管乙中加入5mL饱和碳酸钠溶液,按图连接好装置。用酒精灯对试管甲加热,当观察到试管乙中有明显现象时停止实验。试回答:
[例21] 如右图所示,在试管甲中先加入2mL
95%的乙醇,并在摇动下缓缓加入2mL浓硫酸,充分摇匀,冷却后再加入2g无水乙酸钠,用玻璃棒充分搅拌后将试管固定在铁架台上。在试管乙中加入5mL饱和碳酸钠溶液,按图连接好装置。用酒精灯对试管甲加热,当观察到试管乙中有明显现象时停止实验。试回答:
(1)试管乙中观察到的现象是_____________________________________________
(2)加入浓硫酸的目的是_________________________________________________
(3)该实验中使用球形管除起冷凝作用外,另一重要作用是__________________________
(4)试管乙中饱和碳酸钠溶液的作用是____________________________________________
2.液体的溶解 一般液体可直接加水溶解,振荡或搅拌可以加速溶解。特别注意浓H2SO4的溶解(稀释)方法--应将浓硫酸缓缓注入水中并不断搅拌,乙醇和浓硫酸、浓硝酸与浓硫酸的混合均如此。
1.固体的溶解 研细→搅拌→加热(但必须是加热不水解或不发生化学变化的物质),均可加速固体的溶解(如FeCl3、NaHCO3的溶解等,均不可加热)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com