
题目列表(包括答案和解析)
12、某厂废液中含有大量Ag+、Fe3+、Al3+,用下图方法进行分离(部分反应条
 件省略):
件省略):
(1)写出下列物质的化学式:
试剂x 、试剂z 。 晶体E 、固体G 。
(2)写出下列反应的离子方程式:
沉淀A+试剂y: 滤液D+过量CO2:
11、某煤中含有硫元素,煤在燃烧过程中能产生会引起酸雨的气体A。为降低气体A的排放量,采取的措施之一就是向煤中加生石灰,此法称为“钙基固硫”。这种煤燃烧后,大部分硫元素最终以CaSO4的形式存在。
(1)(3分)若煤中含硫量为0.32%(质量分数),处理1 t这种煤,应至少加入纯度为96%的生石灰 kg。
(2)(4分)在空气污染监测中,常用Br2与气体A的定量反应来测定空气中A的含量。写出水溶液中Br2与气体A反应的化学方程式: 。
10、二口恶英是一种含C、H、O、Cl元素组成的混合物,对人体有很强的致畸作用,其主要成分中毒性较大的化合物的结构简式为:
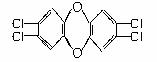 (1)(4分)该物质的分子式为 ;该物质分子结构中最多可能共面的原子数为
。
(1)(4分)该物质的分子式为 ;该物质分子结构中最多可能共面的原子数为
。
(2)(2分)若将上述化合物放入足量NaOH溶液中加热煮沸,则生成物的结构简式为
。
9.以M原子为中心形成的MX2Y2分子中,X、Y分别只以单键与M结合,下列说法正确是
A.若MX2Y2分子为平面四边形就有2种同分异构体
B.若MX2Y2分子为平面四边形则无同分异构体
C.若MX2Y2分子为四面体形就有2种同分异构体
D.若MX2Y2分子为四面体形则无同分异构体
8.用物质的量都是0.01 mol的HCN和NaCN配成1 L混合溶液,已知其中c(CN-)<c(Na+),对该溶液的下列判断正确的是①c(H+)>c(OH-);②c(OH-)>c(H+);
③c(HCN)>c(OH-);④c(HCN)+ c(CN-)== 0.02 mol/L?
A.①④ B.①③④ C.②③ D.②③④
7.( )在10 L密闭容器中,1 mol A和3 mol B在一定条件下发生反应:
A(g)+xB(g) 2C(g)反应经8 min达到平衡,测得此时混合气体共3.4 mol,测得生成物C有0.4
mol,则下列计算结果中错误的是
2C(g)反应经8 min达到平衡,测得此时混合气体共3.4 mol,测得生成物C有0.4
mol,则下列计算结果中错误的是
A.x的值为4 B.平衡时各物质的物质的量浓度之比为1∶4∶2
C.A的转化率为20% D.C的反应速率为0.005 mol·L-1·min-1?
5.( )下列说法不正确的是(NA表示阿伏伽德罗常数)
A.60g SiO2晶体中,含有NA个Si-O键 B.1 mol十七烷分子中,共价键总数为52NA个
C.在4.4gD2118O分子中,含有的中子数为2.4NA个 D.1mol─CH3中,含有的电子数为9NA?( )6.市场上有一种加酶洗衣粉,即在洗衣粉中加入少量的碱性蛋白酶,它的催化活性很强,衣物的汗渍、血迹及人体排放的蛋白质油渍遇到它,皆能水解而除去。下列衣料中不能用加酶洗衣粉洗涤的是①棉织品;②毛织品;③晴纶织品;④蚕丝织品;⑤涤纶织品;⑥锦纶织品
A.①②③ B.②④ C.③④⑤ D.③⑤⑥
3.( )已知A、B、C、D、E是核电荷数依次增大的五种短周期元素,原子半径按D、E、B、C、A的顺序减小,B和E同主族,下列推断不正确的是
A.A、B、E一定在不同周期 B.D为第二周期
C.A、D可能在同一主族 D.C和D的单质可能化合为离子化合物
 ( )4.吸入人体内的O2有2%转化为活性氧如,活性氧能加速人体衰老,目前正尝试用亚硒酸钠Na2SeO3(Se为VIA族元素)
( )4.吸入人体内的O2有2%转化为活性氧如,活性氧能加速人体衰老,目前正尝试用亚硒酸钠Na2SeO3(Se为VIA族元素)
消除活性氧。下列说法中不正确的是
A.Na2SeO3溶液的pH>7 B.消除活性氧时,Na2SeO3是还原剂
C.H2SeO4的酸性比H2SO4强 D.H2Se的稳定性比HBr弱
2.( )下列离子方程式书写正确的是
A.等物质的量浓度的FeI2溶液与溴水等体积混合2Fe2++ 2I-+ 2Br2======2Fe3++ I2+ 4Br-
B.铜与浓硝酸反应 Cu + 2H++ 2NO3-======Cu2++ 2NO↑ + H2O
C.用氨水吸收少量的SO2 2NH3·H2O + SO2======2NH4++ SO32-+ H2O
D.NaHSO4溶液与过量的Ba(OH)2反应 H++ OH-======H2O
2.如何正确识别图象
(1)看图象:一看面(横轴和纵轴各表示什么)二看线(线的走向,变化趋势),三看点(是否过原点。线的交点及拐点),四看要不要作辅助线(如等压线、等温线)
(2)想规律:联想外界条件对化学平衡对化学反应速率和化学平衡的影响规律。
(3)作判断,依题意仔细分析并作出正确的判断。
★例题精析
[例1]:反应A+3B=2C+2D在四种不同情况下的反应速率分别为:
①V(A)=0.15mol/L·s ②V(B)=0.6mol/L·s
③V(C)=0.4mol/L·s ④V(D)=0.45mol/L·s
该反应进行的快慢顺序是:_____________________________
[例2]甲、乙两位同学在实验室做实验,分别看到如下现象,甲同学将Cu片投入到稀HNO3中发现开始气泡生成速率缓慢,一段时间后速率稍加快了一些;乙同学将KMnO4溶液(用稀H2SO4酸化)滴入到FeSO4溶液中,发现开始褪色较慢,后来非常快,请你用有关知识对甲乙两位同学的实验现象进行解释?
[例3]:在一定温度下,把2molSO2和1molO2通入一个一定容积的密闭容器中,发生如下反应:2SO2
+ O2  2SO3 当此反应进行到一定程度时,反应混合物就处于化学平衡态。现在该容器中维持温度不变,令a、b、c分别代表初始加入的SO2 、O2和SO3 的物质的量(mol)。如果 a、b、c取不同的数值,它们必须满足一定的相互关系,才能保证达到平衡时,反应混合物中三种气体的体积分数仍跟上述平衡时的完全相同,请填写下列空白。
2SO3 当此反应进行到一定程度时,反应混合物就处于化学平衡态。现在该容器中维持温度不变,令a、b、c分别代表初始加入的SO2 、O2和SO3 的物质的量(mol)。如果 a、b、c取不同的数值,它们必须满足一定的相互关系,才能保证达到平衡时,反应混合物中三种气体的体积分数仍跟上述平衡时的完全相同,请填写下列空白。
(1)若a=0,b=0,则c=____________________
(2)若a=0.5,则b=________________和c=_________________
(3)a、b、c必须满足的一般条件是(请用两个方程式表示,其中一个只含a和c,另一个只含b和c)____________________________________________________。
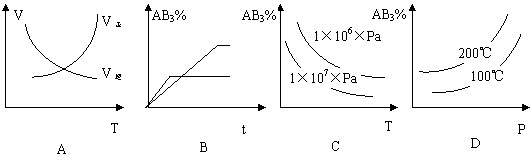 [例4]:对于可逆反应:A2(g)+3B2(g)
[例4]:对于可逆反应:A2(g)+3B2(g)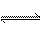 2AB3(g);△H<0,下列图象正确的是:
2AB3(g);△H<0,下列图象正确的是:
|
|||
|
[例5]I.恒温、恒压下,在一个可变容积的容器中发生如下反应:A(g) + B(g) C(g)
C(g)
(1)若开始时放入1molA和1molB,达到平衡后,生成amolC,这时A的物质的量为______________mol
(2)若开始时放入3molA和3molB,达到平衡后,生成C的物质的量为__________mol
(3)若开始时放入x mol A、2molB和1molC,达到平衡后,A和C的物质的量分别是y mol和3a mol,x=____________mol 、y=_____________mol
平衡时,B的物质的量__________________(选填一个编号)
(甲)大于2mol
(乙)等于2mol
(丙)小于2mol
(丁)可能大于、等于或小于2mol
作出此判断的理由是:________________________________________________
(4)若在(3)的平衡混合物中再加入3 mol C,待再次达平衡后,C的质量分数是____________________
Ⅱ.若在维持温度不变,在一个与(1)反应前起始体积相同,且容积固定的容器中发生上述反应。
(5)开始时放入1mol A和1molB达到平衡后,生成b mol C,将b与(1)小题中的a进行比较____________________(选填一个编号)
(甲)a<b (乙)a>b
(丙)a=b (丁)不能比较a和b的大小
作出此判断的理由是__________________________________________________________
例题解答:
例1 ④>③=②>①
例2Cu与HNO3反应放热,使体系的温度升高;生成的Mn2+作催化剂。
例3(3)a+c=2 b+c/2=1
例4 B
例5(1)(1-a) (2)3a
(3)2, 3-3a, 丁
若3a>1,B的物质的量小于2 mol
若3a=1,B的物质的量等于2 mol
若3a<1,B的物质的量大于2 mol
(4)a/(2-a)
(5)乙;因为(5)小题中容器容积不变,而(1)小题中容器的容积缩小,所以(5)小题的容器中的压强小于(1)小题容器中的压强,有利于逆向反应,故反应达到平衡后,a>b。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com