
题目列表(包括答案和解析)
2、漂尘是物质燃烧时产生的粒状漂浮物,颗粒很小,不易沉降。它与空气中的SO2和O2接触时,使空气的酸度增加,漂尘所起的作用可能是
A 催化剂 B 还原剂 C 氧化剂 D 载体
1、下列物质属于纯净物的是
A 溴水 B 重水 C 硬水 D 王水
4.B 5.B 6.(1)①CH4 与C3H4O2 ②C2H2 与C2H6O2 ③C2H4 与C2H4O2 ④C2H6 与C2H2O2 ⑤C3H6 与CH2O2 7.A 8.B
4.有机物物理性质归纳
(1)沸点的规律
①同系物中随碳原子的增加沸点逐渐升高。
②在常温常压下,烃中碳原子数≤4的为气态,烃的衍生物中常见的气体是HCHO、CH3Cl。
③同分异构中直链的高,且支链越多沸点越低。
④碳原子数相同时:R-COOH > RCH2OH > RVHO > RCH3
(2)溶解性规律
①碳原子较少的醇、醛、酸易溶于水,但随着碳原子数的增加溶解度减小,如乙醇与水互溶,而戊醇溶解度为8g。
②苯酚、乙炔微溶于水。 ③烃、酯、油脂、一氯化烃,难溶于水且密度小于1 g/cm-3
④硝基苯、溴代烃、多氯代烃难溶于水且密度大于1 g/cm-3 。
例题精析
[例1]常温常压下,某气态烃和氧气的混合气体V升完全燃烧后,通过浓H2SO4,再恢复到原来温度和压强时,气体体积变为原来的一半,假设烃完全燃烧后无剩余,则该烃可能是:
①C2H4 ②C2H6 ③C3H6 ④C4H6 ⑤C4H8 ⑥CH4 ⑦C3H8
A.①⑤ B.②③ C.①②⑥⑦ D.④⑤

|
A.除苯环外的其余碳原子有可能都在一条直线上,
B.除苯环外的其余碳原子不可能都在一条直线上,
C.12个碳原子不可能都在同一平面上,
D.所有原子有可能都在同一平面上。
[例3]烯烃在一定条件下氧化时,由于C=C键断裂,转化为醛、酮。如
|
|

|
 CH3-C=CHCH3
CH3-C-CH3 + CH3-CHO 已知某烃(C8H14)在上述条件下反
CH3-C=CHCH3
CH3-C-CH3 + CH3-CHO 已知某烃(C8H14)在上述条件下反


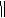 应后,生成三种有机物: CH3-CHO 、CH3 C CH3 、 OHC-CH2-CHO
,
应后,生成三种有机物: CH3-CHO 、CH3 C CH3 、 OHC-CH2-CHO
,
|
[例4]1 mol某链烃能和2 mol HCl发生加成反应,生成1 mol氯代烷,该氯代烷能和6 mol氯气发生取代反应,生成只含碳元素和氯元素的氯代烃。该烃可能是( )
A.丙烯 B.丙炔 C. 1-丁炔 D. 1,3 -丁二烯
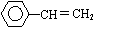
[例5]由苯乙烯( )和羟基乙酸乙酯( HOCH2COOCH2CH3 )组成的混合物中,若碳元素的质量分数为70%,那么氢元素的质量分数约为 ( )
A.4.6% B. 7.7% C. 15.6% D.无法计算
[例6]由等物质的量A和B组成的混合物,其中A为烃(A为直链烷、烯、炔烃),B为烃的含氧衍生物。取混合物0.5mol在1.25mol氧气中充分燃烧,二者恰好反应,生成1.0mol CO2 和1.0 molH2O。请回答:
(1)从分子式的角度看,该混合物的组成可能有几种,以分子式填充下表(可不填满):
|
混合物 |
A |
B |
混合物 |
A |
B |
|
①组 |
|
|
④组 |
|
|
|
②组 |
|
|
⑤组 |
|
|
|
③组 |
|
|
⑥组 |
|
|
(2)在上表混合物中,有一组符合下述条件:取一定量A和B 以任意比混合,只要物质的量之和一定,完全燃烧耗氧量也一定。写出其结构简式:A ,B 。
(3)在上表混合物中,有一组符合下述条件:取一定量A和B 以任意比混合,只要物质的量之和一定,完全燃烧生成的CO2和H2O的物质的量也一定。写出其结构简式:A ,
B 。
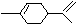
[例7]从柑桔中可炼制萜二烯( ),下列有关它的推测不正确的是( )
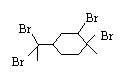 A.分子式为C10H16
B.常温下液态难溶于水
A.分子式为C10H16
B.常温下液态难溶于水
C. 能发生加聚反应
D. 与过量溴的CCl4 溶液反应后产物为
[例8]某有机物的分子式组成为CxHyOz ,取该物质m g在足量O2 中充分燃烧后,将产物全部通过足量的过氧化钠,充分反应后,过氧化钠固体质量也增加mg,则物质分子中必须满足
A.x=y B.x=z C.y=z D.x=y=z
答案:1.C 2.B 3. CH3-CH=CH-CH2-CH=C(CH3)-CH3
3.反应条件对产物的影响
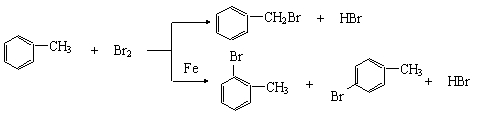
|
饱和碳原子上的卤代反应在光照条例下进行,苯环上的卤代反应在铁粉的催化作用下进行。
(2)苯环上原有取代基对卤代、硝化反应的影响:苯的同系物发生苯环上的取代反应,取代基主要进入烷烃基的邻位和对位。
(3)乙烯的制备过程中C2H5OH 的脱水。
(4)当反应中使用的溶剂不同所得产物也不同,如卤代烃在NaOH 水溶液中发生水解反应,而在NaOH的醇溶液中加热则发生消去反应,前者产物是醇,后者产物是不饱和烃(烯或炔)。
2.关于烃混合物中各组成成分物质的量之比的计算
(1)主要题型:
①已知混合烃的平均分子组成;②已知混合烃的平均相对分子质量;③已知混合烃(气态)完全燃烧时气体体积的变化;④已知混合烃完全燃烧时放出的热量。
(2)解题技巧:十字交叉法
(3)“十字交叉法”的应用范围:①两组分形成的混合体系,②可用于计算物质的量、体积、质量、原子个数等的量之比。
(4)根据有机物参加反应的化学方程式中某些物质的已知量,确定有机物的化学式。
1.烃的燃烧规律:
(1)等物质的量的烃完全燃烧时,消耗氧气的量决定于“X+Y/4”的值,此值大耗氧多。
(2)等质量的烃完全燃烧时,耗氧量决定于CxHy中y/x的值,此值越大,耗氧量越多。
(3)若烃分子的组成中碳、氢原子个数比为1 :2,则完全燃烧后生成CO2和H2O的物质的量相等。
(4)等质量的最简式相同的各种烃完全燃烧时其耗氧量、生成CO2和H2O的量均相等。
(5)气态烃CxHy完全燃烧后生成CO2和H2O 。
 CxHy+(x + y/4)O2 xCO2
+ y/2 H2O
CxHy+(x + y/4)O2 xCO2
+ y/2 H2O
当H2O为液态时(温度低于100℃),1mol气态烃完全燃烧后,气体体积减少△V=1+ y/4
当H2O为气态时(温度高于100℃),1mol气态烃完全燃烧前后,气体总体积的变化有以下三种情况:
①当y=4时,△V=0,反应后气体体积不变。
②当y>4时,△V= y/4 - 1 ,反应后气体总体积增大。
③当y<4时,△V= 1- y/4 ,反应后气体体积减小。
常温常压下呈气态的烃中,只有甲烷、乙烯、丙炔反应前后气体总体积不变。
3. 石油的分馏
石油的分馏
|
 ②炼制 分馏:根据石油中各种烃沸点不同,对石油加热,收集不同沸点范围的蒸馏产物(馏分)的方法(属物理变化)
②炼制 分馏:根据石油中各种烃沸点不同,对石油加热,收集不同沸点范围的蒸馏产物(馏分)的方法(属物理变化)
裂化:在一定条件下,将相对分子质量较大的、沸点较高的烃断裂为相对分子质量小、沸点较低的过程(属化学变化)
 裂解:是一种深度裂化,列解气主要成分是乙烯、丙烯、异丁烯。
裂解:是一种深度裂化,列解气主要成分是乙烯、丙烯、异丁烯。
(2)石油的分馏装置要注意以下几点:
①烧瓶要干燥,原油应占烧容积的1/3到2/3 , ② 加碎石片以防止暴沸,
 ③温度计水银球位于蒸馏烧瓶的支管口处, ④ 冷凝器进、出水方向是下进上出。
③温度计水银球位于蒸馏烧瓶的支管口处, ④ 冷凝器进、出水方向是下进上出。
巧思巧解
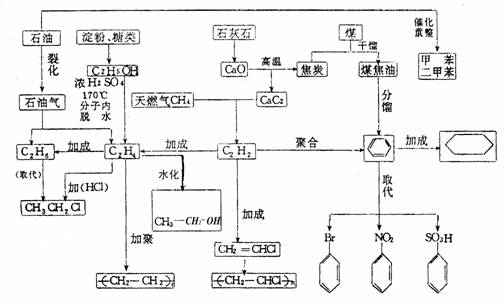
1.各类烃的组成及代表物的结构、特性和相互关系
|
|
烷 |
烯 |
炔 |
苯及其同系物 |
|
通式 |
CnH2n+2 (n≥1) |
CnH2n (n≥2) |
CnH2n-2 (n≥2) |
CnH2n-6 (n≥6) |
|
代表物 |
甲烷 |
乙烯 |
乙炔 |
苯 |
|
碳碳键长 (×10-10m) |
1.54 |
1.33 |
1.20 |
1.40 |
|
键
角 |
 109°28 109°28 |
约120° |
180° |
120° |
|
分子构型 |
正四面体 |
平面型 |
直线型 |
平面正六边型 |
|
主要化学 性质 |
卤代、受 热分解 |
加成、加聚 氧化 |
加成、氧化 加聚 |
取代、 加成 |
|

|
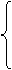
|
|
|
13. Ⅰ.红热的铁能与水蒸气反应,有氢气生成,现用下图所示装置进行铁在高温下与水蒸气反应的实验,并用简单的方法收集,检验生成的氢气。请回答下列问题:
Ⅰ.红热的铁能与水蒸气反应,有氢气生成,现用下图所示装置进行铁在高温下与水蒸气反应的实验,并用简单的方法收集,检验生成的氢气。请回答下列问题:
(1)写出铁在高温下与水蒸气反应的化学方程式 。
(2)干燥管C内盛放的药品是 或 (填化学式)。干燥管的
(m或n)端与g导管相连接。
(3)在D处画出用简单方法用试管来收集氢气的装置图(所需其他仪器自己选择)(4)怎样用简单方法检验收集到的气体是氢气,简述实验操作步骤和现象
。
Ⅱ.设计简单实验说明下列物质的氧化性由强到弱的顺序为:Cl2>FeCl3> I2可选用的药品有:氯水、FeCl3溶液、碘水、KI溶液、NaOH溶液、稀硫酸、盐酸、KSCN溶液、碘化钾淀粉溶液、FeCl2溶液、H2O2、水等。所需仪器自由选择。简述实验步骤、现象、结论;
(1) 。
(2) 。
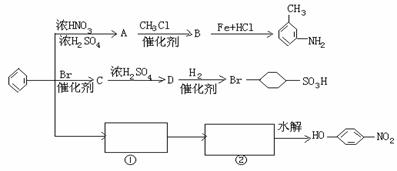 14.已知苯环上原有的取代基对新导入的取代基进入苯环的位置有显著影响。以下是用苯作原料制备一系列化合物的转化关系图:
14.已知苯环上原有的取代基对新导入的取代基进入苯环的位置有显著影响。以下是用苯作原料制备一系列化合物的转化关系图:
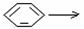 (1)写出C转化为D的化学方程式:
。
(1)写出C转化为D的化学方程式:
。
(2)图中 ①→②省略了反应条件,请在①和②上方的方框里填写对应物质的结构简式。
(3)B分子苯环上的任意两个氢原子被溴原子取代后,得到的二溴代物有 种同
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com