
题目列表(包括答案和解析)
23(6分)A、E为短周期元素的单质,B、C为化合物,他们之间的转化关系如下图所示:
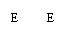
A →B →C
C溶于水且能产生气体,回答下列问题,写出全部可能的情况(写化学式)
第一种情况:A B C 。
第一种情况:A B C 。
第一种情况:A B C 。(可以不填满,也可补充)
24、(12分) A、B、C、D、E、F、G、H、I分别代表九种不同的有机物(其中A是化学工业重要原料之一).它们之间的相互转化关系如下图,请回答下列问题:

(1)A的结构式为________ ________;F的结构简式为_________ _______________;
(2)写出下列转化的化学方程式①C→D________________________________________,
②G→H_________________________________________________________________.
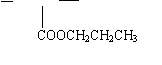 ( 3)已知有机物 [CH2-CH]n
的透气性比
( 3)已知有机物 [CH2-CH]n
的透气性比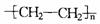 好.做为隐形眼镜的材料,
好.做为隐形眼镜的材料,
应该具有良好的透气性和亲水性,请从H的结构上分析它可以作为隐形眼镜材料的原因:
.
21、(12分)能源可划分为一级能源和二级能源,自然界中以现成形式提供的能源称为一级
能源;需依靠其它能源的能量间接制取的能源称为二级能源;氢气是一种高效而没有污染的二级能源,它可由自然界中的水来制取:2H2O(l)=2H2(g)+O2(g) △H= + 517.6KJ/ mol
(1)下列属于一级能源的是 。
A 电能 B 水力 C 天然气 D 焦炉气 E 风能 F 氢氧燃料电池
(2)已知:CH4(g)+2O2(g)=2H2O(l)+CO2(g) △H= -890.3千焦,18gH2和CH4(该混合气的平均相对分子质量为9),充分燃烧后,放出的热量为 KJ
(3)关于用水制取二级能源氢气,以下研究方向正确的是 。
A 构成水的氢和氧都是可燃烧的物质,因此可研究在水不分解的情况下,使氢成为二级能源
B 设法将太阳光聚集,产生高温,使水分解产生氢气
C 寻找高效催化剂,使水分解产生氢气,同时释放能量
D 寻找特殊化学物质,用于开发廉价能源,以分解水制取氢气
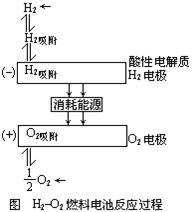 (4)燃料电池的基本组成为电极、电解质、燃料和氧化剂。此种电池能量利用率可高达80%(一般柴油发电机只有40%左右),产物污染也少。人们已将它应用于航天飞行器上。 下图为氢氧燃料电池反应的完整过程
(4)燃料电池的基本组成为电极、电解质、燃料和氧化剂。此种电池能量利用率可高达80%(一般柴油发电机只有40%左右),产物污染也少。人们已将它应用于航天飞行器上。 下图为氢氧燃料电池反应的完整过程
请将左图方框中的电极反应填补完整:
H吸附______________________________,
O2吸附______________________________;
(5)在理论上不能设计原电池的化学反应是 。
A HCl+NaOH==NaCl +H2O △H<0
B 2CH3OH(l)+3O2(g)==2CO2(g)+4H20(l) △H<0
C 4Fe(OH)2(s)+2H2O(l)+O2(g)=== 4Fe(OH)3(s) △H<0
D 2H2(g)+O2(g)=== 2H2O △H<0
 22、(11分)A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。
22、(11分)A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。
(1)A中反应的离子方程式为 。(2分)
(2)B中Sn极的电极反应式为 ,(2分)
Sn极附近溶液的pH(填“增大”、“减小”或“不变”) 。(2分)
(3)比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是 。(2分)
(4)有A、B、C、D四种金属,将A、B用导线连接后浸入稀H2SO4中,A上放出氢气,B逐渐溶解生成B2+;电解含A2+和C2+的混合溶液时,阴极上先析出C;将D放入含B2+的硝酸溶液中,D表面有B析出,同时生成D2+。则这四种金属阳离子的氧化性由强到弱的顺序为__________________________________。(3分)
20、(9分)实验室用铜和硫酸制取CuSO4有几种方法:
Ⅰ、甲学生进行了下列实验:取6.4g铜片和10mL18mol·L-1浓硫酸放在圆底烧瓶中共热,直到反应完毕,最后发现烧瓶中还有铜片剩余。他根据自己所学的化学知识,认为烧瓶中还有较多的硫酸剩余。他这样认为的理由是: .
|
Ⅱ、乙同学认为甲设计的实验方案不好,他自己设计的思路是2Cu+O2 2CuO;CuO+H2SO4 CuSO4+H2O。对比甲的方案,乙同学的优点是:
Ⅲ、为了同样达到乙同学的优点,你能不能根据电化学原理也设计一个用铜和硫酸制取CuSO4的方案?(其它材料任选)
19、(4分)(1)指出下列使用仪器或用品的第一步操作:
托盘天平: 。
红色石蕊试纸: 。
(2)指出做下列实验时,从安全角度考虑必须进行的实验操作或加入的实验用品:
点燃氢气 。
石油分馏(课堂演示) 。
18、周期表中有些元素有“对角线相似”现象(即周期表中处于对角线位置的两元素性质相似),如Li与Mg;Be与Al;B与Si等两两性质相似。现用熔融LiCl电解的方法可得锂和氯气。若用已潮解的LiCl加热蒸干并强热至熔融,再用惰性电极电解,结果得到金属锂和一种无色无味的气体。据此,下列说法正确的是
A、无色气体为电解生成的锂与水反应放出的H2 B、电解时产生的无色气体是O2
C、电解前LiCl在加热时已发生水解 D、无色气体是阳极放出的Cl2与水作用生成的O2
将正确的答案填入下表中
|
序号 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
答案 |
|
|
|
|
|
|
|
|
|
序号 |
9 |
10 |
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
|
答案 |
|
|
|
|
|
|
|
|
|
|
第Ⅱ卷(共76分)
17、t℃时,在V
mL密度为d  的
的 (相对分子质量为M)饱和溶液中,加入足量的NaOH溶液,充分反应后过滤(假设滤液无损失),在滤液中加入适量硝酸使溶液呈中性后,再加入4 mL 1.0 mol/L的
(相对分子质量为M)饱和溶液中,加入足量的NaOH溶液,充分反应后过滤(假设滤液无损失),在滤液中加入适量硝酸使溶液呈中性后,再加入4 mL 1.0 mol/L的 溶液恰好完全反应,则t℃时
溶液恰好完全反应,则t℃时 的溶解度
的溶解度
A 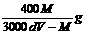 B
B  C
C 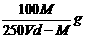 D
D 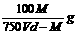
16、下列描述属于物质的物理性质的是
A 碳酸的不稳定性 B 盐酸的易挥发性
C CO的毒性 D 浓硫酸的吸水性
15、两个体积相同的容器,一个盛有NO,另一个盛有N2和O2,两容器内的气体质量相等,下列说法正确的是:
A 它们的分子数一定相同 B 它们的密度一定相同
C 它们一定具有相同的(平均)分子量 D 它们的压强一定相同
14、常温下,在含有H+、SO42-、Fe2+的溶液中,加入下列离子后,溶液中各种离子仍能大量共存的是 A ClO- B AlO- C HCO3- D I-
13、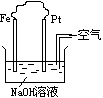 关于右图装置中的叙述正确的是
关于右图装置中的叙述正确的是
A 这是电解NaOH溶液的装置
B 这是一个原电池装置
C Pt为正极,其电极反应为:2H2O+O2+4e-=4OH-
D Fe为负极,其电极反应为:4OH- - 4e-=H2O+O2↑
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com