
题目列表(包括答案和解析)
2、自由的1mol H+和自由的1molOH-结合为1mol H2O ;
1、反应在稀溶液中进行;
2、书写注意事项:
①要注明反应时的温度和压强,若是常温常压则可不注明;
②要注明各物质的状态和晶型(如白磷、红磷两种晶型);
③热化学方程式中的化学计量数以“mol”为单位,可以是分数(但一般情况下不写分数),△H的单位与化学方程式的写法有关。但△H的单位永远是kJ·mol-1;
④△H>0时反应为吸热,△H<0时反应为放热,所以△H的值一定带有“+”、“-”号。
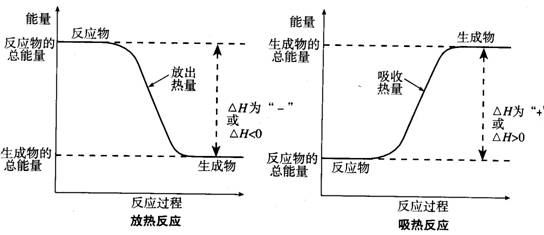
1、表示化学反应热效应的化学方程式称为热化学方程式。
4、具有唯一现象
(1)溶于水显碱性的气体:NH3
(2)空气中无色变红棕色的气体:NO
(3)在一定条件下具有漂白性的淡黄色固体:Na2O2
((4)遇SCN- 显红色,遇苯酚显紫色,遇OH― 生成红褐色沉淀:Fe3+
(5)在空气中能自燃的固体物质:P4
(6)遇Ag+ 有沉淀,沉淀不溶于稀HNO3
若沉淀为白色:Cl-; 若沉淀为浅黄色:Br-; 若沉淀为黄色:I-;
(7)可溶于NaOH的白色沉淀为Al(OH)3,可溶于NaOH的金属氧化物:Al2O3 (ZnO )
(8)能与NaOH作用产生H2 的单质:金属为铝;非金属为硅
(9)能与新制Cu(OH)2悬浊液混合加热生成砖红色沉淀的酸性物质:HCOOH
☆例题精析
[例1]为了除去粗盐中的 Ca2+ 、Mg2+ 、SO42― 及泥沙,可将粗盐溶于水,然后进行下列五项操作。其中正确的操作顺序是( )。 (1991年全国高考题)
①过滤②加过量NaOH溶液③加适量盐酸④加过量Na2CO3 溶液⑤加过量BaCl2 溶液
A ①④②⑤③ B ④①②⑤③ C ②⑤④①③ D ⑤②④①③
[例2]对要除去CO2 气体中所含的少量HCI气体,最好的方法是将混合气通过( )。 (1996年试测题)
A NaHCO3 溶液 B Na2CO3 溶液 C.饱和石灰水 D氨水
[例3]下列每组各有三对物质,它们都能用分液漏斗分离的是( )。
A.乙酸乙酯和水,酒精和水,苯酚和水B.二澳乙烷和水,苯和水,硝基苯和水
C.甘油和水,乙醇和水,乙酸和乙醇 D.油酸和水,甲苯和水,已烷和水
例4仅用水就能鉴别的一组物质是( )。 (1997年上海市高考题)
A苯、乙酸、四氯化碳 B乙醇、乙醛、乙酸
C乙醛、乙二醇、硝基苯 D苯酚、乙醇、甘油
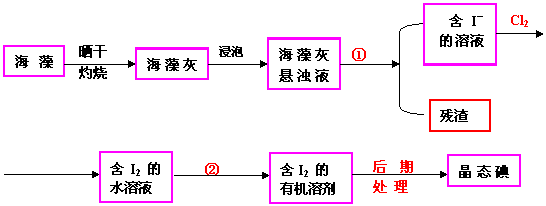 [例5 ]实验室里从海藻中提取碘的流程如下图:
[例5 ]实验室里从海藻中提取碘的流程如下图:
(1)
 指出制取碘的过程中有关的实验操作名称:①__________②________________
指出制取碘的过程中有关的实验操作名称:①__________②________________
(2) 提取碘的过程中,可供选择的有机试剂是______________
A 甲苯、酒精 B 四氯化碳、苯
C 汽油、乙酸 D 汽油、甘油
(3) 为使海藻中I― 转化为碘的有机溶液,实验室里有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器、物品,尚缺少的玻璃仪器是_____
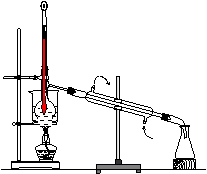
(4) 从含碘的有机溶液中提取碘和回收有机溶剂,还需要经过蒸馏,观察上图装置,指出其中错误之处,并加以改正__________
进行上述蒸馏操作时,使用水浴的原因是______最后晶态碘在___里聚集
3、烟、雾
(1)在空气中出现白雾的:HCl 、HBr 、HI 、HNO3
(2)在空气中出现白烟的:NH3 + HCl 、NH3 + HNO3
(3)燃烧时出现白色烟雾的:P + Cl2
(4)燃烧时出现棕黄色烟的:Cu + Cl2
2、沉淀的颜色变化
(1)Fe2+:遇碱液生成沉淀,其颜色转变为:白→灰绿→红褐
(2)Ag+:遇碱液生成沉淀,其颜色转变为:白→黑
1、火焰颜色
(1)苍白色:H2 在Cl2 中燃烧
(2)蓝色:CO在空气中燃烧
(3)淡蓝色:CH4 、H2 在空气中燃烧
(4)金属元素的焰色反应
6.离子交换法 例如用磺化煤(NaR)做阳离子交换剂,与硬水里的Ca2+、Mg2+进行交换,而使硬水软化。
有机物的分离和提纯
有机物的提纯要依据被提纯物质的性质,采用物理方法和化学方法除去杂质。一般情况是加入某种试剂,与杂质反应,生成易溶于水的物质,再用分液的方法除去杂质。如除去乙酸乙酯中混有的乙酸和乙醇,应在混合物中加入饱和的碳酸钠溶液,杂质乙酸与碳酸钠反应,生成了易溶于水的乙酸钠(同时降低乙酸乙酯的溶解度),充分搅拌后,用分液漏斗分液,可得纯净的乙酸乙酯。
在分离和提纯中有的的杂质不只一种,需用多种试剂和多种除杂分离方法,要注意安排好合理的除杂顺序。
5.利用物质的两性除去杂质 例如在Fe2O3里混有少量的Al2O3杂质,可利用Al2O3是两性氧化物,能与强碱溶液反应,往试样里加入足量的 NaOH溶液,使其中 Al2O3转化为可溶性 NaAlO2,然后过滤,洗涤难溶物,即为纯净的Fe2O3。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com