
题目列表(包括答案和解析)
4.在0℃,1.01×105Pa时,分别向甲、乙、丙三个容器中加入30.0mL同浓度的盐酸,再加入不同质量的由两种金属组成的合金粉末,测量放出气体的体积。若在甲、乙、丙三个容器中加入与盐酸同体积同浓度的NaOH溶液,再分别加入与上述实验相同质量的同种合金,测量放出气体的体积,如下表:
|
反应容器 |
甲 |
乙 |
丙 |
|
加入合金质量(g) |
0.510 |
1.53 |
3.57 |
|
与盐酸反应生成气体的体积(L) |
0.560 |
0.672 |
0.672 |
|
与氢氧化钠反应生成气体的体积(L) |
0.336 |
x |
y |
⑴根据表中数据可以计算得出的是 (填字母编号);
A.合金的组成 B.合金中各组分的含量 C.盐酸的物质的量浓度 D.盐酸溶液的密度
能计算出的量的值为 。
⑵若两种金属是下列选项中的某两种金属,则从甲容器中的两次实验来看:
①若不经计算,肯定没有 (填字母编号);
A.40Ca B.56Fe C.64Cu D.24Mg E.27Al
②通过计算讨论合金的成分 。
⑶根据⑵的推测结果,计算x和y的值分别为多少?
3.根据烷、烯、炔烃燃烧的反应式,有人总结出以下规律:对于烷烃有n(烷烃)=n(H2O)-n(CO2),对于烯烃有n(H2O)-n(CO2)=0,对于炔烃有n(炔烃)=n(CO2)-n(H2O)。请回答下列问题:
(1)某混合气体由C2H6和C3H4组成。将1.0体积混合气在氧气中充分燃烧,产生的CO2体积比水蒸气多0.2体积(相同状况下测定),通过计算确定C2H6和C3H4的体积。(设体积单位为升)
(2)某混合气由烯烃和烷烃或烯烃和炔烃组成。组成中可能是两种气体,也可能是多种气体。将1.0体积混合气在氧气中充分燃烧,产生3.0体积CO2和2.4体积水蒸气(相同状况下测定)
①判断混合气体有 两类烃组成。
②上述判断的理由是_________________________________________.(用简要文字叙述)。
③上述两类烃的体积比为__________________________
2.眠尔通是白色结晶性粉末,学名“2-甲基-2-正丙基-1,3-丙二醇双氨基甲酸酯”。化学式C9H18N2O4。眠尔通是弱安定药,用于治疗烦躁、焦虑和神经衰弱性失眠等症,副作用少,毒性低。眠尔通合成路线如下:
A B
B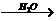 C
C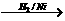 D
D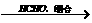 E
E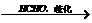 F(
F(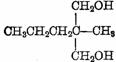 )
)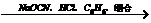 眠尔通
眠尔通
①写出“眠尔通”的结构简式;
②系统命名法命名F;
③推断A-E各物质的结构简式;
1.Ⅰ 分别取等质量的甲烷和A(某饱和一元醇)、B(某饱和一元醛)、C(某稠环芳香烃含氧衍生物),若它们完全燃烧,分别生成了物质的量相同的CO2 。则:
⑴A的分子式为___________________;B的分子式为________________;C的分子式为________________(C的分子式有多种可能,只写分子量最小的一种)。
⑵写出符合上述要求时,CH4和A、B、C的分子组成必须满足的条件是___________________(以n表示碳原子数,m表示氧原子数,只写通式)。
Ⅱ 化学式为C5H4的烃,理论上同分异构体的数目可能有30多种。如:
① CH2=C=C=C=CH2 ② CH≡C-CH=C=CH2
③
 ④
④  -C≡CH ⑤
-C≡CH ⑤
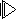 -CH=CH2……
-CH=CH2……
请不要顾忌这些结构能否稳定存在,完成下面各小题:
(1).异构体①、②是链状分子,请再写出2种链状分子的结构简式:
,_______________ _______。
(2).若核磁共振表明氢原子的化学环境没有区别,则满足条件的异构体除①、③外还有 _____ ____ 。(只需答出一例)
(3).除题干和以上小题涉及到的异构体外,请再写出2种异构体,要求每种异构体都有对称性(存在一条对称轴)。
________________________ , ____________________________。
6.下图是以C7H8为原料合成某聚酰胺类物质(C7H5NO)n的流程图。
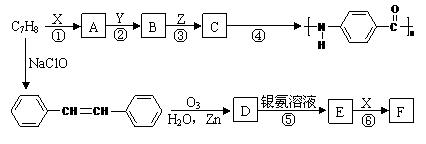
已知:Ⅰ、当一取代苯进行取代反应时,新引进的取代基因受原取代基的影响而取代邻、对位或间位。使新取代基进入它的邻、对位的取代基:-CH3、-NH2;使新取代基进入它的间位的取代基:-COOH、-NO2;
Ⅱ、R-CH=CH-R’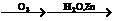 R-CHO+R’-CHO;
R-CHO+R’-CHO;
Ⅲ、-NH2易被氧化;-NO2可被Fe和HCl还原成-NH2
⑴X、Y、Z是下列试剂中的一种,其中X是_____,Y是_____,Z是_____(填序号)
①Fe和HCl ②酸性KMnO4 ③浓硝酸
⑵A-F中互为同分异构体的有_____________________________
⑶步骤②③______(填“能”或“不能”)对调,理由________________________________
⑷写出④的反应方程式___________________________________________________
写出⑤的反应方程式___________________________________________________
停课期间
每日一餐(七)
5、
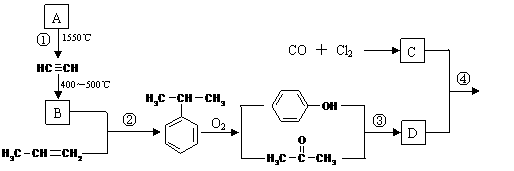 聚碳酸酯
聚碳酸酯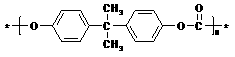 是一种优良的工程塑料,下图表示的是以丙烯和A(“西气东输”工程的主要气态物质)为原料合成该塑料的过程。
是一种优良的工程塑料,下图表示的是以丙烯和A(“西气东输”工程的主要气态物质)为原料合成该塑料的过程。
已知:㈠苯酚分子中与羟基相连碳原子的邻位及对位上的氢原子有很好的反应活性,容易跟含羰基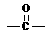 的化合物发生缩合反应,生成新的有机物和水
的化合物发生缩合反应,生成新的有机物和水
㈡苯酚还可以跟酰氯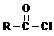 反应生成酯,如:
反应生成酯,如:
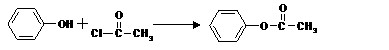 ⑴写出D的结构简式D______________
⑴写出D的结构简式D______________
⑵反应①除了乙炔外还有另一物质生成,写出该反应的方程式___________________
⑶已知反应②为加成反应,写出该反应的方程式_________________________________
⑷反应④为______反应,写出该反应的方程式________________________________
4.Ⅰ.红热的铁能与水蒸气反应,有氢气生成,现用下图所示装置进行铁在高温下与水蒸气反应的实验,并用简单的方法收集、检验生成的氢气。请回答下列问题:
(1)写出铁在高温下与水蒸气反应的化学方程式________________________________。
(2)干燥管C内盛放的药品是________或________(填化学式)。干燥管的________(m或n)端与g导管相连接。
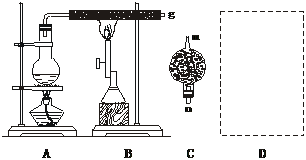
(3)在D处画出用简单方法用试管来收集氢气的装置图(所需其他仪器自己选择)。
(4)怎样用简单的方法检验收集到的气体是氢气,简述实验操作步骤和现象________。
Ⅱ.设计简单实验说明下列物质的氧化性由强到弱:Cl2>FeCl3>KI,可选用的药品有:氯水、FeCl3溶液、碘水、KI溶液、NaOH溶液、稀硫酸、盐酸、KSCN溶液、碘化钾淀粉溶液、FeCl2溶液、H2O2等。所需仪器自由选择。简述实验步骤、现象、结论。
(1)________________________________________________________________。
(2)________________________________________________________________。
3.某无色溶液中含有K+、Cl-、OH-、SO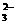 、SO
、SO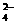 ,为检验溶液中所含的各阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液、溴水和酚酞试液。检验其中OH-的实验方法从略,检验其他阴离子的过程如下图所示。
,为检验溶液中所含的各阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液、溴水和酚酞试液。检验其中OH-的实验方法从略,检验其他阴离子的过程如下图所示。
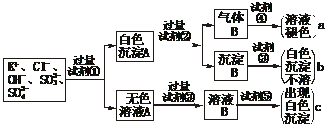
(1)图中试剂①-⑤溶质的化学式分别是:
①________,②________,③________,④________,⑤________。
(2)图中现象a、b、c表明检验出的离子分别是:a________、b________、c________。
(3)白色沉淀A加试剂②反应的离子方程式是_____________________。
(4)无色溶液A加试剂③的主要目的是___________________________。
(5)白色沉淀A若加试剂③而不加试剂②,对实验的影响是__________________。
 (6)气体B通入试剂④发生反应的离子方程式是___________________________。
(6)气体B通入试剂④发生反应的离子方程式是___________________________。
2. 实验室为自然科学(化学)兴趣小组的同学准备了四种红色溶液,它们分别可能是酸性KMnO4溶液、滴有酚酞的NaOH溶液、滴有石蕊的稀硫酸、品红溶液。另外还提供了常见的必备仪器和药品。为了培养同学们的创新精神和实践能力,老师规定只允许选用一种试剂鉴别上述四种溶液。
(1)甲组同学选用了FeCl2溶液,试写出该组同学鉴别出NaOH溶液的有关化学方程式(是离子反应的写出离子方程式):____________ _____________;
_______________________________________。
(2)乙组同学选用了Na2SO3溶液,他们第一步鉴别出来的溶液是____ ___,对应的现象分别是___________。还需继续完成的实验是(请简要写明操作步骤、现象和结论)_______________________________________________________________; _______________________________________________________________; _________________________________________ _____________________。
(3)丙组同学选用了甲、乙两组另外的一种试剂,鉴别时较甲、乙两组在操作上更为简便,你认为他们选择的试剂可能是___________。
1.右图所示为是中学化学实验中常见的装置,利用该装置可完成的实验有(固体质量已知)_____________
A.Na2O中Na2O2含量的测定
B.某Mg、Al合金中Al含量的测定
C.KHCO3中CaCO3含量的测定
D.NaCl中NH4Cl含量的测定
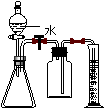 Ⅰ、甲同学将该装置略作改动,设计成了气体溶解度的测量装置。
Ⅰ、甲同学将该装置略作改动,设计成了气体溶解度的测量装置。
⑴实验过程:
①用排空气法收集一锥形瓶的某气体(溶解度约1∶40)
②记下量筒内液体体积的读数
③打开分液漏斗活塞,放下20滴水(约1mL),轻轻摇动锥形瓶。
④打开止水夹,待量筒内液面稳定下来读取液体体积。
⑵该装置中的集气瓶_______(填“能”或“不能”)省,简述理由
______________________________________________________________________。

 Ⅱ、乙同学将装置略作改动后设计了空气中氧气的体积分数测定装置。
Ⅱ、乙同学将装置略作改动后设计了空气中氧气的体积分数测定装置。
⑴装置中铜网内包裹的固体物质可能为___________
⑵在右图方框内将装置的剩余部分补充完整,要求限选用原装置仪器,导管、乳胶管、橡皮塞等连接类仪器不限。
⑶据题意,在表格中填写相应内容
|
测量数据 |
测量方法 |
|
锥形瓶内空气体积 |
|
|
|
|
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com