
题目列表(包括答案和解析)
19.某学生用NaHCO3和KHCO3组成的某混合物进行实验,测得如下数据(盐酸的物质的量浓度相等),下列分析推理不正确的是
|
|
50mL盐酸 |
50mL盐酸 |
50mL盐酸 |
|
m(混合物) |
9.2g |
15.7g |
27.6g |
 (标况) (标况) |
2.24L |
3.36L |
3.36L |
A.盐酸的物质的量浓度为3.0 mol·L-1
B.根据表中数据不能计算出混合物中NaHCO3的质量分数
C.加入混合物9.2g时盐酸过量
D.15.7g混合物恰好与盐酸完全反应
18. 已知反应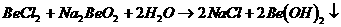 能完全进行,则下列推断中,正确的是( )
能完全进行,则下列推断中,正确的是( )
A.  溶液的pH<7,将其蒸干并灼烧后,得到的残留物可能为BeO
溶液的pH<7,将其蒸干并灼烧后,得到的残留物可能为BeO
B. 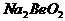 溶液的pH>7,将其蒸干并灼烧后,得到的残留物可能为BeO
溶液的pH>7,将其蒸干并灼烧后,得到的残留物可能为BeO
C.  既能溶于盐酸又能溶于烧碱溶液
既能溶于盐酸又能溶于烧碱溶液
D.  水溶液的导电性强,因此
水溶液的导电性强,因此 一定是离子化合物
一定是离子化合物
17.在一密闭容器中有如下反应:aX(g)+bY(g)  nW(g);ΔH=Q某化学兴趣小组的同学根据此反应在不同条件下的实验数据,作出了如下曲线图:
nW(g);ΔH=Q某化学兴趣小组的同学根据此反应在不同条件下的实验数据,作出了如下曲线图:
 其中,ω(W)表示W在反应混合物中的百分含量,t表示反应时间。其它条件不变时,下列分析可能正确的是
其中,ω(W)表示W在反应混合物中的百分含量,t表示反应时间。其它条件不变时,下列分析可能正确的是
A.图Ⅰ可能是不同压强对反应的影响,且P2>P1,a+b<n
B.图Ⅱ可能是在同温同压下催化剂对反应的影响,且1使用的催化剂效果好
C.图Ⅱ可能是不同压强对反应的影响,且P1>P2,n<a+b
D.图Ⅲ可能是不同温度对反应的影响,且T1>T2,Q<0
16.已知 溶液分别与
溶液分别与 溶液、
溶液、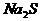 溶液的反应情况如下:
溶液的反应情况如下:
(1)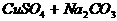
主要:
次要:
(2)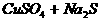
主要: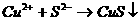
次要:
下列几种物质溶解度大小比较中,正确的是( )
A.  B.
B.

C.  D.
D.
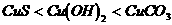
14.青霉素试验针用它的稀释液(200国际单位青霉素/mL),现有1小瓶20万国际单位青霉素,1.0 mL注射器(分刻度0.1 mL),注射用水和几个干净小瓶。现取1.0 mL注射用水滴注入第一瓶内溶解青霉素。吸取0.1 mL溶液在第2瓶中用水稀释成1.0 mL。再吸取0.1 mL在第3瓶中稀释成1.0 mL,又……在第几个小瓶中稀释后青霉素浓度为200国际单位/mL:( )
A. 3 B. 4 C. 5 D. 6
 15.6.2004年7月德俄两国化学家共同宣布,在高压下氮气会发生聚合得到高聚氮,这种高聚氮的N-N键的键能为160KJ/mol(N2分子中的键能为942 KJ/mol),晶体结构如图所示。下列有关高聚氮的说法错误的是
15.6.2004年7月德俄两国化学家共同宣布,在高压下氮气会发生聚合得到高聚氮,这种高聚氮的N-N键的键能为160KJ/mol(N2分子中的键能为942 KJ/mol),晶体结构如图所示。下列有关高聚氮的说法错误的是
A、高聚氮属于分子晶体
B、高聚氮晶体中每个N原子和另外3个N原子相连
C、高聚氮可能成为炸药
D、高聚氮转变成氮气是氧化还原反应
13.下列是除去括号内杂质的有关操作,其中正确的是
A.苯(苯酚)--加浓溴水,振荡静置分液
B.NO(NO2)--通过水洗、干燥后,用向下排气法收集
C.乙烷(乙烯)--让气体通过盛饱和溴水的洗气瓶
D.乙醇(乙酸)--加足量NaOH溶液,蒸馏
12.生物体中细胞膜内的葡萄糖与细胞膜外的富氧体液及细胞膜构成原电池,下列有关电极反应及产物的判断正确的是( )
A负极反应可能是O2+2H2O+4e→4OH--
B 负极反应的产物主要是C6H12O6被氧化成CO32-- HCO3--和H2O
C正极反应可能是C6H12O6+24OH---24e→6 CO2↑+18H2O
D正极反应的产物主要是葡萄糖生成的CO2 HCO3--和H2O
11.下列各组离子,在指定环境中能大量共存的是( )
A. 在 的溶液中,
的溶液中,
B. 在 的溶液中,
的溶液中,
C. 在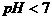 的溶液中,
的溶液中,
D. 在 的溶液中,
的溶液中,
10.下列离子方程式正确的是( )
A.把Fe(OH)3放入氢碘酸中: Fe(OH)3+3H+= Fe3++3H2O
B.Mg (HCO3)2溶液和足量的澄清石灰水反应:
Mg2++ 2HCO3-+ Ca2++ 2OH- = CaCO3↓+ MgCO3↓+ 2H2O
C.Ca(HCO3)2溶液和过量NaOH溶液反应: Ca2++HCO3-+ OH- = CaCO3↓+ H2O
D.把Mg粉放入FeCl3溶液中: 2Fe3++ 3Mg+ 6H2O= 2Fe(OH)3↓+3 Mg2++3H2↑
9.设NA为阿伏加德罗常数,下列叙述正确的是
A 1molFeCl3完全转化为Fe(OH)3胶体后生成NA个胶粒
B1molH2O2与MnO2充分反应转移2NA个电子
C将标准状况下,22.4LH2和4gHe均含有NA个分子
D50℃1×105pa下,46gNO2与0℃2×105pa下46gN2O4均含有3NA个电子
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com