
题目列表(包括答案和解析)
6.随着人们生活水平的提高,小汽车已进入平常百姓家。为了保护行驶人员的安全,常备有防撞气囊,内装有能在撞车后10ms(1ms=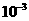 s)内发生爆炸性反应的物质
s)内发生爆炸性反应的物质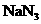 ,化学方程式为
,化学方程式为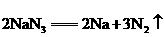 ,驾驶员可在汽车遭撞击后受气囊保护而脱险。此外,气囊内还装有陶土、
,驾驶员可在汽车遭撞击后受气囊保护而脱险。此外,气囊内还装有陶土、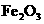 粉等物质,以使气囊内产生的
粉等物质,以使气囊内产生的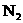 在100ms-200ms内消失,同时气囊内的Na变为
在100ms-200ms内消失,同时气囊内的Na变为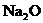 。下列说法中不正确的是( )
。下列说法中不正确的是( )
A.在1mol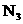 离子中共含有16mol电子
离子中共含有16mol电子
B.配方中,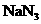 与
与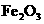 的物质的量之比应在6∶1左右
的物质的量之比应在6∶1左右
C.气囊内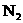 迅速消失的目的是在撞车时不致使人反弹
迅速消失的目的是在撞车时不致使人反弹
D.气囊的保护作用是通过延长作用时间实现的
5.在医院中,为酸中毒病人输液不应采用( )
A.0.9%氯化钠溶液 B.0.9%氯化铵溶液 C.1.25%碳酸氢钠溶液 D.5%葡萄糖溶液
4.下列电子式中错误的是( )
A.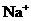 B.
B.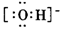 C.
C. D.
D.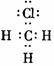
3.以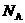 表示阿伏加德罗常数,下列说法中正确的是( )
表示阿伏加德罗常数,下列说法中正确的是( )
A.53g碳酸钠中含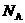 个
个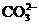 B.0.1mol
B.0.1mol 含
含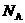 个电子
个电子
C.1.8g重水(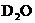 )中含
)中含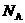 个中子 D.标准状况下11.2L臭氧中含
个中子 D.标准状况下11.2L臭氧中含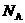 个氧原子
个氧原子
2.上海环保部门为了使城市生活垃圾得到合理利用,近年来逐步实施了生活垃圾分类投放的办法。其中塑料袋、废纸、旧橡胶制品等属于( )
A.无机物 B.有机物 C.盐类 D.非金属单质
1.下列物质一定不是天然高分子的是( )
A.橡胶 B.蛋白质 C.尼龙 D.纤维素
2.推断元素的思路


★例题精析
[例1]同周期的X、Y、Z三种元素,已知如下关系:XH3、H2Y、HZ酸性逐渐增强,则下列判断正确的是:
A.原子半径Z>Y>X B.Z的非金属性最强
C.氢化物的还原性XH3>H2Y>HZ
D.最高价氧化物对应水化物H3XO4
[例2]:A、B、C三种短周期元素,其原子序数依次增大,其中,A元素的最高正价与最低负价的代数和为零,原子的最外层电子数是次外层的2倍,B元素的原子半径是除H原子外所有半径中最小的。C元素的族序数与电子层相等,且处于元素周期表中的ⅢA族。A、B、C三种元素的名称及其在元素周期表的位置是:
A:_________________________________________
B:_________________________________________
C:_________________________________________
[例3]在周期表的主族元素中,甲元素与乙、丙、丁三种元素上下或左右紧邻,甲、乙两元素的原子序数之和等于丙元素的原子序数,这四种元素的最外层电子数之和为20,据此可以判断:元素甲为_____________________元素丙_____________________元素乙和丁所形成的化合物分子式为_____________________或______________________ 。
[例4]A、B、C、D、E、F为原子序数由小到大同周期的短周期元,己知:A、c、F三种原子的最外层共有11个电子,且这三种元素的最高价氧化物的水化物两两之间皆能反应,均能生成盐和水;D元素原子的最外层电子数比次外层电子数少4;E元素原子次外层电子数比最外层电子数多3。
(1)写出下列元素的的符号:A______________ D____________ E____________
(2)B单质在F的单质中燃烧的现象是____________________________________________
反应的化学方程式是___________________________________________________________
(3)A、C两种元素最高价氧化物的水化物反应的离子方程式是_________________________
解答:例1 B、C
例2 A碳 B氟 C 铝
|
例4(1)Na、Si、P (2)产生白烟,Mg+Cl2 = MgCl2
(3)OH-+Al(OH)3=AlO2-+H2O
1. 粒子半径的比较
①同主族元素的原子半径随核电荷数的增大而增大
②周期元素的原子半径随核电荷数的增大而减小
③电子层结相同的离子半径随核电荷数的增大而减小
④同主族元素的离子半径随核电荷数的增大
⑤金属元素的原子半径比离子半径大,非金属元素原子半径比相应的阴离子半径小
⑥同一元素的不同价态的粒子,价态高的离子半径小
4.元素周期表
(1)结构 周期:三短、三长、不完全
族: 七主、七副、Ⅷ与零
(2)表内元素性质递变(原子半径、金属性、最高价氧化物的水化物酸碱性、单质的性质等)
同周期(从左到右)
同族(从上到下)
(3)应用
①预测元素及对应化合物的结构、性质
②寻找未知元素及新物质
★巧思巧解
3.几种量
(!)质量数
(2)同位数的相对原子质量
(3)元素的平均相对原子质量
(4)元素的近似相对原子质量
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com