
题目列表(包括答案和解析)
8、醋酸可以通过分子间氢键双聚。一定温度下,将一定质量的冰醋酸加水稀释过程
中,溶液的导电能力变化如右下图所示,有关说法正确的是
A、a、b、c三点溶液的pH:a>b>c
B、用湿润的pH试纸测量c处溶液的pH值,比实际pH值偏小
C、a、b、c三点溶液用1mol/L氢氧化钠溶液中和,消耗氢氧化钠溶液体积:a>b>c
D、若在“O”点醋酸双聚成八元环分子,则其结构为:
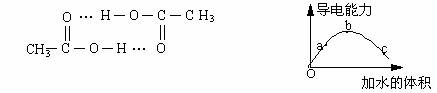
7、实验室利用反应:Na2S2O3+H2SO4====Na2SO4+S↓+SO2↑+H2O,以溶液变浑浊时间的长短来研究影响化学反应速率的因素,下列各组实验中化学反应速率最大的是
组号反应
|
组号 |
反应 温度 (℃) |
参加反应的物质 |
||||
|
Na2S2O3 |
H2SO4 |
H2O的 体积(mL) |
||||
|
体积(mL) |
浓度(mol·L-1) |
体积(mL) |
浓度(mol·L-1) |
|||
|
A |
10 |
5.0 |
0.10 |
10.0 |
0.10 |
5.0 |
|
B |
10 |
5.0 |
0.10 |
5.0 |
0.10 |
10.0 |
|
C |
30 |
5.0 |
0.10 |
5.0 |
0.10 |
10.0 |
|
D |
30 |
5.0 |
0.20 |
5.0 |
0.10 |
10.0 |
6、下列除去杂质的方法正确的是
A、除去CO2中的少量的HCl:通过足量的饱和碳酸氢钠溶液
B、除去N2中的少量的CO:通过足量的灼热的CuO粉末
C、除去KCl溶液中的少量CaCl2:加适量Na2CO3溶液,过滤
D、除去铜粉中混有的铁:加足量稀硝酸,过滤
5、最近有人用一种称为“超酸”的化合物H(CB11H6Cl6) 和C60反应,使C60获得一个质子,得到一种新型离子化合物[HC60]+[CB11H6Cl6]-。这个反应看起来很陌生,但反应类型上却可以跟下列一个化学反应相似,你认为该反应是
A、Mg +2HCl = MgCl2 + H2↑ B、NaOH + HCl = NaCl + H2O
C、NH3 +
HCl = NH4Cl D、H2O +CH3COOH  H3O+ +CH3COO
-
H3O+ +CH3COO
-
4、法国里昂的科学家最近发现一种只由四个中子构成的粒子,这种粒子称为“四中子”,也有人称为“零号元素”。下列有关“四中子”粒子的说法错误的是
A、该粒子不显电性 B、该粒子质量数为4
C、该粒子质量比已发现的氢原子大 D、在周期表中与氢元素占同一位置
3、下列物质按不同类别分组,所得组合最不合理的是
(1)糖类(2)塑料(3)石油(4)蛋白质(5)合成纤维(6)棉花(7)陶瓷(8)玻璃(9)天然气(10)水泥(11)合成橡胶(12)煤(13)油脂(14)羊毛
A、(1)(4)(13) B、(2)(5)(11)
C、(7)(8)(11)(14) D、(3)(9)(12)
2、2005年2月18日英国食品标准署就食用含有添加苏丹红色素的食品可能诱发癌症向消费者发出警告。我国也已开始追查含苏丹红色素的食品。所谓“苏丹红一号”实际上一般称为“苏丹一号”,是一种黄溶剂染料,按化学染料分类称为溶剂黄14(C.L.Solvent,Yellow14),分子式为C16H12N2O,其化学结构属偶氮类染料,是由苯胺重氮化后与2-萘酚偶合制得。有关苏丹红一号下列说法正确的是
A.苏丹红一号在食品中能起到增色的作用,可在辣椒酱中用作添加剂
B.从苏丹红一号分子中碳氢原子个数比例分析,其为不饱和烃
C.苏丹红一号可用于溶解剂、机油、蜡和鞋油等产品的染色
D.食品添加剂对人体危害较大,因此应全面禁止使用
1、唐代医书《外台秘要》一书中记载了水银霜的制法:将水银(即汞)和硫磺共炒后再加入NaCl灼炒之,倒扣一铜盆,片刻后,铜盆内壁便附着一层白色的水银霜。据此可知水银霜的化学成分为
A.HgS B.Na2S C.HgCl2 D.Hg2Cl2
3、电子得失守恒法
守恒法是化学计算的基本方法,电子得失守恒是其中的一种,但凡氧化还原反应别忘了电子得失守恒法的应用。
例:为了测定Cu、Ag合金的成分,将30.0g合金溶于80mL 13.5mol/L的浓HNO3中,待合金完全溶解后,收集到标准状况下6.72L气体,并测得溶液中c(H+)=1mol/L。若反应后溶液体积仍为80mL,试填写:
(1)产物中气体的成分(填化学式)及体积是 ;
(2)被还原的HNO3的物质的量为 ;
(3)合金中Ag的质量为 。
例题精析:
例1 在3BrF3+5H2O=HBrO3+Br2+O2↑+9HF反应中,若有2mol H2O被氧化,则被水还原的BrF3有几摩尔? (4/3 mol)
思考:P+CuSO4+H2O --H3PO4+Cu3P+H2SO4(未配平),问1mol CuSO4能氧化几摩尔P?
例2 配平下列化学方程式:
(1)CH4+O2+Na2O2--Na2CO3+NaOH
例3 将一定量的KClO3加热发生部分分解,然后向反应物中加足量的浓H2SO4并加热,发生如下反应:KClO3+5KCl+3H2SO4  3Cl2↑+3K2SO4+3H2O,如果原KClO3为A mol,
3Cl2↑+3K2SO4+3H2O,如果原KClO3为A mol,
第一步反应KClO3的分解率为a,两步反应产生的O2和Cl2共n mol。
(1)计算当氯元素全部转化为Cl2时a、n的值。(a=5/6,n=1.75A)
(2)讨论a在不同取值范围内的n值,并与(1)中所得n值比较,确定n的最大值。(1.75A)
MnO4― +H2S +H+ = 2Mn2+ +5S↓+8H2O
3Cu2S + 4NO3― +16H+ = 6Cu2+ +3S↓+4NO↑+8H2O
例(1)NO2:2.24L;NO:4.48L (2)0.3mol (3)10.8g
例1. 4/3
例2. 2CH4 +O2 +6Na2O2 =2Na2CO3 +8NaOH
2、重要的氧化剂和还原剂
重要的氧化剂:
(1)活泼非金属单质,如F2、Cl2、Br2、O2 、I2、O3 等。
(2)高价含氧化合物,如浓H2SO4、HNO3、KMnO4、HClO、KClO3、MnO2、Na2O2、
H2O2、K2Cr2O7等。
(3)高价金属阳离子,如Ag+、Hg2+、Fe3+、Cu2+等。
重要还原剂:
(1)活泼金属及某些非金属单质,如Na、Mg、Al、H2、C、Si等;
(2)低价态化合物,如CO、H2S、HCl、SO2、NH3等;
(3)低价态的某些离子,如S2―、SO32―、Fe2+、I―等。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com