
题目列表(包括答案和解析)
3.下列叙述或表示方法中,正确的是
A.等质量的硫蒸汽和硫固体完全燃烧,后者放出的热量多
B.由C(石墨)→ C(金刚石);△H=+119kJ/mol可知,金刚石比石墨稳定
C.在稀溶液中:H++OH-==H2O;△H=-57.3kJ/mol。若将含1molCH3COOH与含1molNaOH的稀溶液混合,放出热量小于57.3kJ
D.1L 0.5mol/L稀硫酸与1L1mol/L的NaOH溶液反应,放出57.3kJ的热,于是有:
H2SO4(aq)+2NaOH(aq)==Na2SO4(aq)+2H2O(aq);△H=-57.3kJ/mol
2.进行下列实验操作时,一般情况下不得相互接触的是
A. 配制溶液时,用以引流的玻璃棒与容量瓶内壁
B.过滤时,漏斗的下端与盛接滤液的烧杯内壁
C.实验室将HCl气体溶于水时,采用的倒置漏斗口与烧杯内的水面。
D.用以检验氨气的湿润红色石蕊试纸与产生氨气的试管口
1.下列说法中,正确的是
A.由同种元素组成的物质一定是纯净物
B.由两种元素组成的分子中一定不存在非极性共价键
C.含有离子键的化合物一定是离子化合物
D.含有极性共价键的分子一定是极性分子
26、(12分)在标准状况下将cmolCl2通入含amolFeBr2、bmolFeI2的溶液中,当c取不同值时,反应后所得溶液中有不同溶质(不考虑生成物与水的反应)。
(1) 将下表中空格填满:
|
c的取值(用含a、b的代数式表示) |
反应后溶液中溶质的化学式 (只要求写盐类化合物) |
|
|
FeBr2、FeI2、FeCl2 |
|
b≤c<1/2(a+3b) |
|
|
|
FeBr3、FeCl3 |
|
|
FeCl3 |
(2)若a=b=1 、c=2时,反应后溶液中属于盐类的溶质是 (写化学式),这些溶质的物质的量之比是 ;
(3)若a=b=1 、c=2.5时,写出Cl2通入溶液中总的离子方程式(限写一个,但需包括所有的离子反应):_________________________________________________________.
25、(6分)有一瓶(约100mL)硫酸和硝酸的混合溶液,取出10.00mL该混合溶液,加入足量氯化钡溶液,充分反应后过滤、洗涤、烘干,可得4.66g沉淀。滤液跟2.00mol/LNaOH溶液反应,共用去35.00mL碱液时恰好中和。试完成下列
(1)则混合溶液中硝酸的物质的量浓度 c (HNO3) = mol/L
(2)另取10.00mL原混酸溶液,加入1.60g铜粉共热,反应的离子方程式为:
在标准状况产生的气体体积为 mL。

 23、(8分)右下图为某有机物的结构简式,每个节点处代表有一个碳原子,与其结合的氢原子的元素符号省略,这种化学式称为“键线式”。又知酯类在铜铬氧化物(CuO·CuCrO4)催化下,与氢气反应得到醇,羰基双键可同时被还原,但苯环在催化氢解过程中不变,其反应原理如下:
23、(8分)右下图为某有机物的结构简式,每个节点处代表有一个碳原子,与其结合的氢原子的元素符号省略,这种化学式称为“键线式”。又知酯类在铜铬氧化物(CuO·CuCrO4)催化下,与氢气反应得到醇,羰基双键可同时被还原,但苯环在催化氢解过程中不变,其反应原理如下:
RCOOR’+2H2 RCH2OH+HO-R’
试填空:
(1)该有机物分子中的三个苯环_________ 共平面
(选填“能”或“不能”)。
(2)该有机物的的化学式为 ________________。
(3)该有机物与足量氢氧化钠溶液充分反应后的产物中,相对分子质量较小钠盐的化学式为 ____________________________________________________________________。
(4)1mol该有机物在铜铬氧化物催化下能与 ______________mol氢气充分反应。
24、(10分)我国第二代身份证采用的是具有绿色环保性能的PETG新材料,PETG新材料可以回收再利用,而且对周边环境不构成任何污染。这一材料是由江苏华信塑业发展有限公司最新研发成功的新材料,并成为公安部定点产地。PETG的结构简式为: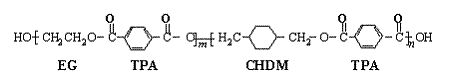
已知:
(1)
(2)RCOOR1 +R2OH  RCOOR2 +R1OH (R、R1、R2表示烃基)
RCOOR2 +R1OH (R、R1、R2表示烃基)
这种材料可采用下列合成路线
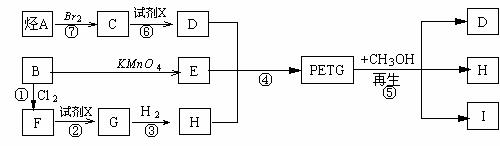
试回答下列:
(1)反应②⑥加入的试剂X是 ; (2)⑤的反应类型是 ;
(3)写出结构简式:B I ;(4)合成时应控制的单体的物质的量
n(D)∶n(E)∶n(H)= ∶ ∶ (用m、n表示)
(5)写出化学方程式:
反应③ _;反应⑥ _____。
22、(10分)已知A-F是中学化学中常见物质,其中A、C、E、F为气体,B、D为液体,D的消费量常作为一个国家工业发达水平的一种标志,F的浓溶液与X共热通常用于实验室制备单质C,X是一种黑色粉末,B分子中有18个电子。反应中部分生成物已略去。
试回答下列:

(1)根据图中信息,B、C、D、X氧化性从强到弱的顺序是 。
(2)B的电子式为: 。
(3)写出反应②的化学方程式: 。
(4)写出反应①、⑥的离子方程式
①__________________________________________________;
⑥__________________________________________________。
21、(8分)有A、B、C、D、E五种短周期元素,它们的原子序数依次增大,其中B是地壳中含量最多的元素。已知A、C及B、D分别是同主族元素,且B、D两元素原子核内质子数之和是A、C两元素原子核内质子数之和的2倍;在处于同周期的C、D、E三元素中,E的原子半径最小;通常条件下,五种元素的单质中有三种气体,两种固体。
试比较D、E两元素的最高价氧化物对应水化物的酸性强弱(填写化学式)
_____________ > ______________ 。
(2)将E单质通入A、B、C三种元素组成的化合物的水溶液中,写出反应的化学方程式:_____________________________________________________________ 。
(3)写出两种均含A、B、C、D四种元素的化合物在溶液中相互反应、且生成气体的离子方程式:_______________________________________________________________。
(4)用A单质和B单质可制取气体燃料电池,该电池用多孔的惰性电极浸入浓KOH溶液,两极分别通入A单质和B单质。写出该电池的电极反应方程式:
负极 :____________________________________;
正极 :_______________________________________。
20、(12分)常温下甲醛是一种无色、有特殊刺激性气味的气体,易溶于水,是世界卫生组织(WHO)确定的致癌物和致畸形物之一。我国规定:居室空气中甲醛的最高容许浓度为0.08mg/m3。
某研究性学习小组设计用如下方法测定某居室空气中甲醛的含量(假设空气中无其它还原性气体):
⑴ 测定原理: KMnO4(H+)溶液为强氧化剂,可氧化甲醛和草酸,
化学反应离子方程式为: 4MnO4-+ 5HCHO + 12H+ == 4Mn2+ + 5CO2↑+ 11H2O
2MnO4-+ 5H2C2O4 + 6H+ == 2Mn2++10CO2↑+ 8H2O
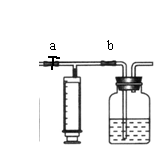
⑵ 测定装置:部分装置如下图所示(a、b为止水夹)
|
|


⑶ 实验步骤:
① 检查装置气密性(气密性良好)。
② 用 (填仪器名称)准确移取25.00 mL 1.00×10-3mol·L-1的高锰酸钾溶液(过量)于广口瓶中并滴入3滴6mol·L-1H2SO4溶液备用。
③ 将2.00×10-3mol·L-1的草酸标准溶液置于 (填仪器名称)中备用。
④ 打开a,关闭b,用注射器抽取100mL新装修的室内空气。关闭a,打开b,再缓缓推动注射器,将气体全部推入酸性高锰酸钾溶液中,使其充分反应。再如此重复4次(共5次)。如果压送气体时速度过快,可能会产生什么不利后果?
_________________________________________________________;
⑤ 将广口瓶中的溶液转入锥形瓶中(润洗广口瓶2-3次,并将洗涤液全部转入锥形瓶)。如果没有润洗,所测甲醛的含量将 (填“偏高”、“偏低”、“无影响”);
⑥ 用标准草酸溶液滴定锥形瓶中的溶液;记录滴定所消耗的草酸溶液体积。
本实验是否需要指示剂?(如果需要,请写出指示剂的名称;如果不需要,试说明终点时的实验现象)。 。
⑦ 再重复实验2次。
⑷ 数据处理:分别于装修完工后的第1天、第7天、第30天(室内始终保持通风换气状况)对室内空气进行取样,通过实验测得以下三组数据(每次实验所取的KMnO4溶液均为 25.00mL):
|
装修后 第n天 |
草酸溶液(mL) |
甲醛的浓度 mg/m3 |
|||
|
1 |
2 |
3 |
平均值 |
||
|
1 |
15.86 |
15.72 |
15.67 |
15.75 |
|
|
7 |
26.17 |
26.36 |
26.38 |
26.27 |
|
|
30 |
30.90 |
30.67 |
30.81 |
30.79 |
|
设 KMnO4溶液的物质的量浓度为c1,KMnO4溶液的体积为V1(mL);
草酸溶液的物质的量浓度为c2,草酸溶液的平均体积为V2(mL)
则:计算室内空气中甲醛浓度(mg/m3)的代数式为 ,计算第30天室内空气中甲醛浓度为_____________(精确到小数点后二位),并判断此时主人________(填“能”或“否”)入住。
19、 (10分)⑴下列仪器中,根据物质的沸点不同分离物质时需要的是
(填编号)。
(10分)⑴下列仪器中,根据物质的沸点不同分离物质时需要的是
(填编号)。
 ①容量瓶 ②普通漏斗 ③蒸馏烧瓶
①容量瓶 ②普通漏斗 ③蒸馏烧瓶
④天平 ⑤分液漏斗 ⑥滴定管
⑦燃烧匙 ⑧温度计 ⑨干燥管
⑵ 右图分别是温度计、量筒、滴定管的一
部分,下述读数(虚线刻度)及说法正确
的是 。
A.①是量筒,读数为2.5mL
B.②是量筒,读数为2.5mL




 C.③是滴定管,读数为3.5mL
C.③是滴定管,读数为3.5mL
D.①是温度计,读数为2.5℃
⑶ 实验室里不同化学试剂的保存方法不尽相同。下图中A、B、C、D、E是常见的一些保存药品的试剂瓶。请把下列常见试剂的序号填写在各试剂瓶下面的括号内(多选倒扣分):
①NaOH溶液 ②浓硫酸 ③Na2CO3溶液 ④白磷 ⑤大理石 ⑥酒精 ⑦氯水 ⑧浓硝酸
|
A |
B |
C |
D |
E |
 |
 水 水 |
 |
 |
 |
|
( ) |
( ) |
( ) |
( ) |
( ) |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com