
题目列表(包括答案和解析)
12、A(NH3的存在将促进SO32-的生成,而出现BaSO3;Cl2 、NO2的存在将使SO2氧化生成SO42-,而生成BaSO4) 13、AB 14、CD 15、BA 16、A 17、D (强碱的PH=13,强酸的PH=2,因为PH之和为15,故强碱和强酸的体积比按1:10混合时,混合液为中性,但题设条件为碱性。因此,强酸的体积应减少,故选D选项正确) 18、AB(由已知数据可知A正确;由S元素守恒和“等体积”混合可知,D正确)
19(1)3分,用镊子夹取白磷,在盛有水的水槽中切割(其它合理答案同样给分) (2) BC(4分:只选一个得2分,选两个且都正确得4分,多选不得分)
1.C 2、B 3、A 4、B 5、C D(因为n(M2+)=n(XO3n-),故n=2,由此可推得XO32-中X的化合价为+4)6、 CD 7、B 8、C(硫酸的密度大于1)9、C 10、AC 11、B
25.(12分) 仔细分析下列各题后回答问题:
(1)高炉炼铁中发生的基本反应之一如下:FeO(s)+CO(g) Fe(s)+CO2(g);(ΔH>0).①对上述反应,在由于升高温度而使化学平衡移动的过程中,高炉内CO2和CO的体积比_________(填“增大”“减小”或“不变”)。
Fe(s)+CO2(g);(ΔH>0).①对上述反应,在由于升高温度而使化学平衡移动的过程中,高炉内CO2和CO的体积比_________(填“增大”“减小”或“不变”)。
②在1100℃时,上述反应达到平衡后,测得CO2和CO的体积比为0.263.在该温度下,如果某时刻C(CO2)=0.025 mol/L、C(CO)=0.1 mol/L,在这种情况下,该反应是否处于化学平衡状态_________(填“是”或“否”);此时,其化学反应速率v(正)_____v(逆)(填“大于”、“小于”或“等于”),
其原因是__________________ ____.
(2)在真空密闭容器中,加入a mol PH4I固体,在一定温度下发生如下反应:
PH4I(s)
 PH3(g)+HI(g)
PH3(g)+HI(g)
4PH3(g)
 P4(g)+6H2(g)
P4(g)+6H2(g)
2HI(g)
 H2(g)+I2(g)
H2(g)+I2(g)
以上三反应建立平衡后,测得HI为b mol,I2(g)为c mol,H2为d mol,求
①平衡后,容器内P4(g)和PH3的物质的量(用代数式表示)分别为________、________.
②a,b,c三者的关系服从a>_________(填含b,c的代数式) b,c,d三者的关系服从b>_________(填含c,d的代数式)
③平衡后,增大压强,容器内n(I2)___________,n(PH4I)_________(填“增加”、“减少”、或“不变”
24.(10分)一定量的Fe和Fe2O3的混和物投入250 mL 2 mol/L 的硝酸溶液中,固体完全溶解后,收集到1.12 L NO(标况下)。欲使铁元素完全沉淀,问向反应后的溶液中加入1 mol/L NaOH溶液多少毫升?
23.(8分)对A、B两种有机物的研究分别获取了如下信息:
①化合物A的相对分子质量小于300.
②在化合物A中ω(C)=71.58%,ω(H)=6.67% , ω(N)=4.91%,其余是氧元素.
③1 mol B水解得到1 mol A和2 mol醋酸.由此确定:(1)化合物A的相对分子质量为_________;化合物B和化合物A相对分子质量之差____ _____.
(2)化合物A的分子式为___________,化合物B的分子式为___________.
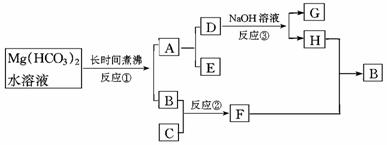
22.(18分)在下列物质间的转化关系中,反应③为电解,每个框中的字母只代表一种物质。试回答:
(1)A的化学式_ __.
(2)反应①的化学反应式,_________ ____;
简述能生成A物质的原因_ __.
(3)反应②的化学反应式_________ ____;
反应的现象是____ __.
(4)反应③中加入NaOH溶液的原因是____________________ ________________.
21.(7分)将Cl2通入足量浓NaOH和H2O2的混合溶液中,发生了一系列的化学反应,最后由于ClO-和H2O2发生反应而放出氧气,并伴随着有闪烁的红光出现。
(1)写出最后生成氧气的离子方程式
__________________________________ ___________.
(2)上述反应中被氧化的元素是__________________.
 (3)若反应中消耗了0.3 mol ClO-,则发生转移的电子数目是________________.
(3)若反应中消耗了0.3 mol ClO-,则发生转移的电子数目是________________.
20.(15分) 已知常温常压下CO2在水中的溶解度不大,CO2与NaOH溶液反应时没有明显现象,某研究小组同学,设计了下图A-E五套装置。欲利用这些装置,能通过观察现象,间接证明CO2与NaOH溶液发生了反应。
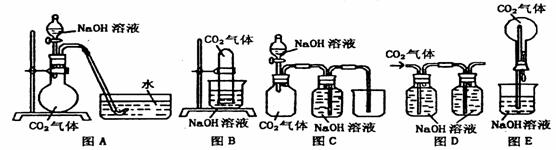
请选用以上实验装置,同时指出操作规程方法和观察到的实验现象,将答案填入下表:(表中已有一个示例)
|
所选装置 |
操作方法 |
实验现象 |
|
B |
将充有CO2试管的橡皮塞打开 |
水槽中NaOH溶液上升到试管中 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
19.(8分) (1)白磷的着火点为40℃,在室温或夏天正常取出时,就可观察到其被氧化而冒”白烟”,请简单说明将如何将大块的白磷切变成小块的白磷。
(2)某学生在实验报告中写出以下的实验操作或实验数据,你认为合理的是 ( )
A.用托盘天平称取29.25g的食盐;B.用湿润的pH试纸测得某溶液的pH为10
C.将浓硫酸沿容器器壁缓缓地倒入酒精中,并不断搅拌;
D.用酸式滴定管量取已知浓度的KMn04溶液20.00mL;
E.做中和滴定实验时,锥形瓶用待测液润洗
18.将0.02 mol/L的HCl溶液与0.04 mol/L 的NaHS溶液等体积混合后,溶液显酸性,则下列关系式中正确的是 ( )
A.c(Na+)>c(Cl-) B.c(H2S)+c(HS-)+c(S2-)=0.02mol/L
C.c(H+)=c(Cl-) D.c(HS- )<c(H2S)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com