
题目列表(包括答案和解析)
3.在加入少量Al(OH)3能溶解的无色溶液中,加入下列各组离子,有可能在溶液中大量共存的是( )
A.NH4+、Na+、HCO3-、ClO- B.K+、MnO4-、NO3-、SO42-
C.Ca2+、Fe2+、Cl-、NO3- D.Na+、AlO2-、SO32-、S2-
2.下列反应的离子方程式错误的是 ( )
A.向碳酸氢钙溶液中加人过量氢氧化钠
Ca2++2HCO3-+2OH- = CaCO3↓+2H2O+CO32-
B.等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合
Ba2++2OH-+NH4++HCO3- = BaCO3↓+NH3·H2O+H2O
C.氢氧化铝与足量盐酸反应 Al(OH)3+3H+ = Al3++3H2O
D.过量CO2通入氢氧化钠溶液中 CO2+2OH- = CO32-+H2O
1.下列离子方程式中正确的是 ( )
A.过量的NaHSO4与Ba(OH)2溶液反应:Ba2++OH-+H++SO42-= BaSO4↓+H2O
B.NH4HCO3溶液与过量NaOH溶液反应:NH4++OH-=NH3↑+H2O
C.苯酚钠溶液中通入少量CO2: -O-+CO2+H2O→
-O-+CO2+H2O→ -OH+HCO3-
-OH+HCO3-
D.FeBr2溶液中通入过量Cl2:2Fe2++2Br-+2Cl2 = 2Fe3++Br2+4Cl-
8.(10分)某无色溶液,其中有可能存在的离子如下:Na+、Ag+、Ba2+、Al3+、AlO2-、S2-、CO32-、SO32-、SO42-,现取该溶液进行有关试验,实验结果如下图所示:


试回答下列问题:
(1)沉淀甲是:___________________________,
(2)沉淀乙是:_________________,由溶液甲生成沉淀乙的离子方程式
为:_____________ ___.
(3)沉淀丙是:__________________.
(4)气体甲成分可能有哪几种?(可以不填满也可以补充)
|
1 |
2 |
3 |
4 |
5 |
6 |
|
|
|
|
|
|
|
(5)综合上述信息,可以肯定存在的离子:____ ___________.
课后练习
7.测定水中溶解氧气的方法是:取a mol水样,迅速加入MnSO4溶液及含有NaOH的KI溶液,立即塞好塞子、振荡,使反应充分;开塞,迅速加入适量H2SO4,此时有I2生成;用Na2S2O3溶液(浓度b mol·L-1)和I2反应,消耗了V mL达到终点(以淀粉作指示剂)。有关方程式为:
①2Mn2++O2+4OH-===2MnO(OH)2(反应很快)
②MnO(OH)2+2I-+4H+===Mn2++I2+3H2O
③I2+2S2O32-===S4O62-+2I-
(1)需要进行滴定的反应是___________________,终点的颜色变化为__________________。
(2)水中溶解O2为(以mg/L为单位)_____________________。
(3)加MnSO4及含NaOH的KI溶液振荡时,塞子若未塞紧(设未溅出溶液),测得结果将___________(填“偏高”“偏低”或“无影响”),原因是_____________________。
6.在含有Na+、Mg2+、HCO3-、SO42-的稀溶液中,它们的物质的量之比为2:1:2:1。
(1)向该溶液中滴加酚酞试液数滴,溶液呈淡粉红色,有关反应的离子方程式为_____________________。
(2)充分加热(1)步所得的溶液,加热的过程中观察到的现象有___________;完全反应后,溶液呈___________色,有关反应的离子方程式为_______________________。
5.下列离子方程式正确的是
A.向Ba(OH)2溶液与稀H2SO4溶液发生中和反应:Ba2++OH-+H++SO42-==BaSO4↓+H2O
B.H2S通入FeCl3溶液中 : 2Fe3++S2-=2Fe2+ +S↓
C.碳酸氢钠溶液与硫酸氢钠溶液反应 : HCO3-+H+==CO2↑+H2O
D.向漂白粉溶液中通入SO2 : Ca2++2ClO-+SO2+H2O==CaSO3↓+2HClO
4.下列反应的离子方程式书写正确的是
A. 向饱和碳酸氢钙溶液中加入过量氢氧化钙溶液:
Ca2++2HCO3-+2OH-=CaCO3↓+2H2O + CO32-
B.金属铝溶于氢氧化钠溶液:Al+2OH-=AlO2-+H2↑
C.用氢氧化钠溶液吸收二氧化碳:2OH-+CO2=CO32-+H2O
D.Mg(HCO3)2 溶液 与过量 NaOH 溶液反应:
Mg2++2HCO3-+2OH- = MgCO3↓+ CO32-+2H2O
3.下列反应的离子方程式正确的是()
A.在硫酸铁溶液中加入足量氢氧化钡溶液:Ba2++SO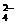 ===BaSO4↓
===BaSO4↓
B.硫化钠水解:S2-+2H2O H2S+2OH-
H2S+2OH-
C.硫酸铜溶液中通入过量的硫化氢:Cu2++S2-===CuS↓
D.溴化亚铁溶液中通入过量氯气:2Fe2++4Br-+3Cl2===2Fe3++6Cl-+2Br2
2.常温下测得某无色溶液中由水电离出的H+浓度为1×10-13mol/L,又知该溶液中还有NO-3,Na+,Cl-,那么该溶液中还一定存在的离子是 ()
A.AlO2-、ClO- B.Mg2+、、SO42- C.Fe2+ 、Cu2+ D.Ba2+、K+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com