
题目列表(包括答案和解析)
0.1mol.L-1NaHA溶液:
NaHA= Na++ HA-
11.解析:本题考查元素及化合物知识,属于基本题型,但同时也考查学生的知识应用能力,特别是:“原子守恒”、“差量法”的运用。反应的总方程式为: 2CH4+O2+6Na2O2==2Na2CO3+8NaOH
12解析:本题考查学生处理问题的能力和知识的迁移能力,考查学生对烃的衍生物的性质的熟练程度
13解析:本题属于图框式元素及其化合物推断题,是近几年高考的常见题型,要求考生知识全面,善于抓住突破口,大胆猜想和推理,周密思维,从而得出正确的结果。
从图中得出的第一印象是丙几乎无处不在,联想到以下几条的反应路线可得出丙是O2


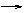 ①Na Na2O Na2O2 NaOH、O2
①Na Na2O Na2O2 NaOH、O2



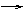 ②S SO2 SO3 H2SO4 O2、H2
②S SO2 SO3 H2SO4 O2、H2



 ③N2 NO NO2 HNO3 O2、H2
③N2 NO NO2 HNO3 O2、H2
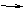
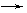
 根据组成三种单质的元素的核电荷数之和为35,(或根据B+C D是Na2O+SO2 Na2SO3,而Na2O+NO 不反应),可推知三种单质分别是Na、S、O2而非Na、N2、O2,则:
根据组成三种单质的元素的核电荷数之和为35,(或根据B+C D是Na2O+SO2 Na2SO3,而Na2O+NO 不反应),可推知三种单质分别是Na、S、O2而非Na、N2、O2,则:



 产物之一
产物之一


 Na O2 Na2O O2 Na2O2 水 O2
Na O2 Na2O O2 Na2O2 水 O2
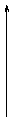





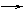
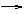
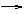 Na2S
Na2SO3 O2 Na2SO4 ②电
Na2S
Na2SO3 O2 Na2SO4 ②电
解






 S O2 SO2 O2 ① SO3 水 H2SO4溶液
S O2 SO2 O2 ① SO3 水 H2SO4溶液
考试时,将物质推出来仅是成功了一半,要养成认真、准确、规范地答题的习惯,以免无谓失分。
14解析:.电解质溶液试题在今几年的全国高考,上海高考Ⅱ卷中屡有出现,这是一道另辟蹊径,思维要求较高的题目。
第(1)问要求书写水解方程式,符合规范才能得分。
第(2)问:A选项只要注意到H2A第一步电离是完全的,就能判断H2A在水溶液中不存在,从而否决它。B选项实质是物料守恒式。C选项实质是电荷守恒式。D选项反映的是:
[OH- ](水电离)= [H+](水电离)。
第(4)问的解答融于第(3)问的解答之中
7. 解析:本题考查学生处理信息的能力和知识的迁移能力。
8解析:本题考查学生利用氧化还原中“化合价升降的总数相等”来解决问题的能力,不必对方程式进行配平,
9解析:本题考查学生对阿伏加德罗常数的正确理解,同时靠查原子结构的基本知识,属于结构的基本问题,学生容易解答
10解析:本题考查学生对化学用语“离子方程式”的理解,以及在书写时应注意的问题,特别是用到“量”和“氧化还原反应”问题时。
6.解析:本题考查学生信息处理能力和基础知识的应用能力,充分利用氧化还原反应的知识来解答,同时利用化合价的代数和为零,
n(Cr3+)= 2.667/(127*2)*2/3=0.007(mol) n(Cl)=4.52/143.5=0.0315(mol) n(Cr3+): n(Cl)=2:7
5.解析:本题考查学生的综合应用能力,用一般的解法就较复杂,如果用“Cu原子守恒”和“关系式法”来解,就变得很简单了:CuCl2~~2HCl由这一关系式可得
CuCl2为0.3mol,CuCO3 →CuO , Cu2(OH)2CO3→2 CuO, CuO-2HCl
4.解析:本题考查学生的知识迁移能力,注重质量守恒定律的理解。
3.解析:本题考查学生化学式中“正负化合价的代数和为零”的知识,属于基本体型学生容易解答,
2.解析:本题考查学生用化合价升降的知识来解决判断氧化还原反应,属于很基本的题型
1.解析:本题考查学生对元素周期表的熟悉情况,特别是原子结构的变化规律。前10号元素最多有两个电子层电子层数之比为1:2或1:1,但只有同一主族最外层电子数相同而电子层数不同,故比值为1:2才满足。
20.(1). 4FeS2 + 11O2 = 2Fe2O3 + 8SO2
(2)接触室、吸收塔
(3) SO2 + O2 = 2SO3
(4)净化二氧化硫和氧气。(因为三氧化硫很易跟水蒸气化合生成酸雾,会影响二氧化硫跟氧气的化合,以及三氧化硫的吸收。)
(5)可以通过调节气阀,控制气体流量,观察甲装置的冒泡速率估计。
(6)原因有两个:
(1)浓硫酸对三氧化硫的吸收效果远好于水,三氧化硫被浓硫酸完全吸收了;
(2)插入浓硫酸溶液的导管插得太深,导致两个吸收瓶内的气压差较大,三氧化硫气体往水中冒出来了,与水蒸气化合形成酸雾。
(7) 用碱液吸收。
命题意图和试题解析
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com