
题目列表(包括答案和解析)
4.中学化学课本中有大量的数据材料,下面是某学生对数据的利用情况,其中不正确的是 ( )
A.利用液体密度可以判断液体物质挥发性的大小
B.利用固体溶解度数据可判断AgCl与KI溶液能否反应
C.由原子(或离子)半径数据可推断某些原子(或离子)的氧化性或还原性强弱
D.利用沸点数据可推测将一些液体混合物分离开来的可能性
3.在体积恒定的密闭容器中,充入3 molA和1 molB发生反应3A(g) + B(g) xC(g) 达到平衡后,C在平衡混合气中的体积分数为A%。若维持温度不变,以1.2 mol A、0.4
mol B、0.6 mol C为起始物质,达到平衡后C的体积分数仍为A%,则x值可能是
( )
xC(g) 达到平衡后,C在平衡混合气中的体积分数为A%。若维持温度不变,以1.2 mol A、0.4
mol B、0.6 mol C为起始物质,达到平衡后C的体积分数仍为A%,则x值可能是
( )
A.1 B.2 C.3 D.4
2.右图中曲线表示原子序数在前20号中的某些连续的元素单质沸点的变化规律(原子序数按递增顺序连续排列),其中A点表示的元素是 ( )
A.Si B.A1
C.Cl D.S
1.下列叙述不正确的是 ( )
A.淀粉、纤维素、油脂都属于天然高分子化合物
 B.能发生酯化反应的酸不一定都是羧酸
B.能发生酯化反应的酸不一定都是羧酸
C.天然蛋白蛋水解的最终产物均是α-氨基酸
D.油脂水解得到的醇是丙三醇
9.某化学课外活动小组对某气体混合物样品设计了如下步骤进行实验。
①取一个配有合适胶塞且洁净、干燥的500mL锥形瓶,用精确度为0.001g的分析天平(下同)准确称量,得到质量为ml。
②往锥形瓶中通入足量的干燥的该气体混合物样品,塞好瓶塞,准确称量,得到质量为m2。
③往锥形瓶中加满水,塞好瓶塞,称量,得到质量为m3。
④查得水的密度为d水(g·cm-3),空气的密度为d空气(g·cm-3),空气的平均相对分子质量为29.0,则该气体混合物样品的平均相对分子质量为: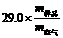 。
。
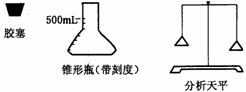 所用的仪器如图:
所用的仪器如图:
请回答下列问题:
(1)实验目的:__________________________________。
(2)计算:
①锥形瓶中空气的质量(写出算式)m空气=______________________________;
②锥形瓶中样品的质量(写出算式)m样品=_______________________________。
(3)问题与讨论:
问题一:实验完成后,有的同学提出,实验不是在标准状况进行的,应该记录实验的温度(T℃)和压强(PkPa),并对有关数据进行换算,你认为是否有必要,并说明理由。
问题二:老师对该小组的实验设计进行点评时指出:为了使实验数据合理、有效,在每次测量时,锥形瓶中的气体(或水)体积都应该相等。对此,你认为应采取的操作是什么?
8.向含下列微粒的溶液中,①HS- ②Fe2+ ③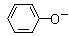 ④
④ 分别加入少量氢氧化钠固体,或少量浓盐酸或几滴酸性KMnO4溶液。(溶液体积变化忽略不计),都使溶液中对应的离子或分子浓度减少的是( )
分别加入少量氢氧化钠固体,或少量浓盐酸或几滴酸性KMnO4溶液。(溶液体积变化忽略不计),都使溶液中对应的离子或分子浓度减少的是( )
A.①④ B.②③ C.①② D.③④
7.根据“绿色化学”的思想,某化学家设计了下列化学反应步骤:
①CaBr2+H2O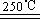 CaO+2HBr ②2HBr+Hg
CaO+2HBr ②2HBr+Hg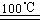 HgBr2+H2↑
HgBr2+H2↑
③HgBr2+CaO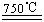 HgO+CaBr2 ④2HgO
HgO+CaBr2 ④2HgO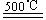 2Hg+O2↑
2Hg+O2↑
该方案的目的是为了制备 ( )
A.HBr B.CaO C.H2 D.Hg
6.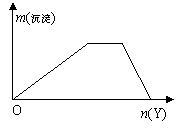 向X溶液中加入Y试剂,产生的沉淀质量随Y的量的变化如图所示,则符合条件的是( )
向X溶液中加入Y试剂,产生的沉淀质量随Y的量的变化如图所示,则符合条件的是( )
A.向NaOH和Ca(OH)2的混合溶液中通入CO2
B.向HCl和AlCl3的混合溶液中滴加NaOH溶液
C.向NH4Cl和AlCl3的混合溶液中滴加NaOH溶液
D.向NH4Cl和MgCl2的混合溶液中滴加NaOH溶液
5.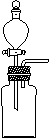 某课外活动小组欲利用如图所示装置制取少量O2、HCl和NH3三种气体,下列所选择的反应试剂均正确的是( )
某课外活动小组欲利用如图所示装置制取少量O2、HCl和NH3三种气体,下列所选择的反应试剂均正确的是( )
|
|
制取O2 |
制取HCl |
制取NH3 |
|
A |
KClO3和MnO2 |
NaCl(固)和浓H2SO4 |
NH4Cl(固)和Ca(OH)2(固) |
|
B |
MnO2和H2O2 |
浓H2SO4和浓HCl |
浓氨水和CaO |
|
C |
Na2O2和H2O |
浓H2SO4和浓HCl |
浓氨水和NaOH(固) |
|
D |
KMnO4(固) |
NaCl(固)和浓H2SO4 |
NH4Cl(固)和Ca(OH)2(固) |
4.将溶质的质量分数为2a%、物质的量浓度为c1 mol·L-1的氨水溶液加入一定量的水,使其溶质的质量分数变为a%,此时物质的量浓度为c2 mol·L-1,则c1和c2的关系是( )
A.c1>2 c2 B. c1<2 c2
C.c2=2c1 D. c1=2c2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com