
题目列表(包括答案和解析)
15、已知下列两个热化学方程式
2H2(气)+O2(气)=2H2O(液);ΔH=-571.6KJ/mol
C3H8(气)+5O2(气)=3CO2(气)+4H2O(液); ΔH=-2220KJ/mol
实验测得氢气和丙烷的混合气体共5mol,完全燃烧时放出热量3847KJ,则混合气体中氢气和丙烷的体积比为
(A)、3:1 (B)、1:4 (C)、1:3 (D):1;1
阳泉一中高考化学复习单元过关
班级 姓名 成绩
14.将3.20g Cu跟30.0mL 10.0mol·L-1的HNO3充分反应,还原产物有NO和NO2.若反应后溶液中有a mol H+离子,则此时溶液中含NO3-离子的物质的量为
(A) (a+0.5)mol (B)2 a mol (C)0.1 a mol (D)(a+0.1)mol
13.下列各组在溶液中反应,不管反应物量是多少,都能用同一离子方程式表示的是 (A).FeBr2与Cl2 (B).Ba(OH)2与H2SO4 (C).HCl与Na2CO3 (D).Ca(HCO3)2与NaOH
12.下列微粒①Al3+ ②Cl- ③N2 ④MnO4- ⑤CO2 ⑥H2O2 ⑦Fe2+ ⑧MnO42-
既具有氧化性又具有还原性的是 (A).①④⑤⑦ (B).③⑥⑦⑧ (C).④⑤⑥⑧ (D).①②③⑥
11、根据以下四个反应:
(1)H2S+I2=2H++2I-+S¯ (2)H2SO3+2H2S=3S¯+3H2O
(3)2I-+Br2=2Br-+I2 (4)H2SO3+I2+H2O=H2SO4+2HI
确定Br-、I-、H2S和H2SO3还原性由强到弱的顺序是
(A)H2S>H2SO3>I->Br- (B)Br->I->H2SO3>H2S
(C)H2SO3>H2S>Br->I- (D)I->Br->H2S>H2SO3
9、NaH是一种白色的离子晶体,其中钠为+1价,NaH与水反应放出氢气,下列叙述中,正确的是
(A).NaH在水中显酸性 (B).NaH中氢离子的电子排布与氦相同
(C).NaH中氢离子半径比锂离子半径大 (D).NaH中氢离子可被还原成氢气
|
|
(B)MnO2+4HCl(浓) = MnCl2+Cl2+2H2O MnO2+4H++2Cl- = Mn2++Cl2+2H2O
(C)Ba(OH)2+H2SO4=BaSO4¯+2H2O Ba2++SO42-=BaSO4¯
(D)NaHS+HCl=NaCl+H2S S2-+2H+=H2S
8.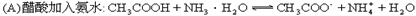 下列反应的离子方程式不正确的是:
下列反应的离子方程式不正确的是:
(B)铜片插入硝酸银溶液:Cu+Ag+=Cu2++Ag

(D)硫氰化钾溶液加入三氯化铁溶液:Fe3++SCN-=[Fe(SCN)]2+
7、在3BrF3+5H2O=HBrO3+Br2+9HF+O2↑中,5mol水能还原的BrF3的物质的量为: (A).1mol (B).4/3mol (C).2mol (D).3mol
6.剧毒物氰化钠(NaCN)存在如下反应:
2NaCN+O2+2NaOH+2H2O→2Na2CO3+2NH3有关叙述正确的是
(A).氧气是氧化剂 (B).水是还原剂
(C).氨是氧化产物 (D).碳酸钠是氧化产物
5.在一定条件下,氯气与碘单质以等物质的量进行反应,可得到一种红棕色液体ICl,ICl有很强的氧化性,ICl跟Zn、H2O反应的化学方程式如下
2ICl+2Zn=ZnCl2+Znl2 ICl+H2O=HCl+HIO
下列关于ICl性质的叙述正确的是
(A).ZnCl2是氧化产物,又是还原产物
(B).ZnI2是氧化产物,又是还原产物
(C).ICl跟H2O的反应,ICl是氧化剂,H2O是还原剂
(D).ICl跟H2O的反应,是自身氧化还原反应
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com