
题目列表(包括答案和解析)
11.下列各组中两种物质在溶液中的反应,可用同一离子方程式表示的是 ( )
A. Cu(OH)2+HCl;Cu(OH)2+CH3COOH B. Na2CO3+H2SO4;Na2CO3+HCl
C. Na2CO3+NaOH;Ca(HCO3)2+NaOH D. BaCl2+H2SO4;Ba(OH)2+H2SO4
10.下列离子在溶液中能大量共存,加入OH-能产生白色沉淀的是 ( )
A. Na+、Ca2+、SO42-、Cl- B. H+、Mg2+、CO32-、S2-
C. K+、Mg2+、SO42-、NO3- D. K+、Na+、NO3-、SO32-
9. 0.1molNa2SO4溶解在多少mol水中,才能使每100个水分子中含有一个Na+离子 ( )
A. 5mol B. 10mol C. 20mol D. 30mol
8.把各组中的气体通入溶液中,溶液的导电能力显著增强的是 ( )
A. CO2(g)通入NaOH溶液 B. CO2(g)通入石灰水
C. NH3(g)通入CH3COOH溶液 D. NH3(g)通入盐酸中
7.离子方程式H++OH-==H2O可表示的化学反应是 ( )
A. 盐酸和氢氧化钡的反应 B. 硝酸和氢氧化镁的反应
C. 硫酸和氢氧化钡的反应 D. 盐酸和氨水的反应
6.根据下列反应判断有关物质还原性由强到弱的顺序是 ( )
H2SO3+I2+H2O==2HI+H2SO4 2FeCl3+2HI==2FeCl2+2HCl+I2
3FeCl2+4HNO3==2FeCl3+NO↑+2H2O+Fe(NO3)3
A. H2SO3>I->Fe2+>NO B. I->Fe2+>H2SO3>NO
C. Fe2+>I->H2SO3>NO D. NO>Fe2+>H2SO3>I-
5. 某氧化剂中,起氧化作用的是X2O72-离子,在溶液中0.2mol该离子恰好能使0.6mol的SO32-离子完全氧化,则X2O72-离子还原后X的化合价为 ( )
A. +1 B. +2 C. +3 D. +4
4.用下列方法:①KMnO4受热分解 ②KClO3受热分解(用MnO2作催化剂)
③2H2O2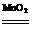 2H2O+O2↑ ④2Na2O2+2H2O==4NaOH+O2↑,若要制得相同质量的氧气,上述四种方法中所转移的电子数目之比是 ( )
2H2O+O2↑ ④2Na2O2+2H2O==4NaOH+O2↑,若要制得相同质量的氧气,上述四种方法中所转移的电子数目之比是 ( )
A. 3:2:1:4 B. 1:1:1:1 C. 1:2:1:2 D. 2:2:1:1
3.硫酸铵在强热条件下分解,生成氨、二氧化硫、氮气和水。反应中生成的氧化产物和还原产物的物质的量之比是 ( )
A. 1:3 B. 2:3 C. 1:1 D. 4:3
2.将4gNaOH溶解在10mL水中,再稀释为1L,从中取出10mL溶液的物质的量浓度是 ( )
A. 1mol/L B. 0.1mol/L C. 0.01mol/L D. 10mol/L
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com