
题目列表(包括答案和解析)
6.下列有关环境、健康、发展的叙述中,不正确的是
A.可吸入颗粒(例如硅酸盐粉尘)形成气溶胶,对人类健康危害极大
B.开发利用绿色能源(例如太阳能)替代化石燃料是人类可持续发展的必由之路
C.装修材料中的苯主要来自胶、漆等,是强致癌物
D.氟氯烃含量是空气质量报告的主要项目之一
24.(8分)向30.0mL硫酸铜溶液中加入过量铝粉,待充分反应后,再向其中加入2.00mol·L-1烧碱溶液至沉淀不再减少,消耗烧碱溶液210mL,且收集到气体0.672L(标准状况)。据此计算:
(1)加入铝粉的质量。
23.(10分)已知X、Y、Z、W是短周期中四种非金属元素,它们的原子序数依次增大。X
元素原子形成的离子就是一个质子,Z、W在元素周期表中处于相邻的位置,它们的单
质在常温下均为无色气体,Y原子的最外层电子数是内层电子数的2倍。
(1)写出元素符号:X ;Y ;Z ;W 。
(2)X单质和Z单质在一定条件下反应生成化合物E,该反应的化学方程式为(注明反
应条件) ;E分子的空间构成型为 ,
电子式为 。
(3)仅由X、Z、W三种元素组成的某种盐是一种速效肥,但长期施用会使土壤酸化,
有关的离子方程式为 。
(4)这四种元素可组成原子个数比为5∶1∶1∶3的化合物(按X、Y、Z、W的顺序),
该化合物的水溶液与足量浓NaOH溶液反应的离子方程式为 。
22. (8分)已知CH2
(8分)已知CH2 CH-CH CH2在不同条件下可与1molBr2发生反应,得到两种不同产物:
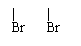 ①CH2
①CH2 CH-CH CH2+Br2
CH2 CH-CH-CH2

 ②CH2
②CH2 CH-CH CH2+Br2
CH2-CH CH-CH2
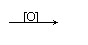 又知炔和烯均可被酸性KMnO4氧化成羧酸:
又知炔和烯均可被酸性KMnO4氧化成羧酸:
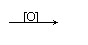 R-CH
R-CH CH-R′
R-COOH+R′-COOH
R-C≡C-R′ R-COOH+ R′-COOH
下图方格中每格均代表一种物质,从起始物A(C4H4,一种链烃)最终可得酯I(C6H8O4是具有六原子环的环状酯)。
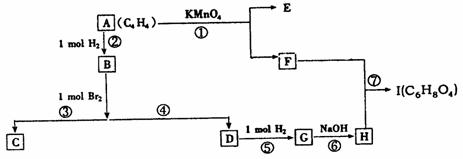
(1)写出下列物质的结构简式:E ,I 。
(2)以上各反应中属于取代反应的有 (填序号)。
(3)反应⑥的化学方程式为 。
21.(4分)将0.3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼
和液态水,放出649.5kJ热量,该反应的热化学方程式为 。
已知:H2O(1) H2O(g),△H=44kJ/mol,则11.2L(标准状况)乙硼烷完全燃烧生成
气态小时放出的热量是 kJ。
 19.(5分)检验右图装置的气密性,通常是将导管放入水中,①用手握住试管,观察到导管口有气泡冒出,②手离开试管后,导管中有一段水柱上升,说明装置不漏气。请回答:
19.(5分)检验右图装置的气密性,通常是将导管放入水中,①用手握住试管,观察到导管口有气泡冒出,②手离开试管后,导管中有一段水柱上升,说明装置不漏气。请回答:
(1)此法的原理是
。
(2)某同学操作时,只做了①没有做②,他即认为装置的气密性良好。你认为他的结论是否正确? (答“是”或“否”)。理由是
。
20.(11分)实验室用浓盐酸、二氧化锰共热制氯气,并用氯气和Ca(OH)2制取少量漂白粉。
现已知反应:2Cl2+2Ca(OH)2 Ca(ClO)2+CaCl2+2H2O,该反应是放热反应,温度稍
高即发生副反应:6Cl2+6Ca(OH)2 Ca(ClO3)2+5CaCl2+6H2O。
 现有3个同学分别设计的3套实验装置如下图:
现有3个同学分别设计的3套实验装置如下图:
(1)写出制取氯气的化学方程式 。
(2)请从以下几个方面对甲乙丙3套实验装置的优缺点作出评价,并将符合题目要求的
选项的序号填在表中空格中。
a.不容易控制反应速率;b.容易控制反应速率;c.有副反应发生;d.可防止副
反应发生;e.污染环境;f.可防止污染环境。
|
|
优 点 |
缺 点 |
|
甲装置 |
|
|
|
乙装置 |
|
|
|
丙装置 |
|
|
(3)上述装置中甲由A、B两部分组成,乙由C、D、E三部分组成,丙由F、G两部分组成,请从上述装置中选取合理的部分,组装一套较完整的实验装置,装置各部分
连接顺序是 (按气流流动的方向)。该组合中还缺少的
装置是 ,原因是 。
(4)实验室若用16mol/L的盐酸100mL与足量的二氧化锰反应,理论上最终生成的次氯酸钙的物质的量最多不超过 mol。
18.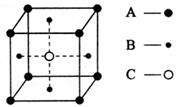 某物质的晶体中含有A、B、C三种元素,其排列
某物质的晶体中含有A、B、C三种元素,其排列
方式如图所示(其中前后两面面心中的B元素的
原子未能画出)。晶体中A、B、C的原子个数比
为 ( )
A.1∶3∶1 B.2∶3∶1 C.2∶2∶1 D.1∶3∶3
第Ⅰ卷选择题答案
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
|
|
|
|
|
|
|
|
|
|
|
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
|
|
|
|
|
|
|
|
|
|
|
|
|
第Ⅱ卷(非选择题 共46分)
17.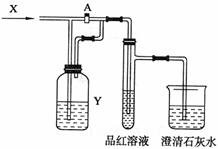 右图是一套检验气体性质的实验装置,向装置
右图是一套检验气体性质的实验装置,向装置
中缓慢通入气体X,若关闭活塞A,则品红溶
液无变化,而澄清石灰水变浑浊;若打开活塞
A,则品红溶液褪色。据此判断气体X和洗气
瓶内溶液Y分别可能是 ( )
|
|
A |
B |
C |
D |
|
X |
SO2 |
H2S |
CO2 |
Cl2 |
|
Y |
饱和NaHCO3溶液 |
浓硫酸 |
Na2SO3 |
NaHSO3溶液 |
16.HClO3是一种具有强氧化性的强酸,预计Cu和HClO3溶液反应的生成物不可能是( )
A.H2 B.Cl2 C.Cu(ClO3)2 D.CuCl2
15.向Cr2(SO4)3的水溶液中加入NaOH溶液,当pH=4.6时,开始出现Cr(OH)3沉淀,随着
pH的升高,沉淀增多,但当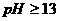 时,沉淀消失,出现亮绿色的亚铬酸根CrO2-。
时,沉淀消失,出现亮绿色的亚铬酸根CrO2-。

 其平衡关系如下:Cr3++3OH- Cr(OH)3 CrO2-+H++H2O
其平衡关系如下:Cr3++3OH- Cr(OH)3 CrO2-+H++H2O
(紫色) (灰绿色) (亮绿色)
向0.05mol/L的Cr2(SO4)3溶液50mL中加入1.0mol/L的NaOH溶液50mL,充分反应后,
溶液中可观察到的现象为 ( )
A.溶液为紫色 B.溶液中有灰绿色沉淀
C.溶液为亮绿色 D.无法判断
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com