
题目列表(包括答案和解析)
26. (共11分)
(共11分)
已知 ① RX+NaOH ROH+NaX
② 同一碳原子上有多个羟基不稳定且自动脱水,如
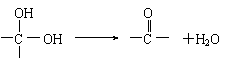
某碳氢化合物A(C9H8),分子有苯环和一个侧链,A能发生下列一系列反应:
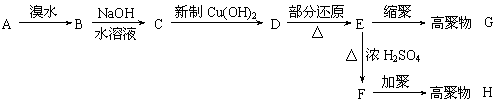
(1)写出下列物质的结构简式
A B
E F
G H
(2)E→F的反应类型
25.(共7分) 有机物中碳的价键结合是否得到饱和,通常用不饱和度表示,例如丙烷、丙烯、苯的不饱和度分别为0、1、4,则
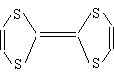
(1) 的化学式为 ,不饱和度为 。
(2)已知某烃有8个氢原子,不饱和度为5,其化学式是 ,
若此烃的碳原子都以单键结合,其结构可表示为 。
24.(共9分) 甲、乙、丙均为中学化学常见气体单质,A、B、C为常见的化合物。可供参考的信息有:
(Ⅰ)A和B都极易溶于水,用两根玻璃棒分别蘸A和B的浓溶液后相互靠近,会看到白烟。
(Ⅱ)甲与乙在一定条件下反应的有关数据为:
|
项目 |
甲 |
乙 |
A |
|
起始时 |
3mol·L-1 |
3mol·L-1 |
|
|
2s末 |
1.8mol·L-1 |
2.6mol·L-1 |
0.8mol·L-1 |
(Ⅲ)它们之间存在如下图所示的转化关系:
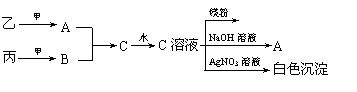
分析上述信息回答下列问题:
(1)丙的电子式为:
(2)用A、B、C的化学式填空:
①水溶液呈酸性的是 。
②固态时属于离子晶体的是 。
(3)甲与乙反应生成A的速率为:v(甲)= 。
(4)写出C与NaOH溶液反应生成A的离子方程式。
23.(共8分) 537℃,1.01×105Pa时,往容积可变的密闭容器中充入2molSO2,1molO2,此时容器的体积为200L。向容器中加入催化剂(固体)并保持恒温恒压,发生反应:
 2SO2(g)+O2(g) 2SO3(g)
2SO2(g)+O2(g) 2SO3(g)
达到平衡时,平衡气体中SO3的体积分数为0.91。
试回答下列问题:
(1)工业上二氧化硫的催化氧化采用常压而不采用高压的原因是:
。
(2)保持上述温度的压强不变,若向容器中只充入2mol SO3并加入固体催化剂,则平衡时,SO2的体积分数是 ,容器的体积为 L。
(3)温度仍保持537℃,容器体积保持200L不变(恒容)。充入amol SO2,bmol O2,并加入固体催化剂,反应达到平衡时,SO3的体积分数仍为0.91,体系压强为1.01×105Pa。若a:b=2:1,则a= 。
22.(共6分)在常温的条件下:
(1)设某pH值的硫酸溶液中水的电离度为α1,相同pH值的硫酸铝溶液中水的电离度为α2,那么α1与α2的数值相比较,α1 α2(填>,<,或=)。
(2)某硫酸和硫酸铝两溶液的pH值都是3,那么硫酸中水电离出的[H+]是硫酸铝溶液中水电离出的[H+]的 倍。
(3)若设某pH值的硫酸溶液中水电离出的[H+]=1.0×10-a mol/L,设相同pH值的硫酸铝溶液中水的电离[H+]=1.0×10-b mol/L(a、b都是小于14的正数),那么a和b之间满足的数量关系是(用一个等式和一个不等式表示) , 。
21.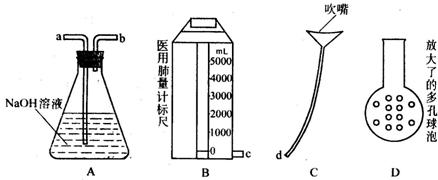 (共12分)某生物科技小组,为了测定人体呼出气体中CO2的体积分数,他们在肺量计上安装了足量的NaOH溶液吸收CO2的装置,然后通过实验测得NaOH溶液吸收CO2后的增重及肺量计的读数变化计算结果。所用仪器如下图所示,并回答有关问题:
(共12分)某生物科技小组,为了测定人体呼出气体中CO2的体积分数,他们在肺量计上安装了足量的NaOH溶液吸收CO2的装置,然后通过实验测得NaOH溶液吸收CO2后的增重及肺量计的读数变化计算结果。所用仪器如下图所示,并回答有关问题:
(1)根据题意,设计一个简单实验装置,其连接顺序(与气体方向一致),是 ;管口连接顺序是 。
(2)有人在装置A中将插入的导管下端改成具有多孔的球泡(如图中D所示),有利于提高实验的准确度,其理由是 ,
若不用多孔的球泡,在呼气时速度不能太急,这是因为
。
(3)如果被测者一次尽力呼出气体后的测试结果是:NaOH溶液质量增加了0.3g,此时肺量计的标尺在3600mL(已换算成标准状况下)处(实验前标尺为0),则呼出气体中CO2的体积分数为 ,此人的肺活量大致为 mL。
20.(共6分)摄影工艺中废定影液的pH<7,其中含有银的化合物,为了回收银进行如下操作:向盛有废定影液的烧杯中,加入少量稀NaOH溶液,再加入硫化钠溶液生成黑色沉淀,过滤,将固体移入坩埚中加碳酸钠和硼砂(催化剂)混合加热,放出二氧化碳和氧气。将残留的固体用水洗涤,即得到固体银,而洗涤液中主要含有硫化钠,试回答下列问题:
(1)开始时为何要向废液中加入少量NaOH溶液?理由:
。
(2)过程中的黑色沉淀物质是什么? 。
(3)写出加热时坩埚内发生反应的化学方程式 。
19.根据“绿色化学”的思想,某化学家设计了下列化学反应步骤:
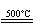
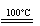
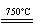
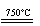 ①CaBr2+H2O CaO+2HBr ②2HBr+Hg
HgBr2+H2↑
①CaBr2+H2O CaO+2HBr ②2HBr+Hg
HgBr2+H2↑
③HgBr2+CaO HgO+CaBr2 ④2HgO 2Hg+O2↑该方案的目的是为了制备( )
A.HBr B.CaO C.H2 D.Hg
学校 班别 姓名 学号
第Ⅱ卷(非选择题,共79分)
18.据报道,某地一辆装载有砒霜的货车因故滑下河道,部分砒霜散落到河中。砒霜的主要成分是AS2O3剧毒,可用于制造杀虫剂和灭鼠剂等。AS2O3是两性偏酸性氧化物,其无色晶体在193℃升华,微溶于水生成H3ASO3;其对应的盐也有毒性,其中碱金属对应的盐易溶于水,其它金属对应的盐几乎不溶于水。根据以上信息,下列说法正确的是( )
A.AS2O3是砷的最高价含氧酸的酸酐
B.AS2O3的晶体为分子晶体
C.可向河水中投入纯碱,以消除对河水的污染
D.可向河水中撒入生石灰,以消除对河水的污染
17.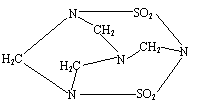 2002年9月14日南京汤山发生了一起震惊全国的特大投毒案,犯罪分子在食品中投入了毒鼠剂--毒鼠强,导致200多人中毒,42人抢救无效死亡;已知毒鼠强的结构简式如右图,有关毒鼠强(化学名:四亚甲基二砜四氨)的下列相关说法正确的是( )
2002年9月14日南京汤山发生了一起震惊全国的特大投毒案,犯罪分子在食品中投入了毒鼠剂--毒鼠强,导致200多人中毒,42人抢救无效死亡;已知毒鼠强的结构简式如右图,有关毒鼠强(化学名:四亚甲基二砜四氨)的下列相关说法正确的是( )
A.毒鼠强属于无机物 B.毒鼠强属于烃
C.四个氮原子构成正四面体 D.毒鼠强的分子式为C4H8N4S2O4
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com