
题目列表(包括答案和解析)
37、有 a、b、c、d 四种一元酸的溶液,通过如下实验:(1)物质的量深度相同的a、c溶液分别滴加甲基橙溶液,a溶液变黄色,c溶液不变色; (2)物质的量浓度相同的b、c的钠盐相比较。b的钠盐溶液pH值小于c的钠盐溶液pH值;
(3)a酸跟d的钠盐反应生成d 酸和a的钠盐。据此确定四种酸的酸性强弱的顺序是________________________________。
36、在25℃时,有pH值为x的盐酸和pH值为y的NaOH溶液,取VxL该盐酸同该NaOH溶液中和,需VyLNaOH溶液,问:
(1)若x+y=14时,则Vx/Vy=_________(填数值);
(2)若x+y=13时,则Vx/Vy=_________(填数值);
(3)若x+y>14时,则Vx/Vy=_________(填表达式),且Vx_____Vy(填>、<或=); (题中的x≤6,y≥8。)
35、与[H+][OH-]=K=1.0×10-22类似,FeS饱和溶液中[Fe2+][S2-]=Ksp,已知某温度下Ksp=6.25×10-18。
(1)饱和FeS溶液的物质的量浓度为______________;
(2)又知H2S饱和溶液中,[H+]2[S2-]=K=1.0×10-22,现将适量FeS投入其饱和溶液中,要使溶液里[Fe2+]达到1mol/L,则应将溶液的pH值调节为______________。
34、已知百里酚酞的变色范围是9.4-10.2。相同物质的量浓度的三种稀溶液: NaH2PO4的pH=4.7;Na2HPO4的pH=10;Na3PO4的pH=12。今有0.5g某种磷酸的钠盐水合物溶于50mL0.1mol/L的H2SO4溶液中,稀释至100mL。取出1/5该溶液(以百里酚酞作指示剂)需0.1mol/L的NaOH溶液26.4mL中和,则钠盐水合物的化学式为_____________。
33、将pH值为6的盐酸与pH值为4的盐酸等体积混合后,溶液中的氢氧根离子的物质的量浓度约是__________________。
32、25℃时,将某强酸和某强碱溶液按1:10的体积比混合后溶液恰好呈中性,则混合前此强酸与强碱溶液的pH值之和是_________
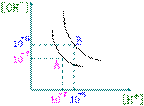
31、设水的电离平衡曲线如右下图所示。
(1)若以A点表示25℃时水在电离平衡时的离子浓度,当温度上升到100℃时,水的电离平衡状态到B点,则此时水的离子积从_________增加到_________;
 (2)将pH=8的Ba(OH)2溶液与
(2)将pH=8的Ba(OH)2溶液与
pH=5时的盐酸混合,并保持100℃的恒
温,欲使混合溶液pH=7,则Ba(OH)2与
盐酸的体积比为__________;
(3)已知AnBm的离子积=[Am+]n[Bn-]m式中的[Am+]n和[Bn-]m表示
离子的物质的量浓度。在某温度下,Ca(OH)2的溶解为0.74g,其饱和溶液密度设为1g/cm3,其离子积为____________;
(4)若在室温下平均每n个水分子只有一个水分子发生电离,则n值是 ____________;室温时10mL水中含有氢氧根离子约有___________个;
(5)常温时0.1mol/LHNO3和0.01mol/LHAc中水的电离度的关系是_____(填>、<、=等符号);
(6)常温时pH值相同的HNO3和HAc中水的电离度的关系是_____;
(7)常温时0.3mol/L的H2SO4和0.6mol/L的NaOH中水的电离度的关系是____;
(8)pH=10的NaOH溶液与pH=10的NaCN溶液中水的电离度之比是_____;
(9)pH=4的HCl溶液与pH=4的NH4I溶液中水的电离度之比是______;
(10)pH=6的HCl溶液和pH=6的NH4Cl溶液,其中水电离出的[H+]分别为xmol/L和 ymol/L,则x/y的比值为__________。
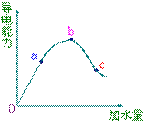
30、在一定温度下,冰醋酸加不稀释过程中,溶液的导电能力如右下图所示,
 请回答:
请回答:
(1)“O”点导电能力为0的理由是
________________________________;
(2)a、b、c三点溶液pH值由小到大
的顺序为_______________________;
(3)a、b、c三点中电离度最大的是
___________;
(4)若使C点溶液中[Ac-]增大,溶液的pH值也增大,可采取的措施是 ①_______________;②________________;③_________________。
0.1mol/L由第3周期某元素形成的某
酸溶液25mL。加入酸溶液的体积V和
安培计的读数的坐标图如图(b)
(1)此酸的化学式为_________;
(2)处于C点时,溶液中导电的阳离子主要是____________;
(3)处于F点时,溶液中导电的阴离子主要是___________;
(4)烧杯中刚加入酸时,观察到的现象是____________________;
(5)上图(b)中,从A→E电流强度I变小的主要原因是______________________________。
29、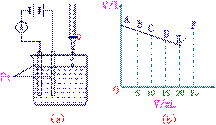 有一实验如右下图所示,将
有一实验如右下图所示,将
30mL 0.1mol/LBa(OH)2溶液置于烧
杯中,然后边搅拌边慢慢加入
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com