
题目列表(包括答案和解析)
3、甲、乙两学生用加热氯酸钾的方法制取氧气。甲取了一定量的氯酸钾和0.1gMnO2,经混合后装入试管内加热,待收集到所需氧气时,停止加热。试管冷却后,乙称得甲留下的反应混合物质量为4.04g,将它继续加热直至氯酸钾完全分解,收到氧气672mL(标准状况)。甲实验时氯酸钾分解的百分_____。
2、现有一份CuO和Cu2O混合物,用H2还原法测定其中CuO的质量x(g)。实验中可能测定如下数据:
w-混合物的质量(g),
wH2O-生成水的质量(g),
wCu-生成Cu的质量(g),
VH2-消耗的H2在标准状况下的体积(L)。
(已知摩尔质量:Cu-64g/mol、CuO-80g/mol、Cu2O-144g/mol、H2O-18g/mol)
(1)为了计算x,至少需要测定上述四个数据中的_____,这几个数据的组合共有_____种,请将这些组合一一填入下表空格中。
说明:①选用w、wH2O、wCu、VH2表示,不必列出具体计算式。
②每个空格中填一种组合,有几种组合就填几种,不必填满。
(2)上述组合中选一个含w的求x的计算式x=_____。
1、H2和O2的混合气体,在120℃和一定压强下体积为aL,点燃后发生反应。待气体恢复至原来温度和压强时,测得体积为bL。则原混合气体中H2和O2的体积分别是_____或_____。
35、(1)过滤,除去污染 (2)往滤液中加入过量铁粉,使Ag+还原为单质银
(3)过滤,将Ag和过量铁从滤液中分离出来
(4)将Ag和铁粉混合物同稀H2SO4处理,使Fe合理化为FeSO4与Ag分离
(5)过滤,分离出银
(6)将(3)(4)步骤滤液合并蒸发,命名FeSO4从溶液中结晶析出
(7)过滤,得FeSO4晶体。
33、(1)Al(OH)3 FeCl3 BaSO4
(2)4Fe(OH)2 + O2 + 2H2O == 4Fe(OH)3
(3)MgCl2
(4)取混合粉末的溶液少许,滴加AgNO3溶液,若有白色沉淀产生,证明有MgCl2存在,若无沉淀,证明无MgCl2。

32、(1)Mg3N2 MgO NH4Cl MgCl2 Mg(OH)2
(2)1:2 (3)Mg3N2 + 8HCl == 2NH4Cl。
30、Na2CO3 KNO3、KCl、NaCl

29、(1)③过滤 ④蒸发 (2)B (3)滤液浑浊 (4)液体飞溅
(5)K2CO3、KCl、K2SO4。
28、(1)大硬质试管、铁架台(附铁夹、酒精灯、单孔胶塞和玻璃导管)
(2)碱石灰,既除去水气也除去CO2
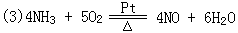
(4)铁架台、分液漏斗、平底烧瓶(或锥形瓶) 胶塞、导管、2Na2O2 +2H2O == 4NaOH + O2↑
5)颜色变浅,因为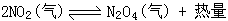 ,是放热反应,降低温度时平衡向正方向移动,红棕色的NO2部分转化为无色的N2O4,故颜色变浅。
,是放热反应,降低温度时平衡向正方向移动,红棕色的NO2部分转化为无色的N2O4,故颜色变浅。
27、(1)稀盐酸 CaCO3 Na2O2
(2)①CaCO3 + 2HCl == CaCl2 + H2O + CO2↑ ②2Na2O2 + 2CO2 == 2Na2CO3 + O2↑ ③2Na2O2 + 2H2O == 4NaOH + O2↑ ④CxHy + (x+y/4)O2 == xCO2 + y/2H2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com