
题目列表(包括答案和解析)
22、将一铜片投入到盛有浓HNO3的烧杯中充分反应,将产生的气体全部收集到一容器中。反应完毕后,把溶液倒入蒸发皿中小心蒸干,然后把固体物质全部移入试管内,加热使之完全分解,产生的气体也一并收集到前一容器中。最后将该容器倒立在盛水的水槽内,待反应完毕,测得容器内还余下无色气体0.448L(标准状况),则参加反应的铜的质量为_____克。
21、某化肥厂用NH3制HNO3,再进一步制NH4NO3。已知:由NH3制HNO3时的产率为88%;由NH3与HNO3反应制NH4NO3时的产率为98%。若用100吨NH4NO3时,用于制HNO3的氨为_____吨,可制出NH4NO3____吨。
20、硝酸工业尾气中的氮的氧化物(NO、NO2)是主要的大气污染之一。常用以下两种治理方法(已简化)。
(1)NaOH吸收法,反应原理如下:
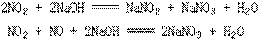
(2)氨催化还原法,反应原理是:
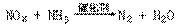
现有一定量的含NO2和NO的硝酸工业尾气(不含其它气体),若用过量的NaOH溶液吸收后,溶液中NaNO3与NaNO2的物质的量之比恰好与原尾气中NO和NO2的物质的量之比相等。
①若用NOx表示该尾气中氮的氧化物的平均组成,则x的值为_____。
②将1体积的该尾气用(2)的方法处理,至少消耗相同状况下的氨气_____ 体积。
③配平化学方程式:

19、将m克氨通过氨的催化氧化法完全制成硝酸,且将硝酸全部溶解在反应中生成的水里制成浓硝酸,其质量分数为_____。
18、已知三种硝酸盐受热分解如下:
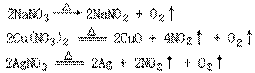
由上述三种盐的一种或多种组成的物质,受热分解时生成amL气体,被水充分吸收后剩余a/6mL气体(气体体积均在标准状况下测定)。符合这一条件的可能组合是:
(1)________,(2)________,(3)________。
17、已知NH3和Cl2在常温下混合可发生下列化学反应:
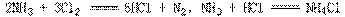
现有Cl2和NH3共aL。混合后充分反应,气体体积为bL。(设反应前后气体体积均在同温同压下测定)。请填表:
|
VNH3:VCl2 |
被氧化的NH3(L) |
|
(1)VNH3:VCl2≤2:3 |
|
|
(2) |
(a+b)/6 |
|
(3)VNH3:VCl2≥8:3 |
|
16、将VmLNO和NO2的混合气通过水吸收后,得到amL无色气体A。将此无色气体A与等体积O2混合,再通过水充分吸收后收集到bmL无色气体B。试回答:
(1)A气体是_____,B气体是_____;
(2)a与b的关系是_____。
(3)V值的取值范围为_____。
15、已知273℃,1.01×105Pa时,1mol气体所占体积为44.8L,现将此条件下V1LSO2和O2的混合气体通过装有催化剂的反应器,充分反应后(假设反应完全)气体的体积为V2L,所得气体用含amolNaOH溶液吸收,恰好完全反应,当产物分别为下列三种情况时,计算并推导a的表达式(用V1、V2表示)。
(1)产物为Na2SO4时,则a=_____,
(2)产物为Na2SO4和Na2SO3时,则a=_____,
(3)产物为Na2SO4和NaHSO3时,则a=_____。
14、用黄铁矿可以制取硫酸,再用硫酸制取化肥硫酸铵。燃烧含FeS2为80%的黄铁矿75吨,生产出79.2吨硫酸铵。若在制取硫酸铵时硫酸的利用率为90%,则用黄铁矿制取硫酸时损失率为_____。
13、为检验久存的一瓶a2SO3是否变质及变质的程度,取干燥试样ag,用适量蒸馏水配成溶液后,加入足量Ba(NO3)2溶液使其全部沉淀,过滤、干燥、称量得沉淀共bg。
(1)试根据试样是否变质及变质情况,求出a与b之间的数量关系。
①若Na2SO3没有变质,则a与b的关系_____;
②若Na2SO3已完全变质,则a与b的关系_____;
③若Na2SO3部分变质,则a与b的关系_____。
(2)若取试样a=10g,假定Na2SO3已有50%(指物质的量)变质,则b值为 _____克?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com