
题目列表(包括答案和解析)
24.化学电池在通讯、交通及日常生活中有着广泛的应用,目前常用的镍(Ni)镉(Cd)电池,其电池总反应可以表示为:

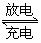

(1)下列有关镍镉电池总反应的说法中,正确的是________(填序号);
①以上反应是可逆反应 ②以上反应不是可逆反应
③充电时化学能转变为电能 ④放电时化学能转变为电能
(2)已知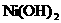 和
和 均难溶于水.有资料表明,一节废镍镉电池可以使一平方米面积的耕地失去使用价值,在酸性土壤中这种污染尤为严重.这是因为____________________ ;
均难溶于水.有资料表明,一节废镍镉电池可以使一平方米面积的耕地失去使用价值,在酸性土壤中这种污染尤为严重.这是因为____________________ ;
(3)另一种常用的电池是锂电池(锂是一种碱金属元素,其相对原子质量为7),由于它的比容量(单位质量电极材料所能转换的电量)特别大而广泛应用于心脏起搏器,一般使用时间可长达十年.电池总反应可表示为: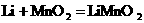 .试回答:
.试回答:
①锂电池比容量特别大的原因是_____________________________________________ ;
②锂电池中的电解质溶液需用非水溶剂配制,为什么这种电池不能使用电解质的水溶液?请用化学方程式表示其原因_______________________________________.
23.在一定条件下,二氧化碳和氧气发生如下反应:
 2SO2(g)+ O2
(g) 2SO3(g)
+ Q (Q>0)
2SO2(g)+ O2
(g) 2SO3(g)
+ Q (Q>0)
(1)写出该反应的化学平衡常数表达式 K=
(2)降低温度,该反应K值 ,二氧化碳转化率 ,化学反应速度 (以上均填增大、减小或不变)
(3)600℃时,在一密闭容器中,将二氧化碳和氧气混合,反应过程中SO2、O2、SO3物质的量变化如图,反应处于平衡状态的时间是 。
(4)据图判断,反应进行至20min时,曲线发生变化的原因是
(用文字表达)
10min到15min的曲线变化的原因可能是 (填写编号)。
a.加了催化剂 b.缩小容器体积
c.降低温度 d.增加SO3的物质的量
22.将镁在空气中燃烧的全部产物溶解在80毫升浓度为2.375摩/升盐酸中,以40毫升0.9摩/升氢氧化钠溶液中和多余盐酸。然后再加入过量的氢氧化钠溶液,把生成的NH3用盐酸全部吸收,经测定氨为0.646克,则燃烧掉镁的质量为: ( )
A. 3.46g B. 2.59g C. 1.392g D. 1.68g
第 Ⅱ 卷 (非选择题 共84分)
21.草酸是二元弱酸,草酸氢钾溶液呈酸性。在0.1mol/LKHC2O4溶液中,下列关系正确的是( )
A c(K+)+c(H+)=c(HC2O4-)+c(OH-)+c(C2O42-)
B c(HC2O4-)+c(C2O42-)=0.1mol·L-1
C c(C2O42-)>c(H2C2O4)
D c(K+)=c(H2C2O4)+c(HC2O4-)+c(C2O42-)
20.某种一元酸(HA)溶液中,加入一定量的一种强碱(MOH)溶液后恰好完全反应,则有关反应后溶液的判断中,一定正确的是 ( )
A.c(A-)≤c(M+) B. c(A-)≥c(M+)
C.若MA不水解,则c(OH-) <c(A-) D.若MA不水解,则c(OH-) >c(A-)
19.同浓度,同体积的下列物质后者滴入前者的过程中,溶液的导电性变化不大 ( )
A.氨水,盐酸 B.硫酸镁,氢氧化钠
C.氢氧化钡,盐酸 D.氢氧化钡,硫酸铜
18.阿伏加德罗常数约为6.02×1023mol-1。下列叙述中正确的是 ( )
A.标准状况下,2.24L苯中约含有3.612×102:个碳原子
B.常温常压下,氧气和臭氧的混合物16s中约含有6.0Q×1O23个氧原子
C.25℃时,1L pH=13的氢氧化钠溶液中约含有6.02×l023个氢氧根离子
D.0.5mol CH4中约含有3.01×1024个电子
17.已知0.1mol/L HCN溶液的PH=4,0.1mol/L NaCN 溶液的PH=12,先将0.2mol/L HCN溶液和0.1mol/L NaOH溶液等体积混合后,溶液中各离子浓度间的关系正确的是 ( )
A. B.
B.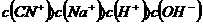
C.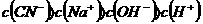 D.
D.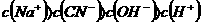
16.在复印室工作时会闻到一股特殊的气味,离复印机越近,该气味越浓.若用润湿的KI淀粉试纸接近该气体,则试纸会变蓝,则该物质的化学式是 ( )
A. B.
B. C.
C.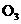 D.
D.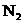
15.一种化学冰袋中含有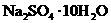 (96g)、
(96g)、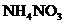 (50g)、
(50g)、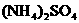 (40g)、
(40g)、 (40g).将
(40g).将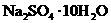 和其他3种盐分盛于2只塑料袋中,用时使它们混合并用手搓揉就可致冷,致冷效果能维持2h-3h.以下关于其致冷原因的猜测肯定错误的是
( )
和其他3种盐分盛于2只塑料袋中,用时使它们混合并用手搓揉就可致冷,致冷效果能维持2h-3h.以下关于其致冷原因的猜测肯定错误的是
( )
A.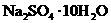 脱水是吸热过程
脱水是吸热过程
B.较长时间致冷是由于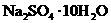 脱水是较慢的过程
脱水是较慢的过程
C.铵盐在该条件下发生复分解反应是吸热反应
D.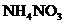 溶于结晶水中会吸收热量
溶于结晶水中会吸收热量
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com