
题目列表(包括答案和解析)
3.下列叙述正确的是
A.发生化学反应时失去电子越多的金属原子,还原能力越强
B.金属阳离子被还原后,一定得到该元素的单质
C. 核外电子总数相同的原子,一定是同种元素的原子
D.能与酸反应的氧化物,一定是碱性氧化物
2.下列说法中正确的是( )
A.冰、水和水蒸气中都存在氢键
B.除稀有气体外的非金属元素都能生成不同价态的含氧酸
C. 金属离子和自由电子间通过金属键形成的晶体是金属晶体
D.CO2与SiO2都是分子晶体,所以它们有接近的熔、沸点
1.下列叙述中,不正确的是
①原子晶体中只含有极性键 ②金属在常温时都以晶体形式存在
③离子晶体一定含离子键,也可能有共价键 ④分子晶体中一定有分子间作用力,有的还可能有氢键
A.①④ B.②③ C.①② D.①③
20.(9分)在100mL 36.5%的浓盐酸(密度为1.18g/cm3)中加入多少mL 2mol/L的稀盐酸(密度为1.08g/cm3),才能配成6mol/L的盐酸(密度为1.10g/cm3)。(要求先计算再简答配制的步骤)
19.(14分)某校化学兴趣小组的同学欲测定某种品牌精中食盐的含量。
下面是该小组所做的有关实验步骤:
①称取某牌袋装味精样品10.0g放入烧杯中,并加适量蒸馏水溶解;
② ;
③ ;
④用蒸馏水洗涤沉淀2-3次;
⑤将沉淀烘干、称量,测得固体质量4.90g
根据上述实验步骤回答下列问题:
(1)补齐所缺少的实验步骤:② ③
(2)实验步骤③所用的玻璃仪器有 ;
(3)检验沉淀是否洗净的方法是: ;
(4)烘干沉淀应采取的方法是 。
(5)若味精标签上标注:“谷氨酸钠含量≥80.0%,NaCl含量≤20.0%,则此样品是否合格?
(填“合格”,“不合格”)
18.(12分)、近年来发现许多生物体组织中存在的少量NO有扩张血管、免疫、增强记忆的功能,成为当前生命科学的研究热点。请回答问题:
(1)NO在大气层中可发生反应:NO+O2  NO2 +
O,NO2 + O
NO2 +
O,NO2 + O NO + O2 ,从反应最终结果看,NO是一种 (填序号)。
NO + O2 ,从反应最终结果看,NO是一种 (填序号)。
A.氧化剂 B.还原剂 C.还原产物 D.氧化产物 E.催化剂
(2)将NO转化为无毒气体,可选用NH3在400℃左右并有催化剂存在下把NO还原为氮气和水,写出该反应的化学方程式。相同条件下能否用天然气代替NH3来处理硝酸尾气 (NOx)。如果可能,请写出能发生反应的化学方程式,并指出是否具有实际意义。
(3)在含Cu+的酶的活化中心中,亚硝酸根离子可转化为NO,写出Cu+与亚硝酸根离子在酸性水溶液中反应的离子方程式 。
(4)把NO气体压缩到1.01×107Pa,再加热到一定温度,发现气体的压力迅速下降,压力降至略小于原压力的2/3,然后压力就不再改变,已知其中一种产物为N2O,则上述变化的化学方程式为 ; 。所得混合气体的平均摩尔质量M的取值范围应该是 。
17.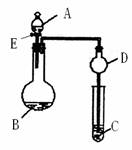 (11分)用如图所示装置(夹持仪器省略)进行实验,将液体A逐滴加入到固体B中,回答下列问题:
(11分)用如图所示装置(夹持仪器省略)进行实验,将液体A逐滴加入到固体B中,回答下列问题:
(1)图中D装置在实验中的作用是 .
(2)若 A为30%H2O2溶液,B为MnO2 ,C盛有氢硫酸
(H2S)饱和溶液,旋开E后,C中的现象为 ,
C中发生反应的化学方程式为 。
(3)若A为浓盐酸,B为KMnO4,C中盛有KI淀粉溶液,
旋开E后,C中的现象是 ;继续通气体于C中,足够长的时间后,发现C中溶液的颜色消失,这是因为在溶液中I2能被Cl2氧化为HIO3,写出该反应的化学方程式 。
(4)若A为浓氨水,B为生石灰,C中盛有AlCl3溶液,旋开E,足够长的时间后,C中的现象是 ,C中发生反应的离子方程式为 。
(5)该题图示装置有多种用途,请举一例(除题中之外)填空:A为 ,B为 ;C中盛 ,其目的为 。
16.在一定条件下,CO和CH4燃烧的热化学方程式分别为 ( )
2CO(g)+O2(g)==2CO2(g) ; △H=-566kJ·mol-1
CH4(g)+2 O2(g)==CO2(g)+2H2O(1) ; △H=-890kJ·mol-1
由等物质的量的CO和CH4的混合气体共4mol,在上述条件下完全燃烧时释放的热量为
A.1173kJ B.1456kJ C.2346kJ D.1780kJ
第Ⅱ卷(共46分)
15.若以ω1和ω2分别表示浓度为a mol·L-1和b mol·L-1氨水的质量分数,且知2 a = b,则下列推断正确的是(氨水的密度比纯水的小)( )
A.2ω1 > ω2 B. 2ω2 =ω1 C.ω2 > 2ω1 D.ω1 < ω2 < 2ω1
14.将某温度下的KNO3溶液190g蒸发掉10g水恢复到原温度,或向其中加入5gKNO3固体,可使溶液达到饱和,则该温度下KNO3溶解度是 ( )
A.1g B.50g C.90g D.100g
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com