
题目列表(包括答案和解析)
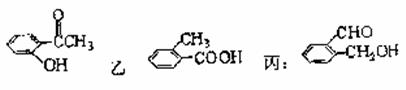
20.(4分)某含氧有机化合物可以作为无铅汽油的抗爆震剂,它的分子量为88.0,含C的质量分数为68.2%,含H的质量分数为13.6%,红外光谱和核磁共振氢谱显示该分子中有4个甲基。请写出其结构简式。
_________________________________________________________________________。
19.(14分)长期存放的亚硫酸钠可能会被部分氧化,现通过实验来测定某无水亚硫酸钠试剂的纯度。实验步骤如下:
① 称量a g样品,置于烧杯中。
② 加入适量蒸馏水,使样品溶解。
③ 加入稀盐酸,使溶液呈强酸性,再加过量的BaCl2溶液
④ 过滤,用蒸馏水洗涤沉淀。
⑤ 加热干燥沉淀物。
⑥ 将沉淀物冷却至室温后,称量。
⑦ 重复⑤、⑥操作直到合格,最后得到b g固体。
回答下面问题:
(1)本实验中是否能用Ba(NO3)2代替BaCl2?其理由是:
_________________________________________________________________________________________________________________________________________________________。
(2)步骤③中加盐酸使溶液呈强酸性的目的是:
________________________________________________________________________________________________________________________________________________________。
(3)步骤⑦的“合格”标准是:_____________________________________________ .
(4)实验测得样品中无水亚硫酸钠的质量分数是:
__________________________________________________________________________。
(列出算式,不需化简)
18.(7)甲、乙、丙、丁分别是盐酸、碳酸钠、氯化钙、硝酸银4种溶液中的一种。将它们两两混合后,观察到的现象是:①甲与乙或丙混合都产生沉淀;②丙与乙或丁混合也产生沉淀;③丁与乙混合产生无色气体。回答下面问题:
(1)写出丁与乙反应的离子方程式:________________________________________ .
(2)这四种溶液分别是甲:_________ 、乙:_________、丙:_______、丁:_______。
17.(5分)用pH试纸测定溶液的pH,正确操作是:
____________________________________________________________________________________________________________________________________-。
16.(12分)室温下,单质A、B、C分别为固体、黄绿色气体、无色气体,在合适反应条件下,它们可以按下面框图进行反应。又知E溶液是无色的,请回答:
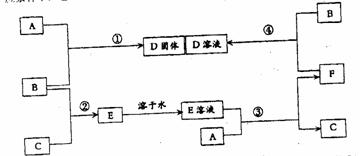
(1)A是_________________、B是_____________、C是_______________(请填化学式)
(2)反应①的化学方程式为:_______________________。
(3)反应③的化学方程式为:_______________________。
(4)反应④的化学方程式为: ________________________。
15.(10分)化合物BrFx与水按物质的量之比3:5发生反应,其产物为溴酸、氢氟酸、单质溴和氧气。
(1)BrFx中,x=______________________。
(2)该反应的化学方程式是:______________________________________。
(3)此反应中的氧化剂和还原剂各是什么?______________________________。
14.(8分)填写下列空白:
(1)写出表示含有8个质子、10个中子的原子的化学符号:__________________。
(2)周期表中位于第8纵行的铁元素属于第______________族。
(3)周期表中最活泼的非金属元素位于第_________纵行。
(4)所含元素超过18种的周期是第_________、__________周期
13.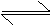 反应L(固)+aG(气)
bR(气)达到平衡时,温度和压强对该反应的影响如下图所示,图中:压强p1>p2,X轴表示温度,Y轴表示平衡混合气中G的体积分数。据此可判断:
反应L(固)+aG(气)
bR(气)达到平衡时,温度和压强对该反应的影响如下图所示,图中:压强p1>p2,X轴表示温度,Y轴表示平衡混合气中G的体积分数。据此可判断:
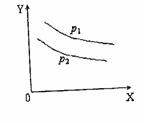 A.上述反应是放热反应
B.上述反应是吸热反应
A.上述反应是放热反应
B.上述反应是吸热反应
C.a>b D.a<b
第II卷(非选择题 共104分)
12.将一定质量的Mg 、Zn、Al混合物与足量稀H2SO4反应,生成H22.8L(标准状况),原混合物的质量可能是( )
A.2g B.4g C.8g D.10g
11.下列反应的离子方程式正确的是( )
A.硫酸铝溶液和小苏打溶液反应 Al3++3HCO3-==3CO2↑+Al(OH)3↓
B.向Ca(ClO)2溶液中通入二氧化硫 Ca2++2ClO-+SO2+H2O==CaSO3↓+2HClO
C.硫化亚铁中加入盐酸 S2-+2H+== H2S↑
D.钠和冷水反应 Na+2H2O==Na++H2↑+2OH-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com