
题目列表(包括答案和解析)
3.在FeCl3,CuCl2,FeCl2混合溶液中,Fe3+、Cu2+和Fe2+的物质的量之比为3∶2∶1,现加入适量铁粉,使溶液中三种离子物质的量浓度之比变为1∶2∶4,则参加反应的铁粉与原溶液Fe3+的物质的量之比为( )。
A.2∶l B.1∶2 C. 1∶3 D.1∶4
2.室温下某溶液中由水电离出的[OH-]=10-5mol•L-1,则其溶质可能是( )。
A.Na2C03 B.H2SO4 C.NaOH D.CH3COOH
1.中国科学家在世界上首次发现铂的一种新原子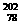 Pt,下列说法不正确的是( )。
Pt,下列说法不正确的是( )。
A.相对原子质量202 B.质量数202 C.原子序数78 D.核内有124个中子
13. SO2是大气污染物之一,为粗略地测定周围环境中SO2的含量,某学生课外活动小组设计了如下实验装置:
SO2是大气污染物之一,为粗略地测定周围环境中SO2的含量,某学生课外活动小组设计了如下实验装置:
(1)检查该装置的气密性时,先在
试管中装入适量的水(保证玻璃导管
的下端浸没在水中),然后_________
(填写操作方法)时,将会看到____
_________________(填写实验现象),
则证明该装置的气密性良好。
(2)向试管中加入0.0005 mol/L的碘水1.0 mL,用适量的蒸馏水稀释后再加入2~3滴淀粉溶液,配制成溶液A。测定指定地点的空气中SO2的含量时,推拉注射器的活塞反复抽气,A溶液由_________色变为_________色时反应恰好完全进行,此时停止抽气,该反应的化学方程式为_____________________________________________。
(3)我国环境空气质量标准中对每次空气质量测定中SO2的最高浓度限值如下表:
|
浓度限值/mg.m-3 |
||
|
一级标准 |
二级标准 |
三级标准 |
|
0.15 |
0.50 |
0.70 |
该学生课外活动小组分成第一小组和第二小组,使用相同的实验装置和溶液A,在同一地点、同时测量空气中SO2的含量。当反应恰好完全进行,记录抽气次数如下(假设每次抽气500 mL)。请将下表填写完整(计算时保留2位有效数字):
|
分组 |
第一小组 |
第二小组 |
|
抽气次数 |
120 |
140 |
|
SO2含量/mg.m-3 |
|
|
判断该地点的空气中SO2的含量属于________(填数字)级标准,_______(“第一”或“第二”)小组的测定结果正确,另一个小组实验结果产生较大偏差的原因是(2个小组所用装置和药品均无问题)__________________________________________________。
12.X、Y、Z是主族元素的单质,K、H是化合物,它们有如下反应(式中各物质的化学计量数和反应条件略)
1 X+K → H+Y ; 2 X+Z → H ;3 Y+Z → K
(1)若X和Y的组成元素不在同一族,请写出符合1式的3个不同的化学方程式(配平)。(3个式子中的3种X和3种Y分别由不同族的元素组成):_________________________________、________________________________________、
______________________________________。
(2)今有某化合物W,它跟化合物K或CO2反应,都能生成单质Y。符合反应化学方程式1、2、3的单质X是_______________,单质Y是________________,单质Z是____________,化合物W是_______________________(均写化学式)。
11.松油醇是一种调香香精,它是α、β、γ 三种同分异构体组成的混合物,可由松节油分馏产品A(下式中的18是为区分两个羟基而人为加上去的)经下列反应制得:
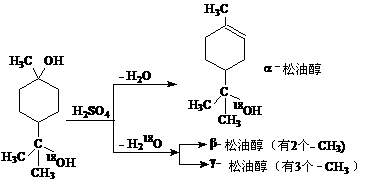
试回答:
(1)α-松油醇的分子式_____________________。
(2)α-松油醇所属有机物类别是____________(多选扣分) a.醇 b.酚 c.饱和一元醇
(3)α-松油醇能发生的反应类型是___________(多选扣分)a.加成 b.水解 c.氧化
(4)在许多香料中松油醇还有少量以酯的形式出现,写出RCOOH和α-松油醇反应的化学方程式___________________________________。
(5)写出结构简式:β-松油醇____________________、γ-松油醇______________________________。
10. 某种豆类作物中所含的天然蛋白质在酶的作用下发生水解,可得到甲、乙2种氨基酸。已知甲的结构简式为
乙的分子式为 C4H7O4N
某种豆类作物中所含的天然蛋白质在酶的作用下发生水解,可得到甲、乙2种氨基酸。已知甲的结构简式为
乙的分子式为 C4H7O4N
(1)由甲形成的三肽中氨基、羟基的数目依次为___________、___________。
 (2)若乙不能发生银镜反应,其分子中没有甲基,则乙的结构简式为__________________。
(2)若乙不能发生银镜反应,其分子中没有甲基,则乙的结构简式为__________________。
(3)乙分子中的 和 发生分子内缩合反应脱去一分子水,所形成的含有四元环结构的化合物的结构简式为_________________________________。
9. 如图所示,温度不变,将某容器分隔为A、B两部分,A容器固定不变,B有可移动的活塞,现在A中充入2molSO2和1molO2,在B中充入2molSO3和1molN2,在相同条件下发生可逆反应:2SO2(g)+O2(g) 2SO3(g),根据下列要求填写空白:
如图所示,温度不变,将某容器分隔为A、B两部分,A容器固定不变,B有可移动的活塞,现在A中充入2molSO2和1molO2,在B中充入2molSO3和1molN2,在相同条件下发生可逆反应:2SO2(g)+O2(g) 2SO3(g),根据下列要求填写空白:
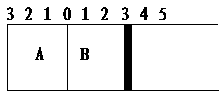 (1)固定活塞位置有3处不动,达到平衡后,
(1)固定活塞位置有3处不动,达到平衡后,
设A中压强为PA,B中压强为PB,则PA与PB
的压强是PA ________ PB(填“<”、“>”、“=”)。
(2)若要使A中与B中平衡状态相同,可移动
活塞的位置应在________处。
(3)若活塞右移到5处,达到平衡后,B中SO3为x mol,A中SO3为y mol,则x和y的关系__________(填“<”、“>”、“=”),理由是____________________________________。
8.已知A、B、C、D、E是核电荷数依次增大的五种短周期元素,原子半径按D、E、B、C、A的顺序依次减小,B和E同主族。下列推断不正确的是( )
A.A、B、E一定在不同周期 C.A、D可能在同一主族
B.C的最高价氧化物的水化物可能显碱性 D.C和D的单质可能化合形成离子化合物
第Ⅱ卷(非选择题共5题,共62分)
7. 恒温恒压下,在容积可变的容器中,反应2NO(g) N2O4(g)达到平衡后,再向容器内通入一定量NO2,又达到平衡时,N2O4的体积分数( )
恒温恒压下,在容积可变的容器中,反应2NO(g) N2O4(g)达到平衡后,再向容器内通入一定量NO2,又达到平衡时,N2O4的体积分数( )
A.不变 B.增大 C.减小 D.无法判断
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com