
题目列表(包括答案和解析)
5.解析:本题考查学生信息处理能力和基础知识的应用能力,充分利用氧化还原反应的知识来解答,同时利用化合价的代数和为零,
n(Cr3+)= 2.667/(127*2)*2/3=0.007(mol)
n(Cl)=4.52/143.5=0.0315(mol) n(Cr3+): n(Cl)=2:7
6解析:本题考查学生用化合价升降的的知识来解决判断氧化还原反应,属于很基本的题型
4.解析:本题考查学生的综合应用能力,用一般的解法就较复杂,如果用
“Cu原子守恒”和“关系式法”来解,就变得很简单了:CuCl2~~2HCl由这一关系式可得CuCl2为0.3mol,CuCO3 →CuO , Cu2(OH)2CO3→2 CuO,
CuO-2HCl
3.解析:本题考查学生对元素周期表的熟悉情况,特别是原子结构的变化规律。前10号元素最多有两个电子层电子层数之比为1:2或1:1,但只有同一主族最外层电子数相同而电子层数不同,故比值为1:2才满足。
2. 解析:本题考查学生的知识迁移能力,注重质量守恒定律的理解。
1. 解析:本题考查元素及化合物知识,属于基本题型,但同时也考查学生的知识应用能力,特别是:“原子守恒”、“差量法”的运用。反应的总方程式为: 2CH4+O2+6Na2O2==2Na2CO3+8NaOH
20.(1). 4FeS2 + 11O2 = 2Fe2O3 + 8SO2
(2)接触室、吸收塔
(3) SO2 + O2 = 2SO3
(4)净化二氧化硫和氧气。(因为三氧化硫很易跟水蒸气化合生成酸雾,会影响二氧化硫跟氧气的化合,以及三氧化硫的吸收。)
(5)可以通过调节气阀,控制气体流量,观察甲装置的冒泡速率估计。
(6)原因有两个:(1)浓硫酸对三氧化硫的吸收效果远好于水,三氧化硫被浓硫酸完全吸收了;
(2)插入浓硫酸溶液的导管插得太深,导致两个吸收瓶内的气压差较大,三氧化硫气体往水中冒出来了,与水蒸气化合形成酸雾。
(7) 用碱液吸收。
命题意图和试题解析(2004年)
19. (1) 饱和食盐水;(2分)装置漏气;(1分)用湿润的碘化钾淀粉试纸先靠近各边接口处检验,漏气处试纸变蓝 (涂肥皂水等合理方法均可)(3分)
(2) 关闭活塞后,若a中仍有气体发生,气体压强增大。将b中液体压入c中,整个装置成为储气装置,不会有气体逸出。(2分)
18.(1) (F)(E)接(D)(C)接(A)(B)[或(B)(A)]接(J)(I)接(H)(G)
(2)黑色氧化铜变红,无水硫酸铜变蓝;因为H2通过灼热的CuO后生成Cu和水蒸气,水蒸气使无水硫酸铜变蓝。
17. 17. (1) 4NH3+5O2=4NO+6H2O ①
2NO+O2=2NO2
3NO2+H2O=2HNO3+NO26 (1)
|
b∕a的取值范围 |
溶质 |
溶质物质的量 |
|
0<b∕a<5∕4
(0.5分) |
NH3 (0.5分) |
(a-4b∕5)mol
(1分) |
|
b∕a=5∕4
(1分) |
/ (0.5分) |
/
(0.5分) |
|
5∕4<b∕a<2 (0.5分) |
HNO3 (0.5分) |
(4b-5a)
∕3mol (1分) |
|
b∕a≥2 (0.5分) |
HNO3 (0.5分) |
amol
(1分) |
(2) HNO3 (1分)
ω(HNO3)=(2.00×63.0∕2.00×63.0+2.00×18.0)×100%=77.8% (1分)
c(HNO3)=1000×1.44×77.8%∕63.0 mol.L-1=17.8 mol.L-1 (2分)
13、(每空2分)(1)O2 (2)
(3)2SO2+O2===2SO3 2H2O =====2H2+O2
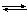 14 (1) 碱性 (1分) A2-+H2O HA-+OH- (1分)
14 (1) 碱性 (1分) A2-+H2O HA-+OH- (1分)
(2) BCD (3分,每个1分,错选0分)
(3) < (1分) H2A第一步电离产生的H+,抑制了HA-的电离。(2分)
(4) c(Na+ )> c(HA-)> c(H+)> c(A2-)> c(OH- ) (2分)
15
(1)

A C B
(A、B、C结构简式正确各1分,配平1分,共4分);
(2)
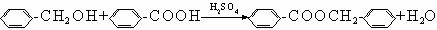
C D E
(D结构简式正确1分,E结构简式正确2分,配平1分,共4分);
(3)



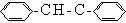 (3分);
(3分);
OH O
(4)A、E;D (每对1个1分,多选、答错倒扣分,但不出现负分,共3分);
(5)C (2分,多选、答错倒扣分,但不出现负分)
16
(1)CH4;H2S (每个1分,共2分);
(2)第VIA;CH3CH2SH (前者1分,后者1分,共2分);
(3)(CH3)2CHSH;C6H5SH (每个2分,共4分);
(4)丙硫酮;乙硫羰酸 (每个2分,共4分);
(5)
(对硝基苯硫酚结构简式正确1分,产物结构简式正确1分,配平1分,共3分);
(6)2 (1分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com