
题目列表(包括答案和解析)
1、下列事故处理中,不正确的是
A、误食铜盐立即喝牛奶或蛋清
B、金属钠着火用水扑灭
C、皮肤沾浓硫酸后,立即用水冲洗
D、碱液流到桌子上,立即往碱液里加适量的醋酸
20.解析:本题考查硫酸的工业制法,注重化学知识与工业生产的紧密结合,考查学生的实际应用能力,以及解决问题的能力,知识迁移的能力.
19.解析:本题是实验设计题,考查学生利用所学的基础知识来制备气体,同时还要考虑气体对空气的污染,不仅考察了学生的能力,而且培养和树立环境保护意识,达到教书育人的目的.本题还要应用到物理学的知识,考查学生的理科综合能力.
18.解析:本题是实验设计题,考查学生的基本实验技能,考查学生利用所学的基础知识进行实验设计和解决实际为了体的能力
17.解析:并列反应计算是高考考查的一个重点和热点,本题既要求抽象的字母计算,又要求给定具体数据的计算,具有较强的灵活性和较高的难度,适合作为压轴题。
(1) 4NH3+5O2=4NO+6H2O ①
2NO+O2=2NO2
3NO2+H2O=2HNO3+NO
将上述反应合并:NH3+2 O2= HNO3+ H2O ②
①当0<b∕a<5∕4,只发生反应①且NH3有剩,溶液中的溶质是NH3
4 NH3 ∽ 5 O2
 4b∕5
b
4b∕5
b
故n(NH3)=(a-4b∕5)mol
②当b∕a=5∕4,只发生且恰好完成反应①,而NO不溶于水,故不存在溶质。
③当5∕4<b∕a<2,发生①②两反应,溶液中的溶质是HNO3,设按①②反应的NH3分别为4xmol ymol,则:
4NH3+5O2=4NO+6H2O
4x 5x
NH3+2 O2= HNO3+ H2O
y 2y y
4x+y=a
5x+2y=b
y=(4b-5a) ∕3 故n(HNO3)= (4b-5a) ∕3mol
0.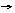 1 0.1 0.1
1 0.1 0.1
 HA- H+ +A2-
HA- H+ +A2-
若是单独存在的0.1mol.L-1 HA-溶液,[H+]=10-2 mol.L-1,第一步电离产生的H+会对第二步电离产生抑制作用,故第二步电离产生的[H+]<10-2 mol.L-1, 故[H+](总)<(0.1+0.01) mol.L-1=0.11 mol.L-1
15 解析 :本题为信息题,考察学生的知识迁移能力,同时也兼顾了学生基础有机化学知识的考察。
(1)化合物A含有醛基,根据其分子式C7H6O,减去醛基(CHO),即得C6H5(苯基),故A为苯甲醛。依据信息(1)进行迁移,利用信息(3),不难判断出B、C的结构,即可写出反应式。
(2)该题是上题的延续,如果说上题不知C的结构式还可以“蒙”对上题的4分,但到此必须明确C为苯甲醇、D为苯甲酸,这可以依据B到D的反应条件进行判断。另外,产物E的结构简式的写法必须注意,千万不要写成PhCH2OOCPh、PhCH2COOPh等错误形式,否则要扣2分(但要注意:写成PhCH2OCOPh是可以的)!
(3)根据“F能与金属钠反应放出氢气”、“醛基以外的基团没有任何变化”、与E(酯)是同分异构体和“不饱和碳碳键上连有羟基不稳定”的提示,可知F中含有2个没有变化的C6H5基团1个OH,但羟基没有和不饱和碳碳键相连,因此可以确定F结构为PhCH(OH)COPh。
(4)考察简单的有机知识。但要注意,A(醛)生成B和C的反应,既有醇(还原)生成,也有酸(氧化)生成,因此它既是还原反应,也是氧化反应。很明显,C和D生成E的反应是酯化反应,此为送分题,悄悄地隐藏在稍难题后面,主要考的是学生的应试心态。
(5)只要写出了F的结构式,该题易于判断,考察的是简单的有机知识。
16解析
本题以重庆井喷伤人事件为题材命题,体现了化学与社会的联系。题目由无机物入手,从结构特征出发,利用已知的有机物为信息进行迁移,考查内容层层深入,涉及有机物命名、酚的反应、氨基酸的性质等有机化学基本内容,具有一定的综合性。
(1)该题是送分题,仅作为引子。
(2)该题是上题的延续,一部分作为引子,一部分引入有机部分--实际考查的是“乙基”!--反过来,教师在教学中应启发学生注意:有机与无机两部分之间是怎样联系?
(3)该题是上题的继续,但暗中逐渐由醇的结构与命名转移到酚的结构与命名,实际考查的是“异丙基、苯基”,同时对“苯硫酚”的考查也为第5小题做铺垫。
(4)本题中继续进行知识迁移,进一步转移到酮和酸(羟基、羰基)的结构与命名的考察,此时具有一定的难度,但只要掌握了“硫放在正常命名前”的含硫化合物命名规律,其实也不难。因此,关键是知识迁移后能否自己悟出其中的规律。
(5)本题考察的是酚类的化学性质,但迁移至“硫酚”。作题时,一定还要注意:一、“对位”不要写错;二、“硝基”不要出现拼写错误!
(6)本题考察的是氨基酸的化学性质,但要注意该氨基酸(半胱氨酸)中含有具有一定酸性的“SH”基团(巯基)。
0.1mol.L-1H2A溶液
H2A= H+ + HA-
0.1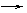 0.1 0.1
0.1 0.1
pH=2, [H+]=10-2 mol.L-1
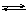 HA- H+ +A2-
HA- H+ +A2-
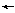
 10-2 10-2 10-2
10-2 10-2 10-2
故:[Na+ ]= 0.1mol.L-1 [ HA-]=0.1-0.01 水也电离产生[H+],故[H+]略大于10-2 mol.L-1 [A2-]=10-2 mol.L-1 [OH- ]=10-14∕10-2
可见:[Na+ ]> [ HA-]> [H+]>[A2-]>[OH- ]
0.1mol.L-1NaHA溶液:
NaHA= Na++ HA-
7. 解析:本题考查学生处理信息的能力和知识的迁移能力。
8解析:本题考查学生利用氧化还原中“化合价升降的总数相等”来解决问题的能力,不必对方程式进行配平,
9解析:本题考查学生对阿伏加德罗常数的正确理解,同时靠查原子结构的基本知识,属于结构的基本问题,学生容易解答
10解析:本题考查学生对化学用语“离子方程式”的理解,以及在书写时应注意的问题,特别是用到“量”和“氧化还原反应”问题时。
11解析:本题考查学生化学式中“正负化合价的代数和为零”的知识,属于基本体型学生容易解答,
12解析:本题考查学生处理问题的能力和知识的迁移能力,考查学生对烃的衍生物的性质的熟练程度
13解析:本题属于图框式元素及其化合物推断题,是近几年高考的常见题型,要求考生知识全面,善于抓住突破口,大胆猜想和推理,周密思维,从而得出正确的结果。
从图中得出的第一印象是丙几乎无处不在,联想到以下几条的反应路线可得出丙是O2


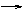 ①Na Na2O Na2O2 NaOH、O2
①Na Na2O Na2O2 NaOH、O2



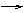 ②S SO2 SO3 H2SO4 O2、H2
②S SO2 SO3 H2SO4 O2、H2



 ③N2 NO NO2 HNO3 O2、H2
③N2 NO NO2 HNO3 O2、H2

 根据组成三种单质的元素的核电荷数之和为35,(或根据B+C D是Na2O+SO2 Na2SO3,而Na2O+NO 不反应),可推知三种单质分别是Na、S、O2而非Na、N2、O2,则:
根据组成三种单质的元素的核电荷数之和为35,(或根据B+C D是Na2O+SO2 Na2SO3,而Na2O+NO 不反应),可推知三种单质分别是Na、S、O2而非Na、N2、O2,则:



 产物之一
产物之一


 Na O2 Na2O O2 Na2O2 水 O2
Na O2 Na2O O2 Na2O2 水 O2





 Na2S
Na2SO3 O2 Na2SO4 ②电
Na2S
Na2SO3 O2 Na2SO4 ②电
解






 S O2 SO2 O2 ① SO3 水 H2SO4溶液
S O2 SO2 O2 ① SO3 水 H2SO4溶液
考试时,将物质推出来仅是成功了一半,要养成认真、准确、规范地答题的习惯,以免无谓失分。
14解析:.电解质溶液试题在今几年的全国高考,上海高考Ⅱ卷中屡有出现,这是一道另辟蹊径,思维要求较高的题目。
第(1)问要求书写水解方程式,符合规范才能得分。
第(2)问:A选项只要注意到H2A第一步电离是完全的,就能判断H2A在水溶液中不存在,从而否决它。B选项实质是物料守恒式。C选项实质是电荷守恒式。D选项反映的是:
[OH- ](水电离)= [H+](水电离)。
第(4)问的解答融于第(3)问的解答之中
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com