
题目列表(包括答案和解析)
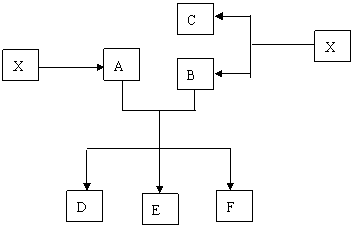
32.(10分)已知X为 和CuO的混合物,取两份等质量的X样品进行下列实验:
和CuO的混合物,取两份等质量的X样品进行下列实验:
|
|
|
|
固体 酸性溶液 无色气体
(1)写出①、②和③步所有反应的化学方程式;
(2)设从③步所得固体D的质量为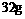 ,溶液E中只含有一种金属离子,气体F在标准状况下体积为
,溶液E中只含有一种金属离子,气体F在标准状况下体积为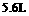 ,试计算取用的每份X的质量和X中
,试计算取用的每份X的质量和X中 和
和 的质量比。
的质量比。
31. (9分)如右图是一密闭容器,已知A端盛有2.3g金属钠,B端盛有
xgHgO,当同时加热容器的两侧支管时,钠着火燃烧,冷却后测得容
器中的空气成分并未发生变化,求x值。
30.(12分)⑴铝在人体中积累可使人慢性中毒,1989年世界卫生组织正式将铝“确定为食品污染源”之一而加以控制。铝在下列使用场合须加以控制的是:①制铝锭 ②制易拉罐 ③制电线电缆 ④制牙膏皮 ⑤用明矾净水 ⑥制炊具 ⑦用明矾和苏打作食物膨化剂 ⑧用AlOH)3制成药片治胃病 ⑨制防锈油漆
A.①②④⑤⑥⑦⑧ B.②⑤⑥⑦⑧
C.②④⑤⑥⑦⑧ D.③④⑤⑥⑦⑧
⑵小苏打的成分是NaHCO3,胃舒平中含有难溶性的Al(OH)3,它们都是治疗胃酸过多的药物。写出有关的离子反应方程式:______________________________。胃穿孔患者由于胃酸过多时,医生则禁止其服用小苏打,其原因是__________________________。
29.(8分)在长期载人太空飞行的航行器中,每个宇航员平均每天需消耗0.9kg氧气,呼出1.0kg二氧化碳。为了能保持飞船座舱内空气成分的稳定,宇航科学家进行了大量的科学探索。有的科学家得出“金属过氧化物处理系统”,即不断把座舱内的空气通过盛有金属过氧化物(以过氧化钠为例)的容器,并把处理后的气体充入座舱。有关反应的化学方程式是:
①__________________________________;②_______________________________ 。将处理后的气体充入座舱时,应注意采取的一项措施是_____________________________。
有人提出用超氧化钾(K02)代替过氧化钠供氧,预计其优点是_______________________。
28.(10分)A、B、C、D四种化合物其焰色反应均为紫色,A、B、C和盐酸反应均得到D,将固体C加热可制得A,若在A的溶液中通入一种无色无味气体,又可制得C,若B与C的溶液混合可制得A,试推断
(1)A是________,B是_________,C是_________,D是__________。
(2)完成有关方程式:
C A
________________________;A-→C __________________________;
A
________________________;A-→C __________________________;
B+C-→A _______________________________________________。
27.(10分)有A、B、C、D、E、F 6种化合物,其中A、B、C、D是铝元素的化合物,F是一种气体,在标准状况下,F的密度是空气密度的1.103倍。化合物间发生如下反应:
 ①A+NaOH
D+H2O
②B
①A+NaOH
D+H2O
②B A+H2O
A+H2O

 ③C+NaOH(适量)
B+NaCl ④E+H2O
NaOH+F
③C+NaOH(适量)
B+NaCl ④E+H2O
NaOH+F
(1)确定物质A、B、C、D的化学式:A_______,B________,C________,D________。
(2)1 mol和2 mol E在水溶液中发生反应的化学方程式为__________________________。
翰林汇翰林汇25. (11分)已知某白色粉末不是硝酸盐,为鉴定此物质,先将它溶于水制成无色溶液A,再对
A做下列实验,根据现象写出各步推断和最后结论:
|
实 验 步 骤 |
实 验 现 象 |
推 断 |
|
①取少量A,加入BaCl2溶液 |
无现象,得混合溶液B |
|
|
②向B中加入少量NaOH溶液 |
生成白色沉淀C |
|
|
③滤出C,加盐酸 |
放出无色、无嗅气体D |
|
|
④D通入澄清石灰水 |
产生白色沉淀 |
|
|
⑤用A做焰色反应 |
焰色为黄色 |
|
结论:此物质为____________。
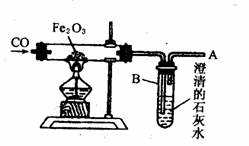 26.(8分)根据下图所示一氧化碳还原铁的氧化物的实验装置,回答下列问题。
26.(8分)根据下图所示一氧化碳还原铁的氧化物的实验装置,回答下列问题。
(1)判断硬质玻璃管中已开始发生反应的方法是_________________________________。
(2)反应过程中发生的现象是_________________________________________________。
(3)在A处点燃可见浅蓝色火焰的原因是_______________________________________。
(4)实验结束时应注意的操作是_______________________________________________。
①先停止通入CO2;②先熄灭酒精灯,并继续通入CO;③熄灭酒精灯,同时停止通入CO;④先熄灭酒精灯,继续通入CO,并点燃排出的CO气体。
24.相同质量的Na、Mg、Al与过量稀硫酸反应,在相同状况下产生H2的质量比为 ( )
A. 36:69:92 B. 92:69:36 C. 1:1:1 D. 3:2:1
第 Ⅱ 卷 (非选择题 共78分)
23.由铁、锌、铝、镁四种金属中的两种组成的混合物10g,与足量的盐酸反应产生的氢气在标准状况下为11.2L,则混合物中一定含有的金属是 ( )
A. 锌 B. 铁 C. 铝 D. 镁
22.按下列过程,最终能够实现的是 ( )
|
|
|


 A.Fe
FeCl2溶液
FeCl3溶液
FeCl3晶体
A.Fe
FeCl2溶液
FeCl3溶液
FeCl3晶体
|
|
|


 B.FeSO4溶液
Fe(OH)2 Fe(OH)3
Fe2(SO4)3溶液
B.FeSO4溶液
Fe(OH)2 Fe(OH)3
Fe2(SO4)3溶液
|

|
|
|
 C.
镀锌铁片
静置5min,刻痕处呈红色
C.
镀锌铁片
静置5min,刻痕处呈红色
|
|
|
|


 D.Cu CuO
CuSO4溶液
胆矾
D.Cu CuO
CuSO4溶液
胆矾湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com