
题目列表(包括答案和解析)
13.已知较低温度时:2NO2+H2O=HNO2+HNO3。结合已学过的有关知识推断下列结论,其中正确的是:(1)HNO3比HNO2更稳定;(2)HNO2的分解产物为NO和H2O;(3)HNO2的分解产物为NO2、NO和H2O。
A、只有(1) B、(1)(2) C、(2)(3) D、(1)(3)
12.恒温条件下,将NO2装入带活塞的的密闭容器中,当反应2NO2(g)  N2O4(g)达到平衡后,下列叙述正确的是
N2O4(g)达到平衡后,下列叙述正确的是
A.慢慢压缩气体体积,若体积减小一半,则压强为原来的两倍
B.若在恒温恒容积时通入一定量的NO2,平衡向左移动,混合气体的平均相对式量减小
C.若体积减小一半,压强增大,但小于原来的两倍
D.若在恒温恒压时通入一定量的N2O4,平衡不移动,但混合气体的平均相对式量增大
11.设NA表示阿伏加德罗常数的值,下列说法正确的是
①足量的CO2与31g Na2O2发生反应,转移的电子数为NA
②100mL1mol/L FeCl3溶液中,阴、阳离子总数大于0.4NA
③12g金刚石中所含的C-C键数为2NA ④18g的D2O与NA个CH3-具有相同的电子数
⑤标准状况,22.4L NO和22.4L O2的混合气体所含分子数为1.5NA
⑥在铜与硫的反应中,1 mol铜失去的电子数为2 NA
⑦62 g Na2O溶于水后所得溶液中含有O2- 离子数为NA
⑧46 g 二氧化氮和46 g四氧化二氮含有的原子数均为3 NA
⑨常温常压下1 mol NO2气体与水反应生成NA个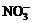 离子
离子
⑩1 mol水与足量的某金属单质在一定的条件下反应电子转移数最多可为2NA
A.①②④⑥⑧了 B⑤⑥⑦⑧⑨ C.②③⑤⑧⑩ D. ④⑧⑨⑩
10、下列各组离子能在指定溶液中,大量共存的是
①无色溶液中:K+,Cl-,Na+,H2PO4-,PO43-,SO42-
②使PH=11的溶液中:CO32-,Na+,AlO2-,NO3-,S2-,SO32-
③水电离的H+浓度C(H+)=10-12mol·L-1的溶液中:Cl-,HCO3-,NO3-,NH4+,S2O32-
④加入Mg能放出H2的溶液中:Mg2+,NH4+,Cl-,K+,SO42-
⑤使甲基橙变红的溶液中:Fe3+,MnO4-,NO3-,Na+,SO42-
⑥酸性溶液中:Fe2+,Al3+,NO3-,I-,Cl-,S2-
A ①②⑤ B ①③⑥ C ②④⑤ D ①②④
9、已知相同浓度的碳酸中c(CO32-)比偏铝酸中的c(AlO2-)大得多,则下列推论中正确的是:
A.通入适量CO2于AlO2-溶液中,有CO32-生成
B.含CO32-的溶液容易使Al(OH)3溶解变成AlO2-
C.HCO3-只能Al3+反应而不能和A1O2-反应
D.在水溶液中HCO3-不能与A1O2-大量共存
8、最近,科学家用一种称为“超酸”的化合物H(CB11H6Cl6)和C60反应,使C60获得一个质子,得到一种新型离子化合物[HC60]+[CB11H6Cl6]-。该反应看起来很陌生,其实在反应类型上可以跟中学化学里某个熟悉的化学反应相类似。该化学反应是 ( )
 A.H2O+CH3COOH
H3O++CH3COO- B.Zn+2HCl
A.H2O+CH3COOH
H3O++CH3COO- B.Zn+2HCl ZnCl2+H↑
C.CO2+2NH3 CO(NH2)2+H2O
D.NH3+HCl NH4Cl
7.2003年诺贝尔化学奖授予了美国科学家Peter Agre和Roderick Mackinnon以表彰他们在“水通道”和“离子通道”的研究成就。Mackinnon教授的研究内容主要是Na+、K+体积很接近,但在生物体内呈现的差别却高达1万倍,他革命性的让科学家观测Na+、K+在进入离子通道前、通道中以及穿过通道后的状态,可为病人在“离子通道”中寻找具体的病因,并研制相应药物。下列关于钠、钾的说法正确的是
A.单质钠的密度比钾的密度小 B.钠和钾在空气中燃烧的产物都是过氧化物
C.钠和钾都是短周期元素 D.钠和钾的合金[ω(K)=50%-80%]熔点比钠和钾都高
6、以下说法中能证明无色透明液体是纯净水的是
A.测得该液体pH=7
B.电解该液体得到氢气和氧气,且其体积比为2:1
C.向其中投入金属钠,钠于液面上迅速游动,并发出丝丝声
D.在l.0l×105Pa压强下测得沸点为373.15K
5、类推的思维方法在化学学习与研究中常会产生错误的结论,因此类推的结论最终要通过实验的验证才能决定其正确与否。下列几种类推的结论中正确的是:
A. 已知Fe与S能直接化合得FeS,推测Cu与S化合直接化合生成CuS
B.已知A12S3不能在水溶液中存在,推测Mg3N2不能在水溶液中存在
C.已知H2O比H2S的沸点高,推测H2S比H2Se的沸点高
D.已知工业上用电解熔化的NaCl制取Na,推测用熔化的A1C13制取Al
4、化学实验中常将溶液或试剂进行酸化,下列酸化处理的措施中正确的是( )
A.定性检验SO32-,将BaCl2溶液用HNO3酸化
B.为提高高锰酸钾溶液的氧化能力,用盐酸将高锰酸钾溶液酸化
C.检验溶液中是否含有Fe2+时,用硝酸酸化
D.验溶液中是否含有SO42-时,在无其他阳离子干扰的条件下,先用盐酸酸化,所得溶液再加BaCl2溶液
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com