
题目列表(包括答案和解析)
1. 下列事实与氢键有关的是
A.水加热到很高的温度都难以分解
B.水结成冰体积膨胀,密度变小
C.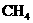 、
、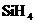 、
、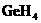 、
、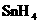 熔点随相对分子质量增大而升高
熔点随相对分子质量增大而升高
D.HF、HCl、HBr、HI的热稳定性依次减弱
4.(★★★★★)在某条件下,容器中有如下平衡反应:
A+4B  2C+D(正反应放热)
2C+D(正反应放热)
此时,A、B、C的物质的量均为a mol,而D的物质的量为d mol。
(1)改变a的取值,再通过改变反应条件,可以使反应重新达到平衡,并限定达到新的平衡时,D的物质的量只允许在d/2到2d之间变化,则a的取值范围 (用a和d的关系式表示)。
(2)如果要使本反应重新建立的平衡中,D的物质的量只允许在d到2d之间取值,则应该采取的措施是 (从下面列出的选项中选择)。
A.升高反应温度 B.增大反应容器内之压强
C.增大反应容器容积 D.降低反应温度
E.减小反应容器内之压强 F.减小反应容器容积
3.(★★★★)若nD=3.0 mol,不论平衡如何移动,其他条件同例题,求x的取值范围。
2.(★★★★)题设同例题,求右侧平衡起始时向逆反应方向移动的x的取值范围。
1.(★★★)题设同例题,求右侧平衡不移动时x的取值。
2.极限思维:有口诀如下:
始转平、平转始,欲求范围找极值。
极限思维是解此类问题的常用方法。
●歼灭难点训练
1.列方程法:根据反应移动的方向,设出某反应物消耗的量,然后列式求解。
26.将一定量的CO2气体通入500mL某NaOH溶液中,充分反应后,将溶液在低温下蒸发,得到不含结晶水的白色固体A,取三份质量不同的A样品分别与50mL相同浓度的盐酸反应,得到气体体积(标准状况)与固体A的质量关系如下表所示:
|
组别 |
1 |
2 |
3 |
|
盐酸体积(mL) |
50 |
50 |
50 |
|
A的质量(g) |
3.80 |
6.20 |
7.20 |
|
气体体积(mL) |
896 |
1344 |
1344 |
问:(1)在表中第 组数据表明加入的50mL盐酸反应后有剩余,理由是 .
26. (7分)某同学用50mL NaOH溶液吸收CO2气体制备Na2CO3.为防止通入的CO2过量而生成NaHCO3,他设计了如下步骤:
(7分)某同学用50mL NaOH溶液吸收CO2气体制备Na2CO3.为防止通入的CO2过量而生成NaHCO3,他设计了如下步骤:
(i)用25mL NaOH溶液吸收过量的CO2气体至CO2气体不再溶解;
(ii)小心煮沸溶液1~2分钟;
(iii)在得到的溶液中加入另一半(25mL)NaOH溶液,使溶液充分混合.
(1)他能否制得较纯净的Na2CO3 ,理由是 .
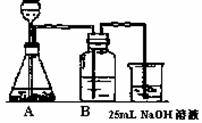
(2)按他的设计,第(i)步实验装置如图
①装置A使用的试剂是石灰石和盐酸.可否使用纯碱代替石灰石 .
②装置B使用的试剂的作用是 .
③为了后续的煮沸、混合等实验,装NaOH溶液的容器还可使用 (填实验仪器).
④有人认为实验步骤(ii)、(iii)的顺序对调,即先混合再煮沸更合理,你认为对吗?为什么?
25.(7分)实验室配制500mL0.1mol/LNa2CO3溶液回答下列问题:
(1)应用托盘天平称取十水碳酸钠晶体____ ___g。
(2)若在称量样品时,药品放在天平右盘上,砝码放在天平左盘上,天平平衡时,则实际称量的碳酸钠晶体是______g(1g以下用游码)。
(3)用托盘天平和小烧杯称出碳酸钠晶体的质量,其正确操作顺序的标号为___________ ____(同一步骤可用多次)。
A.调整零点
B.将游码移至刻度尺的零刻度处
C.将碳酸钠晶体放入小烧杯中称量
D.称量空的小烧杯
E.将砝码放回砝码盒内
F.记录称量结果.
(4)配制Na2CO3溶液时需用的主要仪器有_____________ _______。
(5)若实验遇下列情况,溶液的浓度是偏高,偏低还是不变?
A.加水时越过刻度线_________。
B.忘记将洗涤液加入容量瓶__________。
C.定容后摇匀液面低于刻度线______________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com