
题目列表(包括答案和解析)
解:设需甲醇的质量为xg ,生成的N2体积为YL,
(1)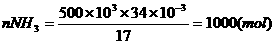
(2)6NH3 ~ 6NHO3 ~ 5CH3OH ~ 3N2
6 5 ×32 3×22.4
1000×0.95×0.84 x y
解得:x=21280(g)=21.82(kg) y=8.9376×103(L)
解:略
26(9分)(1)t℃和ρPa时D的气体密度ρ(g·L-1)或D气体的摩尔质量(g·mol-1)(2分)
m=19.5+11.0-3.00×ρ=30.5-3ρ (2分)或:19.5+11.0-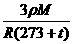
(2)盐酸的物质的量浓度(Cmol/L)(1分)
计算式:Mg+2HCl=MgCl2+H2↑
24 2 得:C=4(mol/L)(1分)
0.48 0.01×C
 讨论:①当C(HCl)≥4mol/L,应:Mg
H2↑
讨论:①当C(HCl)≥4mol/L,应:Mg
H2↑
24 22.4 VH2=0.448(L) (2分)
由:2Na2CO4 ~ O2↑
2×122 22.4
0.9mol VL
得:V=0.083L=83(ml)24(15分)(一)测定样品铜的质量分数(2分),(三)(2)
|
|
|
||||||
2H2O 2H2O+O2↑ (2分);(3)2Cu+O2 2CuO(1分) C+O2 CO2(1分)
22(10分)D、CO2、F、NH3(各1分)A、NH4HSO4, B、Ba(HCO3)2(各2分);
“A”不能推(NH4)2SO4,因为其水溶液呈弱酸性,“B”不能推Ba(HSO3)2,因为其水溶液呈弱酸性。NH+ 4 +HCO- 3 +2OH-=NH3↑+CO2- 3 +2H2O(2分)
20(14分)①方法1:将CH3COONa晶体溶于适量水中,然后滴入酚酞溶液,显红色。方法2:取适量CH3COOH溶液,向其中加入中甲基橙溶液,呈红色,然后加入适量CH3COONa晶体,溶液颜色为橙色。(每空2分)②(10分)(1)OH-、K+、Cl-、SO2- 4 ; (2)Ba2+、Ag+、Fe3+、NO- 3 ;(各2分)(3)Fe、Ag(各1分); (4)OH-、Cl-、Fe+、Ag+、SO2- 4 、、、Ba2+(3分)KNO3(1分)
25(6分)用甲醇处理含有氨的废水,在某种细菌中作用下,发生如下反应:
|
 ①NH3+O2 HNO3+H2O
①NH3+O2 HNO3+H2O
|
 ②6HNO3+5CH3OH 3N2↑+5CO2↑+13H2O
②6HNO3+5CH3OH 3N2↑+5CO2↑+13H2O
(1)方程式①配平后的系数分别为: 。
(2)对某废水处理时,氨有95%转化为硝酸,硝酸有84%转化为氮气。若废水中含NH3 34mg·L-1,处理这样的废水500m3(密度以1g·cm-1计算),计算需甲醇的质量(kg)和放出氮气的体积(L)。
26.(9分)计算以下两小题时,除必须应用所给的数据外,还各缺少一个数据,指出该数据的名称和符号(包括单位),并列出计算式。
(1)在温度为t℃时和压强为ρ Pa的情况下,19.5gA与11.0gB恰好完全反应,生成固体C和3.00L的D气体,计算生成的C的质量(m)。
缺少的数据是:
计算式为m=
(2)已知:M(Mg)=24g·mol-1,Vm=22.4L·mol-1,今有0.48g金属镁与10mL的盐酸反应,计算生成的H2在标态的体积(VH2)。缺少的数据:
计算式为:
 单元十三化学实验
单元十三化学实验
(五)问题讨论:
(1)E中盛试剂为 ,其作用是 。
(2)根据上述实验方案测得的铜的质量分数,跟实际的质量分数相比,是偏高、偏低、是相等? ,原因是 。
(3)如需要对同学设计的实验装置进行改进,请提出改进的方案是
。
(四)计算:实验时,C中反应完全,D中吸收完全,根据所得数据,样品中铜的质量分数
= (用含W,m1,m2的代数式表示)。
(三)实验步骤:
(1)
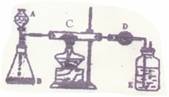 在C中加入样品粉末W,在D中装入药品后,
在C中加入样品粉末W,在D中装入药品后,
称得质量为m,选择仪器安装后,检查气密性。
(2) 打开A的活塞,慢慢滴加溶液,在B中进行
的化学反应方程为:
(3)C进行加热,当C中药品充分反应后,关闭A的活塞,停止加热,C中发生反应的方程式为 。
(4)冷却后,称量D的质量为m2;
(二)实验用品:仪器:天平,分液漏斗,锥瓶,硬质玻璃管,干燥管,酒精灯,洗气瓶等。
23.(8分)已知过氧碳酸钠(Na2CO4)和盐酸反应的化学方程式为:
 2Na2CO4+4HCl=4NaCl+O↑+2CO2↑+2H2O
2Na2CO4+4HCl=4NaCl+O↑+2CO2↑+2H2O
商品过氧碳酸钠中往往含有
少量的碳酸钠。为测定其纯度
,现称取0.90g样品进行实验。
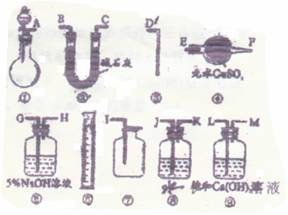
供选用的仪器、试剂如右图所
示。
(1)为了使实验尽可能简单,
应选用的装置是(填编号) 。
(2)所选用的装置的连接顺序是(填字母) 。
(3)若所测定的O2质量为mg,则样品的纯度为 。
(4)实验室有50mL,100mL,500mL三种规格的量筒,实验时用的量筒的规格为
。
24(15分)某同学加热炭粉(过量)和氧化铜和混合物,并用如图所示的装置对获得的铜粉(含炭)样品进行实验测定,请完全实验报告。(一)实验目的: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com