
题目列表(包括答案和解析)
26.(9分)孔雀石和石青是自然界存在的两种碳酸盐类铜矿,它们的化学组成可表示为:
xCuCO3·yCu(OH)2 (x、y为正整数且x≤2 ,y≤2)
(1)孔雀石和石青分别与过量盐酸反应时,孔雀石耗用盐酸的物质的量与生成CO2的物质的量之比为4:1;石青则为3:1。请推算它们的化学组成。
孔雀石: ;
石青: 。
(2)现有孔雀石和石青混合样品,取两份等质量的样品,在一份中加入过量盐酸,生成CO23.36L(标准状况下);加热另一份样品使其完全分解,得到CuO20g,试通过计算确定该混合物中孔雀石和石表的物质的量之比。
25.(6分)K2CO3、KHCO3混合粉末mg,加热到质量不再减少为止,剩余物质的质量为ng,则:
(1)混合物K2CO3的质量为 g。
(2)题干条件中n的数值应满足的范围是 。
(3)若将加热前的该混和粉末与足量盐酸反应,将所得溶液蒸干,可得KCl固体的质量为 g。
24.(6分)有一澄清溶液,其中只可能含有下列离子:H+、K+、Na+、Mg2+、Ba2+、NH4+、Al3+、Fe3+、SO42-、CO32-、Cl-、I-中的某几种,进行如下实验:
(1)用pH试纸检验,试纸呈深红色。
(2)取部分溶液加入少量氯水后分成两份,其中一份加入少许CCl4,振荡、静置后液体分层,下层呈黄绿色;向另一份中加入AgNO3溶液,发现有白色沉淀生成。
(3)另取部分溶液,逐滴加入NaOH溶液至过量,在滴加过程中未发现有沉淀生成。
(4)取(3)所得碱性溶液,加入Na2CO3溶液,有白色沉淀生成,取上层清液进行焰色反应,火焰呈黄色。
(5)取(3)所得的碱性溶液,加热,有气体产生,该气体能使湿润的红色石蕊试纸变蓝色。据以上判断,该溶液中肯定含有 离子, 离子不能肯定 否存在。
23.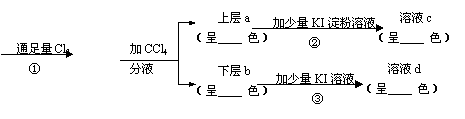 (8分)按下面的实验过程填空
(8分)按下面的实验过程填空
浅绿色FeBr2溶液 黄色液体
(1)在图表中填上相应的内容。
(2)写出反应的化学方程式:
①
②
22.(7分)某化学反应的反应物和产物如下:
KMnO4+KI+H2SO4→MnSO4+I2+KIO3+K2SO4+H2O
(1)该反应的氧化剂是 。
(2)若该反应方程式是I2和KIO3的化学计量数都是5,则KMnO4的化学计量数是 。请在下面的化学式上标出电子转移的方向和数目。
KMnO4+KI+H2SO4→
(3)若不限定某些物质的计量数,可能配平的化学计量数有许我组,原因是
。
21.(3分)在101kPa, 1.00gC6H6(1)燃烧生成CO2和H2O(1),放出41.8kJ的热量,请写出表示C6H6(1)燃烧热的热化学方程式:
20. (12分)某种含有少量氧化钠的过氧化钠试样(已知试样质量为1.560g,锥形瓶和水的质量为190.720g),利用下图装置测定混合物中Na2O2的质量分数,每隔相同时间读得电子天平的数据如表:
(12分)某种含有少量氧化钠的过氧化钠试样(已知试样质量为1.560g,锥形瓶和水的质量为190.720g),利用下图装置测定混合物中Na2O2的质量分数,每隔相同时间读得电子天平的数据如表:
(1)写出Na2O2与H2O反应的化学方程式 。
(2)计算过氧化钠质量分数时,必需的数据是 、 、
。
|
操作I:将样品加入稀盐酸中 → 溶液转移 → 操作II → 称量
①操作II的名称是 。
②需直接测定的物理量是 。
③测定过程中需要的仪器有电子天平、蒸发皿、酒精灯、还需要 、
(固定、夹持仪器除外)
④在转移溶液时,如溶液转移不完全,则Na2O2质量分数的测定结果 (填“偏大”“偏小”或“不变)。
19.(3分)用托盘天平和小烧杯称量一角匙NaOH的质量,正确的操作顺序为(填序号,可重复) 。
A.调整零点,使指针静止时处于标尺中间B.将游码拨到刻度尺的零处
C.取NaOH放烧杯中称量 D.称量小烧杯的质量
E.将砝码放回砝码盒内 F.记录称量结果
18.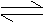 氯水的成分中含Cl2、、HCl、HClO,在与其它物质反应时,有时以Cl2为主,有时以HCl、HClO为主,然后Cl2+H2O HCl+HClO平衡发生移动。则新制氯水与下列溶液的反应中属于前者的是 ( )
氯水的成分中含Cl2、、HCl、HClO,在与其它物质反应时,有时以Cl2为主,有时以HCl、HClO为主,然后Cl2+H2O HCl+HClO平衡发生移动。则新制氯水与下列溶液的反应中属于前者的是 ( )
①NaHS ②NaOH ③KI ④AgNO3
A.①④ B.①②③ C.①② D.①③
第Ⅱ卷(选择题,共54分)
17.亚氯酸盐(如NaClO2)可用作漂白剂,在常温下不见光时可保存约1年。但在酸性溶液中因生成亚氯酸而发生分解:5HClO2=4ClO2+H++Cl-+2H2O分解时,刚加入硫酸反应缓慢,随后突然反应迅速,释放出气态的二氧化氯,这是因为 ( )
A.酸使亚氯酸的氧化性增强 B.溶液中的H+起催化作用
C.溶液中的Cl-起催化作用 D.逸出ClO2使反应的生成物浓度降低
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com