
题目列表(包括答案和解析)
12、 某温度下,反应H2(g)+I2(g) 2HI(g)+Q,在一带有活塞的密闭容器中达到平衡,
某温度下,反应H2(g)+I2(g) 2HI(g)+Q,在一带有活塞的密闭容器中达到平衡,
下列说法不正确的是
A、 恒温压缩体积,平衡不移动,颜色加深
B、恒压迅速充入HI,开始时正反应速率减小
C、恒容,升温正反应速率减小
D、 恒容,充入H2,I2的百分比含量降低
9、 在CuCl2水溶液中存在如下平衡:[Cu(H2O)4]2++4Cl- [CuCl4]2-+4H2O能使黄绿
在CuCl2水溶液中存在如下平衡:[Cu(H2O)4]2++4Cl- [CuCl4]2-+4H2O能使黄绿
(蓝) (绿)
色CuCl2溶液向蓝色转化的操作是
A、蒸发浓缩 B、加水稀释 C、加入AgNO3 D、加入食盐晶体
 10、反应A(g)+xB(g) yC(g),将A与B按体积比1:x混合反应当A的转化率是50%时,反应前混合气体的密度是反应后混合气体密度的
10、反应A(g)+xB(g) yC(g),将A与B按体积比1:x混合反应当A的转化率是50%时,反应前混合气体的密度是反应后混合气体密度的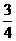 (同温同压),则x、y的值可能是
(同温同压),则x、y的值可能是
A、3,4 B、3,2 C、3,3 D、1,1
 11、在容积一定的密闭窗口中,反应A B(g)+C(s)达平衡,若继续升高温度,容器内气体的密度增大,下列判断正确的是
11、在容积一定的密闭窗口中,反应A B(g)+C(s)达平衡,若继续升高温度,容器内气体的密度增大,下列判断正确的是
A、 压强对该反应的平衡移动没有影响
B、在平衡体系中加入C,混合气体平均分子量增大
C、若正反应为吸热反应,则A为非气态
D、 若正反应为放热反应,则A为气态
8、

 下列平衡:C2H2+H2 C2H4……① 2CH4 C2H4+2H2……②当降低温度时,①式
下列平衡:C2H2+H2 C2H4……① 2CH4 C2H4+2H2……②当降低温度时,①式

 向右移动,②式向左移动,试判断下列式中C+2H2 CH4+Q1 2C+H2 C2H2+2Q2
向右移动,②式向左移动,试判断下列式中C+2H2 CH4+Q1 2C+H2 C2H2+2Q2
 2C+2H2 C2H4+2Q3
Q1、Q2、Q3的大小顺序为
2C+2H2 C2H4+2Q3
Q1、Q2、Q3的大小顺序为
A、Q1>Q2>Q3 B、Q1> Q3> Q2 C 、Q2> Q1 >Q3、 D、Q2>Q3 >Q1
7、下列事实不能用勒沙特列原理说明的是
A、 往氢硫酸溶液中加入盐酸,[S2-]降低。
B、温度不变时,敞口久置于空气中的饱和KNO3溶液含有晶体析出。
C、在合成氨的工业生产中,使用较高的温度有利于提高产量。
D、 在密闭容器中,水面上方的蒸气压强随温度升高而增大。
6、 在PCl5(g) PCl3(g)+Cl2(g),达到平衡后,其它条件不变,向平衡体系中加入37Cl2,达到新平衡后,含37Cl的PCl3的物质的量与原平衡相比
在PCl5(g) PCl3(g)+Cl2(g),达到平衡后,其它条件不变,向平衡体系中加入37Cl2,达到新平衡后,含37Cl的PCl3的物质的量与原平衡相比
A、增大 B、减小 C、不变 D、不能确定
5、对处于化学平衡的体系,以化学平衡与化学反应速率的关系可知:
A、化学反应速率变化时,化学平衡一定发生移动。
B、化学平衡发生移动时、化学反应速率一定变化。
C、正反应进行的程度大、正反应速率一定大。
D、只有催化剂存在下,才会发生化学反应速率变化,而化学平衡不移动的情况。
4、在一个固定体积的密闭容器中,放入mmol的A和nmol的B,发生如下反应:
 mA(g)+nB(g)
PC(g),平衡时C的浓度是wmol·L-1,若维持容器的体积不变,起始时放入amolA、bmolB和cmolC,要使平衡时C的浓度仍为wmol·L-1,则a、b、c必须满足的条件是
mA(g)+nB(g)
PC(g),平衡时C的浓度是wmol·L-1,若维持容器的体积不变,起始时放入amolA、bmolB和cmolC,要使平衡时C的浓度仍为wmol·L-1,则a、b、c必须满足的条件是
A、a:b:c=m:n:p B、a:b=m:n和
C、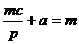 和
和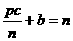 D、a=
D、a=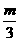 , c=
, c=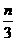 和c=
和c=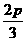
3、现有三个体积相等的密闭容器中都进行如下反应:
 CO2+H2 CO+H2O(g),反应所处的温度相同,但反应的起始浓度不同,其中甲:
CO2+H2 CO+H2O(g),反应所处的温度相同,但反应的起始浓度不同,其中甲:
[H2]=[CO]=amol 乙:[CO2]=amol [H2]=2amol 丙[CO2]=[H2]=[H2O]=amol,达到平衡时,CO的浓度由大到小的顺序排列正确的是
A、丙>甲>乙 B、甲>乙>丙 C、乙>丙>甲 D、乙>甲>丙
2、在2L密闭容器中,盛有2mol X和2molY物质进行如下反应:
 X(s)+3Y(g)
Z(g),当反应进行到10s后,测得生成0.5mol Z,这期间的平均反应速率为
X(s)+3Y(g)
Z(g),当反应进行到10s后,测得生成0.5mol Z,这期间的平均反应速率为
A、vX=0.05mol·s-1 B、vX=0.025mol·L-1·s-1
C、vy=0.05mol·L-1·s-1 D、vy=0.075mol·L-1·s-1
1、 对于反应A2+3B2 2AB3以下表示的反应速率中,速率最大的是
对于反应A2+3B2 2AB3以下表示的反应速率中,速率最大的是
A、vA=0.4mol·L-1min-1 B、vB=0.8mol·L-1min-1
C、v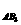 =0.6mol·L-1min-1
D、v
=0.6mol·L-1min-1
D、v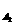 =0.01mol·L-1·S-1
=0.01mol·L-1·S-1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com