
题目列表(包括答案和解析)
1.下列晶体中,不属于原子晶体的是 ( )
A.干冰 B.水晶 C.晶体硅 D.金刚石
13. ⑴ 生成的CO2以及未反应的CO ⑵ 管内固体由红色变为黑色 ⑶ 6e-
⑷ 为了排尽装置内的空气 ⑸ CO和H2O(g) 点燃
⑹ HCOOH 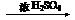 H2O+CO↑ 浓H2SO4 脱水
H2O+CO↑ 浓H2SO4 脱水
⑺
12. ⑴ +3 ⑵Cl-;Ag+、CO32-、OH-;H+、Cu2+;观察溶液颜色,如为蓝色则有Cu2+;加足量铁粉,有气泡产生,则有H+。(其它答案合情合理亦可)
11. ⑴ I-被ClO-氧化为I2,遇淀粉变蓝, 2H++ClO-+2I- H2O+I2+Cl-(或H2O+ClO-+2I-
H2O+I2+Cl-(或H2O+ClO-+2I- 2OH-+I2+Cl-)
2OH-+I2+Cl-)
⑵ I2和SO32-反应生成I-, H2O+I2+H2SO3 4H++SO42-+2I-
4H++SO42-+2I-
⑶ ClO->I->SO42-
10. ⑴
KMnO4 、O2 ⑵ Cl2+K2MnO4 2KCl+MnO2+O2↑ ⑶ 6
2KCl+MnO2+O2↑ ⑶ 6
1. D 2. D 3. D 4. D 5. B 6. B 7. B 8. C 9. A
13.(22分)如图所示一氧化碳还原铁的氧化物的实验装置,回答下列问题。

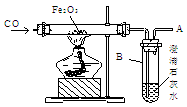
(1)硬质玻璃管右端出来的气体是_____________________。
(2)反应过程中硬质玻璃管发生的现象是_________________________________________。
(3)该反应中电子转移数目为________________。
(4)实验开始时应先通入一段时间的CO,是为了______________________________________。
(5)在A处排出的气体是_______________,如何进行除去尾气?_______________。
(6)写出实验室制取CO的化学方程式________________________________________,利用了________的__________性。
(7)在上面方框内,试用简图画出CO的发生装置,并标明试剂。
 第一单元 化学反应及其能量变化 参考答案
第一单元 化学反应及其能量变化 参考答案
12.(12分)(1)24mL浓度为0.05mol/L的Na2SO3溶液恰好与20mL浓度为0.02mol/L的K2Cr2O7溶液完全反应。已知Na2SO3被K2Cr2O7氧化为Na2SO4,则元素Cr在还原产物中的化合价为 。
(2)某电解质溶液中,可能大量存在有Ag+、H+、Cu2+、CO32-、OH-、Cl-离子,你认为一定有的离子是______,一定没有的离子是 ;还需要进一步确认的离子是_______,怎样判断有无
。
11. (15分)(1)在淀粉碘化钾溶液中,滴入少量次氯酸钠溶液,立即会看到溶液变蓝色,这是因为 ,反应的离子方程式是 。
(2)在碘和淀粉形成的蓝色溶液中,滴加亚硫酸溶液,发现蓝色逐渐消失,这是因为
,反应的离子方程式是 。
(3)对比(1)和(2)实验所得,将I2、ClO-、SO42-按氧化性由强到弱的顺序排列为 。
10. (12分)在氯酸钾的分解反应里,二氧化锰的催化问题到目前还没有肯定的解释。鉴于制得的氧化中有氯气的气味,生成的氯化钾又略显紫红色,认为反应过程如下:
Ⅰ: 2KClO3
+ 2MnO2  2A + B↑+ C↑ Ⅱ: 2A
2A + B↑+ C↑ Ⅱ: 2A  D + MnO2
+ C↑
D + MnO2
+ C↑
Ⅲ: B + D  2KCl + + C↑
2KCl + + C↑
(1)反应Ⅰ中氧化产物是(填化学式) 。
(2)反应Ⅲ的化学方程式为 。
(3)按上述反应过程,若制取1.5mol氧气,总共有 mol电子发生转移。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com