
题目列表(包括答案和解析)
5.等物质的量浓度的下列溶液中,c(NH4+)最大的是( )
A.NH4HSO4 B.NH4HCO3 C.NH4Cl D.NH4NO3
4.用物质的量都是0.1mol的CH3COOH与CH3COONa配制成1L溶液,已知其中c(CH3COO-)>c(Na+),有关该混合液的下列判断正确的是( )
A.c(H+)>c(OH-) B.c(CH3COOH)>c(CH3COO-)
C.c(CH3COO-)+c(CH3COOH)=0.2mol/L D.c(CH3COO-)+c(OH-)=0.1mol/L
3.某酸的酸式盐NaHY在水溶液中,HY-的电离度小于HY-的水解程度。有关叙述中正确的是( )
A.H2Y在电离时为:H2Y+H2O HY-+H3O+
HY-+H3O+
B.在该盐的溶液中,离子浓度为:c(Na+)>c(Y2-)>c(HY-)>c(OH-)>c(H+)
C.在该盐的溶液中,离子浓度为:c(Na+)>c(HY-)>c(Y2-)>c(OH-)>c(H+)
D.HY-水解方程式为:HY-+H2O Y2-+H3O+
Y2-+H3O+
2.某二元酸H2A在水中发生电离:H2A H++HA-,HA-
H++HA-,HA- H++A2-。下列叙述中不正确的是( )
H++A2-。下列叙述中不正确的是( )
A.在NaHA溶液中c(Na+)>c(HA-)>c(OH-)>c(H+)
B.在Na2A溶液中c(Na+)>c(A2-)>c(OH-)>c(H+)
C.在NaHA溶液中c(Na+)>c(H+)=c(HA-)+2c(A2-)>c(OH-)
D.在H2A溶液中c(H+)=c(HA-)+2c(A2-)+c(OH-)
1.实验室中配制一种混合溶液,要使溶液中c(K+)=c(Cl-)=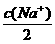 =c(SO42-),可选用的溶质可能是( )
=c(SO42-),可选用的溶质可能是( )
A.KCl、Na2SO4 B.NaCl、K2SO4
C.NaCl、Na2SO4、K2SO4 D.KCl、Na2SO4、K2SO4
在溶解中盐的离子跟水所电离出的H+或OH-生成弱电解质的反应,叫做盐类的水解。
强酸弱碱盐如NH4Cl、Al2(SO4)3等水解后溶液呈酸性;强碱弱酸盐如CH3COONa、Na2CO3等水解后溶液呈碱性。多元弱酸盐还要考虑分步水解,如CO32-+H2O HCO3-+OH-、HCO3-+H2O
HCO3-+OH-、HCO3-+H2O H2CO3+OH-。
H2CO3+OH-。
水是一种极弱的电解质,它能微弱地电离,生成H3O+和OH-,H2O H++OH-。在25℃(常温)时,纯水中c(H+)=c(OH-)=1×10-7mol/L。
H++OH-。在25℃(常温)时,纯水中c(H+)=c(OH-)=1×10-7mol/L。
在一定温度下,c(H+)与c(OH-)的乘积是一个常数:水的离子积KW=c(H+)·c(OH-),在25℃时,KW=1×10-14。
在纯水中加入酸或碱,抑制了水的电离,使水的电离度变小,水电离出的c(H+)水和c(OH-)水均小于10-7mol/L。在纯水中加入弱酸强碱盐、弱碱强酸盐,促进了水的电离,使水的电离度变大,水电离出的c(H+) 或c(OH-)均大于10-7mol/L。
电解质溶解于水或受热熔化时,离解成能自由移动的离子的过程叫做电离。
强电解质如NaCl、HCl、NaOH等在水溶液中是完全电离的,在溶液中不存在电解质分子。弱电解质在水溶液中是少部分发生电离的。25℃0.1mol/L的如CH3COOH溶液中,CH3COOH的电离度只有1.32%,溶液中存在较大量的H2O和CH3COOH分子,少量的H+、CH3COO-和极少量的OH-离子。多元弱酸如H2CO3还要考虑分步电离:
H2CO3 H++HCO3-;HCO3-
H++HCO3-;HCO3- H++CO32-。
H++CO32-。
9.一定条件下,可逆反应X(g)+3Y(g)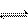 2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),平衡时,X、Y、Z的浓度分别为0.1mol·L-1,0.3 mol·L-1,0.08 mol·L-1,则下列判断不合理的是
A.c1∶c2=1∶3
B.平衡时,Y和Z的生成速率之比为3∶2
2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),平衡时,X、Y、Z的浓度分别为0.1mol·L-1,0.3 mol·L-1,0.08 mol·L-1,则下列判断不合理的是
A.c1∶c2=1∶3
B.平衡时,Y和Z的生成速率之比为3∶2
C.X、Y的转化率不相等 D.c1的取值范围为0<c1<0.14 mol·L-1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com