
题目列表(包括答案和解析)
13.某温度下在密闭容器中发生如下反应:2M(g)+N(g)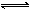 2E(g)
2E(g)
若开始时只充入2 mol E(g),达到平衡时,混合气体的压强比起始时增大了20%;若开始时只充入了2 mol M和 1 mol N的混合气体,达到平衡时M的转化率为
A.20% B.40% C.60% D.80%
12.反应2SO2+O2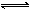 2SO3经一段时间后,SO3的浓度增加了0.4 mol·L-1,在这段时间内用O2表示的反应速率为0.04 mol·L-1·s‑1,则这段时间为
2SO3经一段时间后,SO3的浓度增加了0.4 mol·L-1,在这段时间内用O2表示的反应速率为0.04 mol·L-1·s‑1,则这段时间为
A.0.1 s B.2.5 s C.5 s D.10 s
11.1体积pH=2.5的盐酸与10体积某一元酸强碱溶液恰好完全反应,则该碱溶液的pH等于
A.9.0 B.9.5 C.10.5 D.11.0
10.心酮胺是治疗冠心病的药物,它具有如下结构简式:
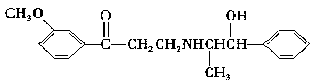
下列关于心酮胺的描述,错误的是
A.可以在催化剂作用下和溴反应 B.可以和银氨溶液发生银镜反应
C.可以和氢溴酸反应 D.可以与浓硫酸和浓硝酸的混合液反应
9、有一种白色粉末由等质量的两种物质混合而成,分别取适量该白色粉末置于三支试管中进行实验。
(1)逐滴加入6 mol·L-1盐酸,同时不断振荡试管,有气泡产生,反应结束后得到无色透明溶液
(2)加热试管中的白色粉末,试管口有水滴凝结
(3)逐滴加入6 mol·L1硫酸,同时不断振荡试管,有气泡产生,反应结束后试管中还有白色不溶物
下列混合物中符合以上实验现象的是
A.NaHCO3、AgNO3 B.BaCl2、MgCO3
C.NH4HCO3、MgCl2 D.CaCl2·6H2O、Na2CO3
8.若1.8 g某金属跟足量盐酸充分反应,放出2.24L(标准状况)氯气,则该金属是
A.Al B.Mg C.Fe D.Zn
7.久置空气中会发生颜色变化,但颜色变化不是由于跟氧气反应引起的物质是
A.过氧化钠固体 B.亚硫酸钠固体 C.硫酸亚铁晶体 D.苯酚晶体
6.下列分子中含有的电子数目与HF相同,且只有两个极性共价键的是
A.CO2 B.N2O C.H2O D.CH4
29.抗击“非典”期间,过氧乙酸(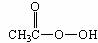 )是广为使用的消毒剂。它可由H2O2和冰醋酸反应制取,所以在过氧乙酸中常含有残留的H2O2。测定产品中过氧乙酸浓度c0涉及下列反应:
)是广为使用的消毒剂。它可由H2O2和冰醋酸反应制取,所以在过氧乙酸中常含有残留的H2O2。测定产品中过氧乙酸浓度c0涉及下列反应:
① MnO4_+ H2O2+ H+=== Mn2++ O2+ H2O
②H2O2+2I-+2H+===I2+2H2O
③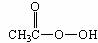 +2I-+2H+===CH3COOH+I2+H2O
+2I-+2H+===CH3COOH+I2+H2O
④I2+2S2O32-====S4O62-+2I-
请回答以下问题:
(1)配平反应①的离子方程式(配平系数填入答题卡相应的方框内):
MnO4_+ H2O2+ H+=== Mn2++ O2+ H2O
(2)用Na2S2O3标准溶液滴定I2时(反应④)选用的指示剂是 。
(3)取b0 mL 待测液,用硫酸使溶液酸化,再用浓度为a1 mol·L-1的KMnO4标准溶液滴定其中的H2O2,耗用KMnO4体积为b1 mL(反应①,滴定过程中KMnO4不与过氧乙酸反应)。
另取b0 mL 待测液,加入过量的KI,并用硫酸使溶液酸化,此时过氧乙酸和残留的H2O2都能跟KI反应生I2(反应②和③)。再用浓度为a2 mol·L-1的Na2S2O3标准溶液滴定生成的I2,耗用Na2S2O3溶液体积为b2 mL。
请根据上述实验数据计算过氧乙酸的浓度(用含a1、a2、a0、b1、b2的代数式表示)。
C0= 。
(4)为计算待测液中过氧乙酸的浓度c0 ,加入的KI的质量已过量但没有准确称量,是否影响测定结果 (填“是”与“否”)。
28.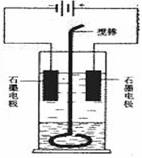 在玻璃圆筒中盛有两种无色的互不相容的中性液体。上层液体中插入两根石墨电极,圆筒内还放有一根下端弯成环状的玻璃搅棒,可以上下搅动液体,装置如右图。接通电源,阳极周围的液体呈现棕色,且颜色由浅变深,阴极上有气泡生成。停止通电,取出电极,用搅棒上下剧烈搅动。静置后液体又分成两层,下层液体呈紫红色,上层液体几乎无色。根据上述实验回答:
在玻璃圆筒中盛有两种无色的互不相容的中性液体。上层液体中插入两根石墨电极,圆筒内还放有一根下端弯成环状的玻璃搅棒,可以上下搅动液体,装置如右图。接通电源,阳极周围的液体呈现棕色,且颜色由浅变深,阴极上有气泡生成。停止通电,取出电极,用搅棒上下剧烈搅动。静置后液体又分成两层,下层液体呈紫红色,上层液体几乎无色。根据上述实验回答:
(1)阳极上的电极反应式为 。
(2)阴极上的电极反应式为 。
(3)原上层液体是 。
(4)原下层液体是 。
(5)搅拌后两层液体颜色发生变化的原因是 。
(6)要检验上层液体中含有的金属离子 ,现象是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com