
题目列表(包括答案和解析)
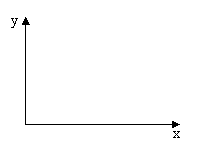
25、(11分)把a mol NH3、O2组成的混合气体
导入密闭反应器中,在催化剂存在下发生化学反应。
若混合气体中O2为x mol。反应生成的HNO3为y mol,
试确定O2的物质的量x取不同范围时,HNO3的物质的
量y的计算式,并画出相应的函数图象。
24、(8分)材料科学是近年来与化学有关的科学研究的特点,某新型无机非金属材料K由两种非金属元素组成,它是一种超硬物质,具有耐磨、耐腐蚀、抗冷热冲击、抗氧化的特性。它是以中学化学中的常见物质为原料来生产的,图中所示为其生产过程,其中虚线框内转化是为探究C的组成而设,G、F、H均难溶于水且为白色粉末,图中除M,K(均含A元素)外均为中学化学常见物质:
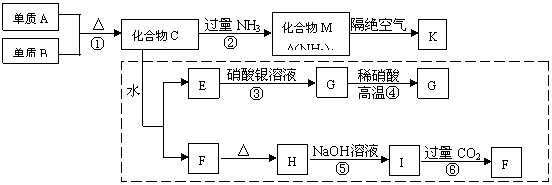
请回答下列问题:
(1)指出K可能所属的晶体类型 ,K晶体中A原子周围化学键的键角均相等,键角值为
(2)写出化学式:单质B ,化合物F
(3)写出下列反应的离子方程式:
反应③ 反应⑤
(4)写出反应④的化学方程式
23、(16分)(1)pH = 2的某酸H A与pH=12的某碱B(OH)
A与pH=12的某碱B(OH) 等体积混合后,溶液的pH = 8
等体积混合后,溶液的pH = 8
 ①反应所生成正盐的化学式为
;
①反应所生成正盐的化学式为
;
②该盐中 离子一定能水解,水解离子方程式为 ;
(2)试用离子方程式表示下列各变化
①将FeCl3饱和溶液滴入到沸水中 ;
②向①所得的混和物中逐滴加入盐酸: ;
其现象为 ;
③向FeCl3溶液中滴加KSCN ;
若向FeCl3溶液中先加入NaF;再加入KSCN则看不到溶液呈红色,其原因不可能是
(填序号,多选倒扣分)
A、Fe3+强氧化性将F-氧化
B、Fe3+与F-形成复杂的稳定的化合物
C、Fe3+与F-发生双水解转化为Fe (OH)3沉淀
④若向FeCl3溶液中先加入足量的HCl,再加入NaF和KSCN,则仍能显血红色,其原因是 。
22、(12分)已知电极材料:铁、铜、银、石墨、锌、铝;电解质溶液;CuCl2溶液、HNO3浓溶液、盐酸,按要求回答下列问题:
(1)电工操作中规定不能把Cu导线和铝导线绞拧在一起做为连接使用,请说明原因
(2)若电极材料为Cu和铝,电解质溶液为浓HNO3,能否形成原电池? ;
若能,写出电极反应式,正极
负极 ,若不能请说明理由
(3)在右框中画出简图,
使反应Cu + 2H+ = Cu2+ + H2 ↑
能够发生,并指出电极材料和电
解液的试剂。
(4)通常所说的燃料电池都是以铂为电极,将燃烧反应的化学能转化为电能,在燃料电池中,可燃物在 极反应, 在另一极反应。
21、(7分)由短周期元素组成的电子数相等的四种离子A-、B+、C2+、D3+。已知A-与B+、C2+、D3+均能反应,其反应现象如下:
|
|
B+ |
C2+ |
D3+ |
|
A- |
加热生成气体 |
生成白色沉淀 |
生成白色沉淀,当A过量时沉淀消失 |
(1)写出A-的电子式:
(2)写出离子方程式:
A-+ B+
A- + C2+
A-(过量)+ D3+
20、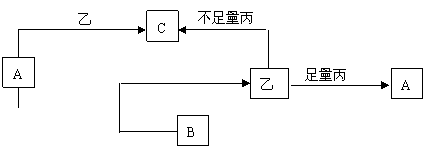 (10分)一定条件下发生如图所示的转化关系,其中A、B、C为中学化学中常见元素的化合物,甲、乙、丙均为单质。
(10分)一定条件下发生如图所示的转化关系,其中A、B、C为中学化学中常见元素的化合物,甲、乙、丙均为单质。
(1)若A是CO2,甲能在A中剧烈燃烧 ①化合物B的电子式为 ,
单质丙分子式 ;②现有下列药品和制气装置:实验药品:a.氯酸钾 b.大理石
c.过氧化钠 d.二氧化锰 e.甲酸 f.浓硫酸 g.稀硫酸 h.浓硝酸 i.双氧水 j蒸馏水
可供选择的制气装置:
如要选出其中一种装置,再选择上述所给的一些药品,既可以制取CO2,又可以制取气体丙,该装置最好选择 (填数字代号),制取CO2应选用的药品是 ,制取气体丙的化学反应方程式
③已知实验室常用浓硫酸与甲酸加热反应制取气体C,则可选择的制气装置是
(2)若A、B、C均为溶液,单质乙在常温下为液态,反应均在溶液中进行,写出A与甲按物质的量之比为1:1发生反应的离子方程式
。
19、(8分)(1)通常实验室把金属钠保存在装有一定量煤油的大口试剂瓶中,请具体说明在实验中,你将如何从试剂瓶中取用金属钠。(4分)
(2)试用所学知识解释在常温下Al很难与水反应,但却能与NaOH溶液反应放出H2。(4分)
|
9 |
10 |
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
|
|
|
|
|
|
|
|
|
|
|
第Ⅱ卷(非选择题,共78分)
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
|
|
|
|
|
|
|
|
18、把7.4g十水碳酸钠和小苏打组成100 ml溶液,c (Na+) = 0.6 mol/L,若把等质量的混合物加热到恒重时,则残留物的质量是 ( )
A. 7.4g B. 3.18g C. 5.2g D. 无法计算
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com