
题目列表(包括答案和解析)
23.(8分)用来治疗炭疽病的抗生素环丙沙星的结构简式如下图所示:

(1)环丙沙星的化学式为__________。
(2)环丙沙星可能发生的有机反应类型有__。(填字母代号)
A.取代反应 B.加成反应 C.消去反应 D.酯化反应 E.银镜反应
(3)lmol环丙沙星在金属Ni催化下最多可结合氢气的物质的量为___。
22.(10分)下图表示中学化学中常见物质间的转化关系:
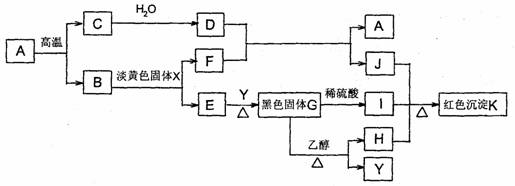
回答下列问题:
(1) x的电子式是_____。
(2)写出化学式:A____;K______。
(3)写出下列反应的化学方程式①D十F→;②G+乙醇→
21. (8分)某二元酸(用H2A 表示)在水中的电离方程式是:
H2A =H+ + HA-; HA- H++A2-。
H++A2-。
回答下列问题:
(1) Na2A溶液显__(填“酸性’、“中性”或“碱性”),理由是(用离子方程式表示)__。
(2)若0.lmol/L NaHA溶液的pH=2、则0.lmol/L H2A溶液中氢离子的物质的量浓度可能是0.11 mol/L(填“<”、“=”、或“>”)理由是____。
20.(14分)某化学兴趣小组用含有铝、铁、铜的合金制取纯净的氯化铝溶液、绿矾晶体和胆矾晶体,以探索工业废料的再利用。其实验方案如下:
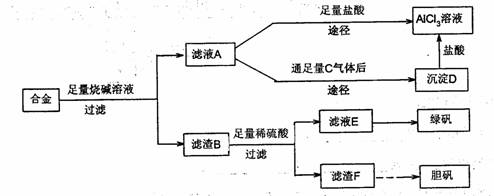
试回答下列问题:
(1)过滤用的器材已有:滤纸、铁架台、铁圈和烧杯,还要补充的玻璃仪器是_____。
(2)由滤液A制得AlCl3。溶液有途径I和II两条,你认为合理的是__,理由是__。
(3)从滤液E中得到绿矾晶体的实验操作是___。
(4)写出用滤渣F制备胆矾晶体的化学方程式________。
⑸有同学提出可将方案中最初溶解合金的烧碱改用盐酸,重新设计方案,也能制得三种物质,你认为后者的方案是否更合理______,理由是________。
19.(8分)某同学为测定一定质量的钠与水反应产生H2体积,
设计了右图装置进行实验。(固定装置省略)
(1)实验开始,欲使钠与水接触反应,应如何操作?____。
(2)反应开始后,试管中能观察到的现象是___。
(3)己知有关物质的密度ρ(K):0.86g/cm3 、 ρ (Na): 0.97g/ cm3 、 ρ(煤油):0.8g/ cm3 。如果将钠换成相同大小的钾进行上述实验,结果钾反应完所用的时间比钠反应完所用的时间_(填“长”或“短,’),其原因是___。
18.将0.2mol/L的KOH溶液与0.lmol/L的H2SO3溶液等体积混合后,溶液中各粒子浓度大小关系正确的是
A.c(K+)+c(H+)=c(OH-)+c(HSO3-)+c(SO32-)
B.c(K+)+c(OH-)=c(H+)+2c(SO32-)+3c(HSO3-)+4c(H2SO3)
C.c(K+)>c(SO32-)>c(HSO3-)>c(H2SO3)
D.c(SO32-)+c(HSO3-)+c(H2SO3)=0.lmol/L
第II卷(非选择题,共78分)
17.在反应11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4中,7.5mo1 CuSO4可氧化的P 原子的物质的量为
A.1.5mol B.2.5mol C.3mol D.5.5mol.
16.通以相等电量,用惰性电极分别电解足量的硝酸银和硝酸亚汞(亚汞的化合价为+1)溶液,若被还原的硝酸银和硝酸亚汞的物质的量之比为2:1,则下列表述正确的是
A.两个阴极产物的物质的量之比为n(Ag):n(Hg)=2:1
B.两个阳极产物的物质的量不相等
C.硝酸亚汞的化学式为HgNO3
D.电解过程中,阳极附近溶液的pH值逐渐下降
15.向0.2mol NaOH和0.1mo1 Ba(OH)2的溶液中持续稳定地通入6.72L(标准状况)CO2气体。下列表示溶液中离子的物质的量与通入CO2的体积关系的图象中,符合题意的是,(气体的溶解和离子的永解都忽略不计)

14.氢氧燃料电池是将多孔镍电极放置在KOH溶液中,然后分别向两极通入H2和O2,即可产生电流。下列叙述中正确的是
A.通入H2的电极为正极
B.正极的电极反应式为O2+2H2O+4e-= 4OH-
C.工作时,负极区溶液pH降低
D.工作时,溶液中的阴离子移向正极
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com