
题目列表(包括答案和解析)
28、(3分×4+1分);⑵40%;⑶小于,α22,1+α1
27、(3分×4)
(1)请写出这一系列烷烃化学式的通式 _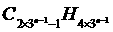 。
。
(2)请写出这一系列烷烃中第6种烷烃的化学式 _ C485H972_______________。
(3)碳元素质量分数约为 _85.7%_ (保留三位有效数字)。
(4)请写出它们化学式的通式
________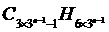 _____ 。
_____ 。
26、(3分)(1)该反应的化学方程式是 SiO2+Na2CO3+CaF2==2NaF+CO2↑+CaSiO3 (2分)(2)转移的电子数可能是下列数值中的 B、D(序号)
A、10 B、24 C、32 D、96
(3分) (3): 96.3%
|
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
19 |
20 |
21 |
22 |
23 |
24 |
25 |
|
D |
AB |
D |
AD |
D |
C |
C |
B |
BD |
C |
D |
D |
B |
D |
C |
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
B |
D |
D |
B |
D |
D |
B |
B |
D |
B |
32、(8分)将一块部分被氧化的Na投入盛满水的且倒置于水槽内的容器中,最终在容器中可收集到448mL(标况)气体.以电火花引燃容器里的气体,气体的体积最终减少到112mL(标况),经测知,水槽和容器内溶液总体积为800mL.溶液的PH值为13.求金属钠及其各种氧化产物的物质的量.
31、(4分)为了测定固体样品中Br-的含量,可用0.2mol/L硝酸银溶液去滴定已称重的样品溶液,为省去繁琐的计算 ,当取的样品质量为某数据时,滴定所用硝酸银溶液的毫升数恰好等于样品中Br-的质量分数的100倍.试确定固体样品的质量是多少克?
30、四氯化锡常温下是无色液体,在空气中极易水解,熔点-36℃,沸点114℃,金属锡的熔点为231℃,拟利用图中的仪器,设计组装一套实验装置,用熔融的金属锡跟干燥的氯气直接作用制取无水四氯化锡(此反应过程放出大量的热)。请回答下列各问题。
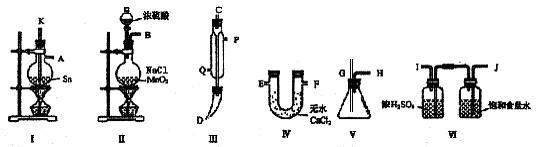
(1)用玻管(未画出)连接上述装置,正确的顺序是(填各接口的代码字母)________接________、________接________、________接________、________接________、________接________。(4分)
(2)装置Ⅵ的作用是___________;装置Ⅳ的作用是_____________。
(3)冷凝管理冷却水的流向是从__________进入,从__________流出。
(4)实验时应先点燃_____________处酒精灯,加热温度应大于______________℃,待__________即可停止加热。
(5)已知四氯化锡遇水强烈水解,产物之一是固态二氧化锡,那么四氯化锡水解的化学方程式为________。
(6)如果将制取的四氯化锡少许暴露于空气中,预期可看到的现象是____________。
(7)为了防止污染空气,在装置的最后应____________。
29、(4分×4)已知乙醛甲基上的氢原子是α氢原子,活性较大,可以与醛类中的醛基发生反应,如:
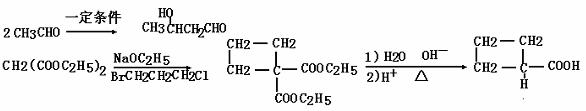
现由乙烯和丙二酸等物质合成I,合成路线如下:
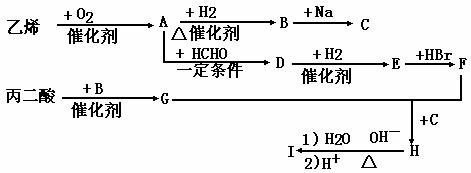
试回答下列问题:
(1)写出下列物质的结构简式:
E、______________________ H、_________________________ I、________________
(2) 写出A生成D的化学方程式(有机物写出结构简式)
_________________________________________________________________
28、(3分×4+1分)1000℃时,某容器中乙烷分解达平衡:
C2H6(气)⇌C2H4(气)+H2(气),平衡常数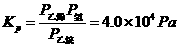 (式中P氢等均为各气体成分的分压)⑴平衡时容器中总压为P1,C2H6离解率为α1,则Kp的表达式为:Kp(P1, α1)= ;
(式中P氢等均为各气体成分的分压)⑴平衡时容器中总压为P1,C2H6离解率为α1,则Kp的表达式为:Kp(P1, α1)= ;
⑵P1=2.1×105Pa时,α1= ;
⑶恒温,将容器的容积扩大至原平衡的D倍,再达平衡时,C2H6离解率变为α2。α1与α2的关系为:α1 α2(大于、小于或等于)
Kp的表达式为: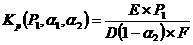 ,
,
式中E= ,F= 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com