
题目列表(包括答案和解析)
17.

在一定条件下(不需添加另的反应物),经不同的化学反应,可实现如上图的各种变化。其中,反应③④⑤属氧化还原反应,而反应①、②属非氧化还原反应。X、F和Y为单质,且F是空气的主要成份之一,其余为化合物,据此请填空:
⑴物质A是 ,F是 ,X是 ,Y是 。
⑵写出反应②的化学方程式: 。
⑶写出反应④的化学方程式,并注明反应条件: 。
16.(5分)请写出10个分子式,使每个分子中都含有18个电子。
、 、 、 、 、
、 、 、 、 。
15.(6分)若以X、Y和Z代表三种元素,且知X与Y可形成原子数之比为1:1的化合物甲,Y与Z也可形成原子数之比为1:1的化合物乙,又知甲分子含18个电子,乙分子含38个电子,请填空:
⑴元素Y在第 周期。⑵化合物甲的分子式是 。
⑶化合物乙的分子式是 。
14. (13分)1,2,3,4-四氢化萘的结构简式是
,分子式是C10H12。常温下为无色液体,有刺激性气味,沸点207℃,不溶于水,是一种优良的溶剂,它与液溴发生反应:C10H12+4Br2 C10H8Br4+4HBr。生成的四溴化萘常温下为固态,不溶于水。有人用四氢化萘、液溴、蒸馏水和纯铁粉为原料,制备少量饱和氢溴酸溶液,溶液实验步骤如下:①按一定质量比把四氢化萘和水加入适当的容器中,加入少量纯铁粉。②慢慢滴入液溴,不断搅拌,直到反应完全。③取下反应容器,补充少量四氢化萘,直到溶液颜色消失。过滤,将滤液倒入分液漏斗,静置。④分液,得到的“水层”即氢溴酸溶液。
(13分)1,2,3,4-四氢化萘的结构简式是
,分子式是C10H12。常温下为无色液体,有刺激性气味,沸点207℃,不溶于水,是一种优良的溶剂,它与液溴发生反应:C10H12+4Br2 C10H8Br4+4HBr。生成的四溴化萘常温下为固态,不溶于水。有人用四氢化萘、液溴、蒸馏水和纯铁粉为原料,制备少量饱和氢溴酸溶液,溶液实验步骤如下:①按一定质量比把四氢化萘和水加入适当的容器中,加入少量纯铁粉。②慢慢滴入液溴,不断搅拌,直到反应完全。③取下反应容器,补充少量四氢化萘,直到溶液颜色消失。过滤,将滤液倒入分液漏斗,静置。④分液,得到的“水层”即氢溴酸溶液。
回答下面问题:
⑴下面示意图中的装置,适合步骤①和②操作的是 。
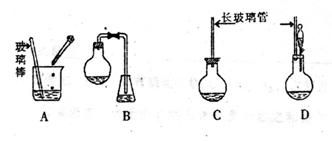
⑵步骤②中如何判断“反应完全” 。
⑶步骤③中补充少量四氢化萘的目的是 。
⑷步骤③中过滤后得到的固体物质是 。
⑸已知在实验条件下,饱各氢溴酸水溶液中氢溴酸的质量分数是66%,如果溴化反应进行完全,则步骤①中四氢化萘和水的质量比约是1: (保留小数点后1位)。
13.(6分)把淀粉溶液溶于沸水中,制成淀粉胶体。
⑴鉴别水溶液和胶体可以利用的方法是
。
⑵60℃左右时,在淀粉胶体中加入淀粉酶,充分反应。然后把反应后的全部液体装入半透膜里,系紧袋口,并把它悬挂在盛有蒸馏水的烧杯里。从半透膜袋里析出的物质是 ,该操作的名称是 。

12. 苯并[a]芘是一种稠环芳香烃(它的分子是研究致癌效应的参照标准),其结构式中有5个环互相并合如图。每外碳原子上都有一个双键(C=C),分子中共有m个双键,五个原子数为n个,则m、n分别等于
苯并[a]芘是一种稠环芳香烃(它的分子是研究致癌效应的参照标准),其结构式中有5个环互相并合如图。每外碳原子上都有一个双键(C=C),分子中共有m个双键,五个原子数为n个,则m、n分别等于
A 10,30 B 10,32 C 11,30 D 11,32
第Ⅱ卷
(共四大题,9小题,共76分)
11.下列说法正确的是
A 电解NaOH溶液时,溶液浓度将减小,pH增大
B 电解H2SO4溶液时,溶液浓度将增大,pH减小
C 电解Na2SO4溶液时,溶液浓度将增大,pH不变
D 电解NaCl溶液时,溶液浓度将减小,pH不变
10.A和M为两种元素,已知A位于短周期,且A2-与M+的电子数之差为8,则下列说法正确的是
A A和M原子的电子总数之和可能为11 B A和M的原子序数之差为8
CA和M原子的最外层电子数之和为8 D A和M原子的最外层电子数之差为7
9.在一杯透明的液体中加入一小颗固体,整杯液体完全转变成固体,则原溶液和析出的固体分别可能是
A过饱和溶液,不带结晶水的晶体 B 饱和溶液,带结晶水的晶体
C过饱和溶液,带结晶水的晶体 D –10℃的过冷水,冰
8.某溶液中含三种离子,加入过量氨水有沉淀生成 ,过滤后滤液中加过量盐酸,又有沉淀生成,再过滤,滤液中加入过量Na2CO3溶液,仍有沉淀生成,原溶液中含有的离子可能是
A Ag+、Fe2+、Ca2+ B Al3+、Mg2+、Ba2+ C Ca2+、Fe2+、Ba2+ D Ag+、Mg2+、Ba2+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com