
题目列表(包括答案和解析)
2.“神舟五号”飞船发射成功,表明我国载入航天技术已达到世界先进水平。在运送飞船的某些火箭推进器中盛有液态肼 和液态氧化剂
和液态氧化剂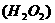 ,它们充分混合反应后的产物之一是
,它们充分混合反应后的产物之一是
A.氮气 B.氧气 C.氨气 D.氢气
1.据报道,用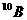 合成的
合成的 有很好的抗癌治癌作用。下列叙述正确的是
有很好的抗癌治癌作用。下列叙述正确的是
A.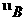 与
与 互为同位素 B.
互为同位素 B.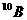 与
与 互为同分异构体
互为同分异构体
C.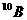 的质子数与中子数相等 D.
的质子数与中子数相等 D.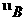 与
与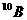 的核外电子数相差1
的核外电子数相差1
26、(10分)将多磷酸钠溶液通过氢型阳离子交换柱,进行Na+与H+的交换,得到多磷酸,其结构为:
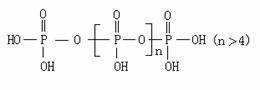
交换后的溶液用0.1 mol/L的NaOH溶液滴定。在消耗NaOH溶液42.0mL和50.00 mL时各有一个滴定终点。请回答:
(1)有两个滴定终点的原因是 。
(2)求结构中的n值。
25、(8分)将等物质的量的氧化铝、氧化铁的混合物溶于100mL硫酸中,而后逐滴加入1.00mol/lNaOH溶液。当加入的NaOH的体积V1=50mL时,开始有沉淀析出,且沉淀量随NaOH加入量逐渐增加。当NaOH的体积V2=650mL时,沉淀量达到最大值,继续滴加NaOH时,沉淀量逐渐减小。当V3≥750mL时,沉淀量不再改变。
计算(1)所用硫酸的物质的量浓度。
(2)混合物中氧化铝的质量
24、(10分)青霉素(C16H18N2O4S)的结构简式为
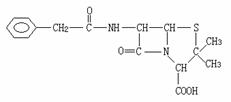
它是人们经常使用的一种抗生素,但是经过多年的使用,不少病菌对青霉素产生了抗药性,为此科学家又研制了一种新的青霉素-氨苄青霉素来代替青霉素。
下图是由青霉素制取氨苄青霉素的合成路线:
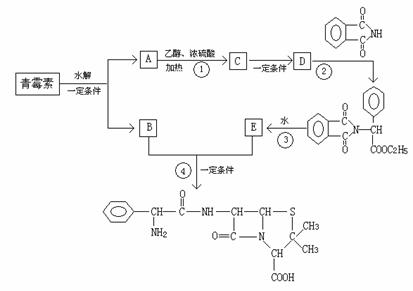
已知:有机物分子中和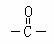 相连的碳原子称为α-碳原子,其上面连着的氢原子称为α-氢原子,在一定条件下,α-氢原子易被取代。请回答下列问题:
相连的碳原子称为α-碳原子,其上面连着的氢原子称为α-氢原子,在一定条件下,α-氢原子易被取代。请回答下列问题:
(1)从下列选项中,写出反应①②③④的反应类型:
① ②
③ ④
(2)写出D的结构简式
(3)写出反应①、③的化学方程式
①
③
23、(8分)某有机物含C、H、N、O四种元素,下图为该有机物球棍模型。
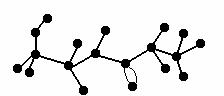
(1)该有机物的化学式为 ,结构简式为 。
(2)该有机物可能发生的化学反应有(填序号)
①水解 ②加聚 ③取代 ④消去 ⑤酯化
(3)该有机物发生水解反应的化学方程式为
22、(9分)A、B、C、D是中学化学中常见的四种化合物,它们分别由两种元素组成。甲、乙、丙是单质,甲、丙、A、C、D常温下均为气体,B为液体。这些单质和化合物之间存在如下关系:
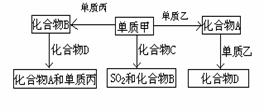
⑴写出B物质的分子式: 。
⑵写出下列A物质的电子式:
⑶写出单质甲跟化合物C反应,生成SO2和化合物B的化学方程式 。
⑷在密闭容器中,化合物B跟化合物D在高温下生成A和单质丙的反应是可逆反应,其化学方程式为 ;反应达平衡后,若增大体系的压强,该平
衡 (填向左移动、向右移动、不移动);其理由是 。
21、(11分)A、B、C、D均为短周期元素。A、B可形成两种液态化合物,其最简式分别为BA和B2A。A与D可形成气态化合物DA、DA2。A、B、D可组成离子化合物,该晶体化学式为B4A3D2,其水溶液呈弱酸性。B与D可形成一种极易溶于水的碱性气体X。B与C可形成极易溶于水的酸性气体Y。已知X分子与B2A分子中的电子数相等。Y分子与最简式为BA的分子中的电子数相等。请回答:
(1)写出元素的名称:A , C
(2)Y分子是 分子(填极性或非极性)。
(3)写出下列反应的化学方程式并标明电子转移的方向和数目
①C2+(BA)n→A2
②C2+X(过量)→D
(4)B4A3D2水溶液呈酸性,写出其呈酸性的离子方程式
(5)已知液态X与B2A相似,也可以发生微弱的电离,电离出含有相同电子数的微粒,则X的电离方程式为:
20、(12分)氧化二氯是棕黄色刺激性气体,熔点:-116℃,沸点:3.8℃。氧化二氯不稳定,接触一般有机物易爆炸;它易溶于水(1:100),同时反应生成次氯酸溶液。制备出之后要冷却成固态以便操作和贮存,制备少量Cl2O,是用干燥的氯气和HgO反应(还生成HgO•HgCl2)。装置示意如图,铁架台和夹持仪器已略去)
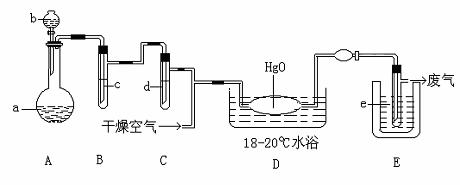
(1)A中盛有的固体深色试剂a是 ,分液漏斗中试剂b是
(2)B中盛有液体c是 ,C中的液体d是
(3)D中所发生反应的化学方程式是
(4)E中的保温瓶中盛有致冷剂,它应是 (在干冰、冰水、液态空气中选择),在E的内管得到的氧化二氯中可能含有杂质是
(5)装置A、B、C间的连接方式与D、E间的连接方式有明显的区别,这区别是
,用这些不同的连接方式的主要理由是 。
19、(1)(5分)通常实验室把金属钠保存在装有一定量 的大口试剂瓶中,现需要观察金属钠在空气中被氧化的过程,具体实验中需要用到的实验用品有 、 、 、 。
(2)(5分)现有一瓶醋酸,要测定其中已电离的CH3COOH分子的占原溶液中醋酸分子总量(包括已电离和未电离的)的百分率,其实验方案如下:(1)先测定溶液的PH,其操作方法是 ,测量溶液PH值的目的是 。
(2)再做 实验(填写实验名称),目的是 。将以上测定所得数据进行处理即可达到实验目的。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com