
题目列表(包括答案和解析)
(二)能力点提示:
1.几种气态烃的实验室制法:
(1)制甲烷
CH3 COONa+NaOH CH4↑+Na2CO3
CH4↑+Na2CO3
要注意断键部位,这也正是要在无水环境中进行的原因;该反应是减少一个碳原子的反应, 如
制乙烷
CH3CH2COONa+NaOH  C2H6↑+Na2CO3
C2H6↑+Na2CO3
制苯
C5H5COONa+NaOH C6H6+Na2CO3
C6H6+Na2CO3
(2)制乙烯
要注意温度控制在170℃左右;该反应是单键变双键的一种反应,如用异丙醇制丙烯:
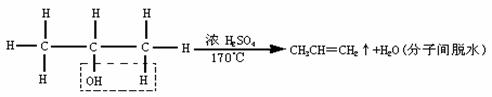
(3)制乙炔
电石与水反应制乙炔时,常伴有特殊难闻的气味,是因为发生以下反应所至:
CaS+2H2O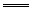 Ca(OH)2+H2S
Ca3P2+6H2O
Ca(OH)2+H2S
Ca3P2+6H2O 3Ca(OH)2+2PH3
3Ca(OH)2+2PH3
Ca3As2+6H2O 3Ca(OH)2+2AsH3↑
3Ca(OH)2+2AsH3↑
2.取代反应的特征
在与卤素单质发生取代反应的过程中,烷烃分子每去掉一个氢原子换上一个卤素原子要消耗1个卤素分子,另外一个卤素原子则与换下来的氢原子结合生成卤化氢(这一点与加成反应是 不同的)。因此烷烃与卤素单质发生取代反应的最大物质的量之比为:CnH2n+2-(2 n+2)X2(卤素单质)
3.加聚反应的书写及高聚物单体的判断
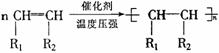 (1)加聚反应的写法:
(1)加聚反应的写法:
① 单烯烃的加聚反应为:
② 共轭二烯烃的加聚反应为:
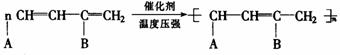
(R1、R2、A、B可以是-H、-CH3、-C2H5或其它基团)
③不同单体加聚时还要考虑可能有不同的连接方式。例如苯乙烯与乙烯间的加聚反应:
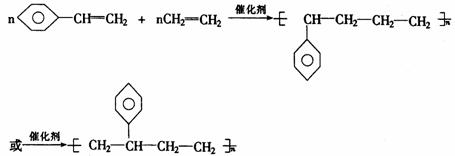
(2)高聚物单体的判断
①聚乙烯型
链节为两个碳原子的,则其单体看作乙烯型,如:
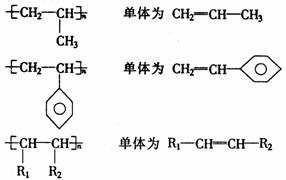
②1,3-丁二烯型
链节为四个碳原子,且2,3碳原子间有C=C,则应对应1,3-丁二烯找单体,如:

③混合型
(ⅰ)当链节有四个碳原子,且C、C间无C=C时,应视为含有2个乙烯型单体,如:

(ⅱ)当链节更长时,首先看有无C=C,若有,则与C=C相边的左 右各一个C原子,共同看
作1,3-丁二烯型,其余C原子每两个看作一个乙烯型结构。如:

4.同分异构体的书写
(1) 同分异构体书写通常是按碳链异构 位置异构
位置异构 官能团异构的顺序书写,也可 按官能团异构
官能团异构的顺序书写,也可 按官能团异构 碳链异构
碳链异构 位置异构的顺序书写。例如写出分子式为C4H8的同分异构体时,首先按碳链异构写出:
位置异构的顺序书写。例如写出分子式为C4H8的同分异构体时,首先按碳链异构写出:
① CH2=CH-CH2-CH3 1-丁烯
②CH2=C-CH3 乙-甲基-1-丙烯,再按位置异构写有:
|
CH3
③CH3-CH=CH-CH3 2-丁烯
④CH3-C=CH2 与②式相同排除,最后按官能团异构写有:
|
CH3
 甲基 环丙烷。注意,烷烃没有官能团异构和位置异构,只有碳链异构,因此,碳原子数相同烷烃
和不饱和烃相比,其同分异构体数目要少。
甲基 环丙烷。注意,烷烃没有官能团异构和位置异构,只有碳链异构,因此,碳原子数相同烷烃
和不饱和烃相比,其同分异构体数目要少。
(2)苯环上同分异构体的书写
①苯和甲苯都没有同分异构体,乙苯等其他苯的同系物,由于取代基在苯环上的相对位置不 同因此存在同分异构体。
分子式为C8H10的同分异构体有四种:
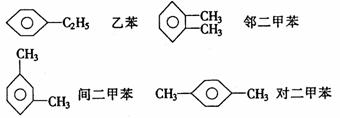
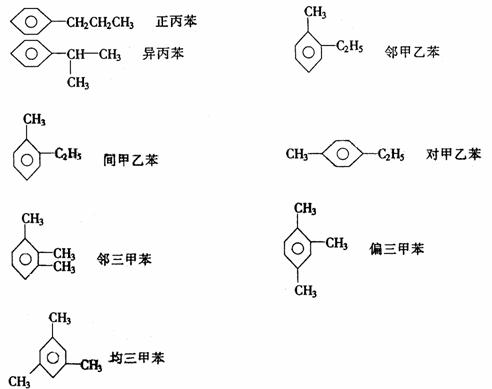
分子式为C9H12的同分异构体有8种:
 E
E
②苯的同系物被一个原子团取代,如:
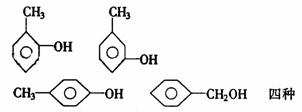
二甲苯的取代
邻二甲苯的一氯代物:
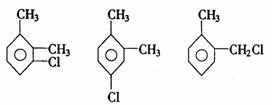
间二甲苯的一氯代物:
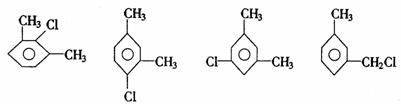
对二甲苯的一氯代物:
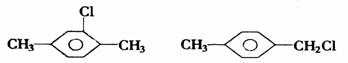
判断因取代基位置不同而形成的同分异构体时可采用“对称轴”法。即在被取代的主体结构 中,划对称轴,取代茎只能在对称轴的一侧,或是在对称轴上而不能越过对称轴(针对一元取代物而言)。如二甲苯的对称轴如下(虚线表示):
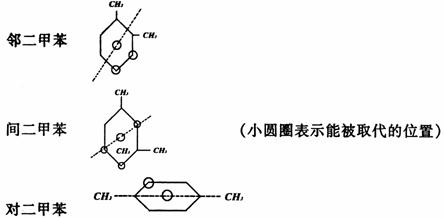
因此,邻、间、对二甲苯苯环上的一元取代物分别有2、3、1种。
5.计算并推断烃的分子式及其结构简式
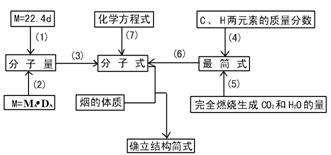
注:
(1)气体摩尔质量=22.4L/mol ×dg/L(d为标准状况下气体密度).
(2)某气体对A气体的相对密度为DA,则该气体式量M=MADA.
(3)由烃的分子量求分子式的方法:
①M/14,能除尽,可推知为烯烃或环烷烃,其商为碳原子数;
②M/14,余2能除尽,可推知为烷烃,其商为碳原子数;
③M/14,差2能除尽,推知为炔烃或二烯烃或环烯烃,其商为碳原子数。
④M/14,差6能除尽,推知为苯或苯的同系物。
6.烃完全燃烧的有关规律
(1)等物质的量的烃(CnHm)完全燃烧时,耗氧量的多少决定于n+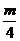 的值,n+
的值,n+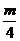 的值越大,耗氧量越多,反之越少。
的值越大,耗氧量越多,反之越少。
(2)等质量的烃(CnHm)完全燃烧时,耗氧量的多少决定于氢的质量分数,即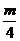 的值,
的值,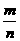 越大,耗氧量越多,反之越少。
越大,耗氧量越多,反之越少。
(3)等质量的烃(CnHm)完全燃烧时,碳的质量分数越大,生成的CO2越多,氢的质量分数越大,生成的H2O越多。
(4)最简式相同的烃无论以何种比例混合,都有:①混合物中碳氢元素的质量比及质量分数 不变;②一定质量的混合烃完全燃烧时消耗O2的质量不变,生成的CO2的质量均不变。
(5)对于分子式为CnHm的烃:
①当m=4时,完全燃烧前后物质的量不变;
②当m<4时,完全燃烧后物质的量减少;
③当m>4时,完全燃烧后物质的量增加.
7.各类烃与H?2加成的物质的量之比:
|
不饱和烃 |
与H2加成的最大物质的量之比 |
|
烯烃 |
1∶1 |
|
二烯烃 |
1∶2 |
|
炔烃 |
1∶2 |
|
苯及其同系物 |
1∶3 |
苯乙烯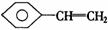 |
1∶4 |
8.二烯烃1,4加成的规律:
只有具备R′-CH=CH-CH=CH-R结构特点的二烯烃才能进行1,4加成,其与卤素单质的加成产物为 :
R′-CH=CH-CH=CH-R
| |
X X
若二烯烃的结构为R-CH=CH-CH2-CH=CH-R′,则不能进行1,4加成,只能进行1,2加成.
9.根据烃的分子式推断其可能具有的结构
从烷烃通式CnH2n+2?出发,分子中每形成一个C=C键或形成一个环,则减少2个氢原子;分子中每形成一个C≡C键,则减少4个氢原子。依此规律可由烃的分子式推测其可能具有的结构,再由其性质可确定其结构简式。例如分子式为C5H8的烃可与等物质的量Br2加成,试推测其可能的结构并写出其结构简式.先根据其分子组成可知其分子比对应的C5 H12少4个氢原子,可能是二烯烃、炔烃或环烯烃,再根据其与Br2的加成比例可知
其为环烯烃,结构简式为 或
或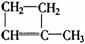 等。
等。
(一)知识点
1.有机化合物的主要特点:
有机物是以碳元素为基本组成元素的化合物。碳元素在有机化合物中形成四个共价键,构成碳链和碳环,与无机物相比有如下特点:
(1)分子结构复杂,种类繁多;
(2)多数难溶于水,易溶于有机溶剂;
(3)导电性差,多数有机物属于非电解质;
(4)多数有机物熔沸点低,易燃烧,受热易分解;
(5)有机反应复杂、副反应多,反应速率慢。
2.烃的分类及其通式

3.各类烃的结构特点及其重要性质
|
烃 |
结构特点 |
重要化学性质 |
|
烷烃 |
链烃、C-C键 |
稳定、取代(特征反应)、氧化(燃烧)、裂解 |
|
烯烃 |
链烃、C=C键 |
不稳定,加成(特征反应)、氧化、加聚 |
|
炔烃 |
链烃、C C键 C键 |
不稳定,加成(特征反应)、氧化、加聚 |
|
二烯烃 |
链烃,2个C=C键 |
不稳定,加成(1,2加成和1,4加成)、氧化、加聚 |
|
苯及其 同系物 |
芳香烃,一个苯环 |
稳定,易取代,能加成,难氧化,苯的同系物侧链易被酸性KmnO4溶液氧化 |
4.同系物与同分异构体
(1)同系物:结构相似,在分子组成上相差一个或几个CH2原子团的物质互称为同系物。注意烷烃和环烷烃、烯烃和二烯烃不互为同系物。
(2)同分异构体:组成(分子式)相同,结构不同的化合物互称为同分异构体。因此碳原子数 相同的烯烃和环烷烃、炔烃和二烯烃互为同分异构体。
5.烃的系统命名法
(1)烷烃:以含碳原子数最多的碳链为主链,称某烷;若碳链上有取代基则作为支链,距支 链较近的一端为起点对碳原子编号命名。若有多个取代基时,按由小到大顺序命名。
(1) 烯烃和炔烃:以含碳碳双键或碳碳叁键的最长碳链为主链命名为某烯或某炔;从距C=C 或C≡C较近的一端为起点对主链碳原子编号;取代基名称写在前面,取代基和双键、叁键的个数用中文二、三等标出,并用阿拉伯数字1,2等标明C=C或C≡C所在位置。如:
CH3-C=CH-CH3
|
CH3
名称:2-甲基 -2-丁烯.
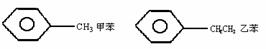
(2) 苯及其同系物:以苯环为母体,先命取代基,再命名苯环,如:

6. 煤和石油
煤和石油
(1)石油是由各种烷烃、环烷烃和芳香烃组成的复杂混合物;
(2)石油的分馏原理;
(3)石油裂化和裂解的目的;
(4)煤的干馏和干馏产物.
7.有关计算
(1)通过计算判断或确定烃的分子组成和结构;
(2)通过烃的燃烧反应,计算烃、耗氧量和产物之间的数量关系。
8.甲烷、乙烯、乙炔的实验室制法及注意事项。
8.了解石油的成分、分馏、裂化和煤的干馏的基本原理及其广泛应用。
7.掌握各类烃有关燃烧反应的计算及其规律。
6.掌握烃的取代反应、加成反应、燃烧反应及加聚反应的化学方程式的书写及其特点,能判断高聚物的单体。
5.掌握甲烷、乙烯、乙炔的实验室制取原理、装置要求;掌握制溴苯、硝基苯的原理、装置特点和操作方法。
4.掌握烷烃、单烯烃和炔烃的系统命名法,能对物质名称和结构简式进行互译。
3.掌握同系物和同分异构体的书写和判断方法。
2.应用烃的组成、通式和性质的知识推断烃的分子式和结构简式。
1.理解烃的分子结构决定烃的化学性质。不同类别的烃的组成和结构决定了它们各自的化学 性质。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com