
题目列表(包括答案和解析)
13、已知CuSO4溶液分别与Na2CO3溶液、Na2S溶液的反应情况如下:
(1) CuSO4 +Na2CO3 主要:Cu2+ + CO32─ + H2O == Cu(OH)2↓+ CO2↑
次要:Cu2+ + CO32─== CuCO3↓
(2) CuSO4 +Na2S 主要:Cu2+ + S2─== CuS↓
次要:Cu2+ + S2─+ 2H2O == Cu(OH)2↓+ H2S↑
下列几种物质的溶解度大小的比较中,正确的是
A、CuS <Cu(OH)2<CuCO3 B、CuS >Cu(OH)2>CuCO3
C、Cu(OH)2>CuCO3>CuS D、Cu(OH)2<CuCO3<CuS
12、25℃时,将某强酸溶液和某强碱溶液按1∶10的体积比混合后,溶液恰好呈中性,则混合前此强酸与强碱的pH之和为
A、12 B、13 C、14 D、15
11、下列关于实验现象的叙述不正确的是
A、把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡
B、用锌片做阳极,铁片做阴极,电解氯化锌溶液,铁片表面出现一层锌
C、把铜片插入三氯化铁溶液中,在铜片表面出现一层铁
D、把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出的速率加快
10、下列四种溶液中,①pH=0的盐酸;②0.1mol/L的盐酸;③0.01mol/L NaOH溶液;④pH=11 NaOH溶液。由水电离生成的氢离子浓度之比(①∶②∶③∶④)是
A、1∶10∶100∶1000 B、0∶1∶12∶11
C、14∶13∶12∶11 D、14∶13∶2∶3
9、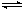 水的电离过程为H2O H+ + OH─,在不同温度下其平衡常数为K(25℃)=1.0×10-14,K(35℃)=2.1×10-14,则下列叙述正确的是
水的电离过程为H2O H+ + OH─,在不同温度下其平衡常数为K(25℃)=1.0×10-14,K(35℃)=2.1×10-14,则下列叙述正确的是
A、c(H+)随温度的升高而降低 B、水的电离过程是吸热的
C、水的电离平衡常数与浓度、温度有关 D、在35℃时,c(H+) > c(OH─)
8、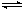 20℃时,1LH2S的饱和溶液,浓度约为0.1mol/L,其电离方程式为:第一步 H2S
20℃时,1LH2S的饱和溶液,浓度约为0.1mol/L,其电离方程式为:第一步 H2S
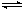 H+ + HS─;第二步 HS─ H+ + S2─。若要使该溶液的pH增大的同时,c(S2─)减小,可采用的措施是①加入适量的NaOH溶液;②加入适量的水;③通入适量的SO2;④加入适量硫酸铜固体;⑤加入少量盐酸
H+ + HS─;第二步 HS─ H+ + S2─。若要使该溶液的pH增大的同时,c(S2─)减小,可采用的措施是①加入适量的NaOH溶液;②加入适量的水;③通入适量的SO2;④加入适量硫酸铜固体;⑤加入少量盐酸
A、①③⑤ B、②④⑤ C、②③ D、③④⑤
7、下列事实能说明亚硝酸是弱电解质的是
A、亚硝酸钠溶液的pH大于7 B、用亚硝酸溶液做导电实验灯泡很暗
C、亚硝酸溶液不与硫酸钠反应 D、亚硝酸易分解产生NO、NO2
6、一种pH=3的酸溶液和一种pH=11的碱溶液等体积混合后测得溶液的pH=5.6其原因可能是
A.浓的强酸和稀的弱碱溶液反应 B.浓的弱酸和稀的强碱溶液反应
C.等浓度的强酸和弱碱溶液反应 D.生成了一种强酸弱碱盐
5、下列物质的溶液加热蒸干、灼烧后,所得的固体成份不相同的是
A、FeCl2、FeCl3 B、NaHCO3、Na2CO3
C、NaAlO2、AlCl3 D、Mg(HCO3)2、MgCl2
4、下列溶液中一定显碱性的是
A、溶液中:c(OH─)>c(H+) B、溶液的pH>7
C、滴加甲基橙后溶液显黄色 D、滴加甲基橙后溶液显红色
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com